写真は、120923、中2理科の授業です。
定期テスト3日前なので、120923から部活が停止ですね。
はりきって定期テスト範囲を勉強していきましょう。
理科の場合、学校だけだと、実験して終わり~とか★
その内容や意味を理解するのが難しいような気がします。
だから、ちゃんとした問題になったときに解けません。
学校が悪いわけではありません。
問題を解いて点を取るには、さらに自分の勉強が必要です。
それを助けるのは、塾などの仕事になりますね。
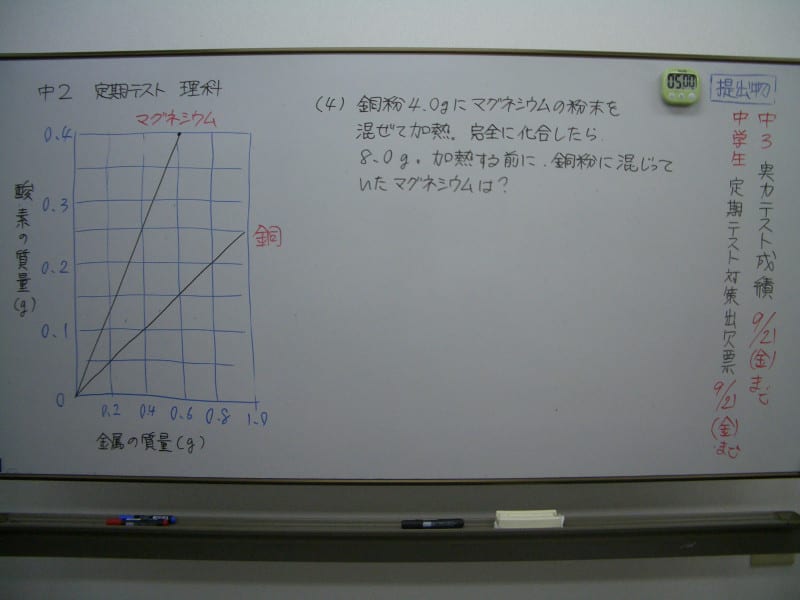
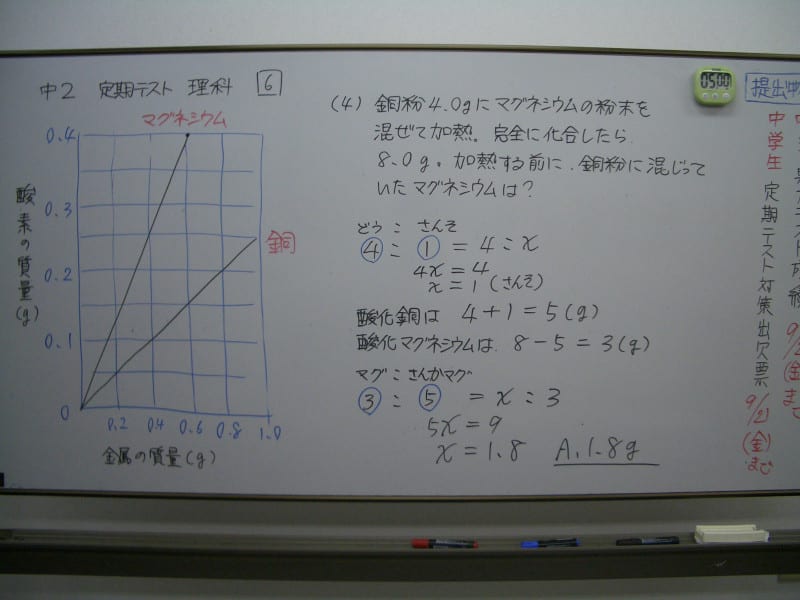
問題「銅粉4.0gにマグネシウムの粉末を混ぜて加熱し、完全に化合させたところ、酸化物全体の質量は8.0gになった。加熱する前に、銅粉に混じっていたマグネシウムの質量は何gか」
写真にあるグラフから、わかることを読み取っていってください。
まず「マグネシウム:酸素」は?
グラフのメモリのピッタリしたところが・・・。
「マグネシウム:酸素=0.6:0.4」です。
あとは、もっとも簡単な整数の比で表すことになります。
「マグネシウム:酸素=0.6:0.4=6:4=3:2」です。
次に「銅:酸素」は?
グラフのメモリのピッタリしたところが・・・。
「銅:酸素=0.4:0.1」です。
あとは、もっとも簡単な整数の比で表すことになります。
「銅:酸素=0.4:0.1=4:1」です。
下準備ができたところで、あとは計算していきましょう。
銅粉4.0gと化合する酸素の質量は?
「銅:酸素=4:1」から、比と比の値の式を作ります。
まあ、作らなくてもそのままでわかりますが、一応★
→ 4:1=4:x
4x=4
x=1
銅粉4.0gと化合する酸素の質量は1gとなります。
ということは、酸化銅の質量は?
銅と酸素をドッキングしてください。
→ 4+1=5
酸化銅は5gとなります。
だとすると、酸化マグネシウムの質量は?
酸化物全体の質量から、酸化銅の質量を引いてください。
→ 8-5=3
酸化マグネシウムの質量は3gとなります。
「マグネシウム:酸素=3:2」で化合するんでしたよね。
それなら、酸化マグネシウムの割合は・・・。
→ 3+2=5
したがって、「マグネシウム:酸化マグネシウム=3:5」です。
酸化マグネシウムは3gなので・・・。
加熱する前のマグネシウムを、比と比の値の式で求めましょう。
→ 3:5=x:3
5x=9
x=1.8
加熱する前のマグネシウムは、「1.8g」となります。
↑できましたか?
普段から個別で、中2の理科を勉強していなければ・・・。
テスト前だけ勉強しても、理論や計算は難しいかも★
できれば、普段から通塾、勉強するとよいと思います☆
---------------------------------------------------------------------