写真は、101123、中3期末テスト対策講座です。
101123、韓国が大変な目に遭っていますね。
なぜ、もっと国際的に「怒り」がないのでしょうか?
やたらと行動の分析をしたりして、冷静な、他人事な感じ・・・。
日本だって射程圏内。
いつどうなるかも、わからない気もします。
外交をしっかりやって、胸を張って安心して日々暮らせますように。
さて、いつもは対策講座で理社を勉強するのですが・・・。
この日は、期末テスト1日目の理科と数学を勉強しました。
社会(と英語)は、期末テスト2日目前日の101125に勉強しましょう。
国語(英語と数学も)は、先週の時点で勉強してしまいました。
イオンは、平成21年度から始まった移行措置の内容ですね。
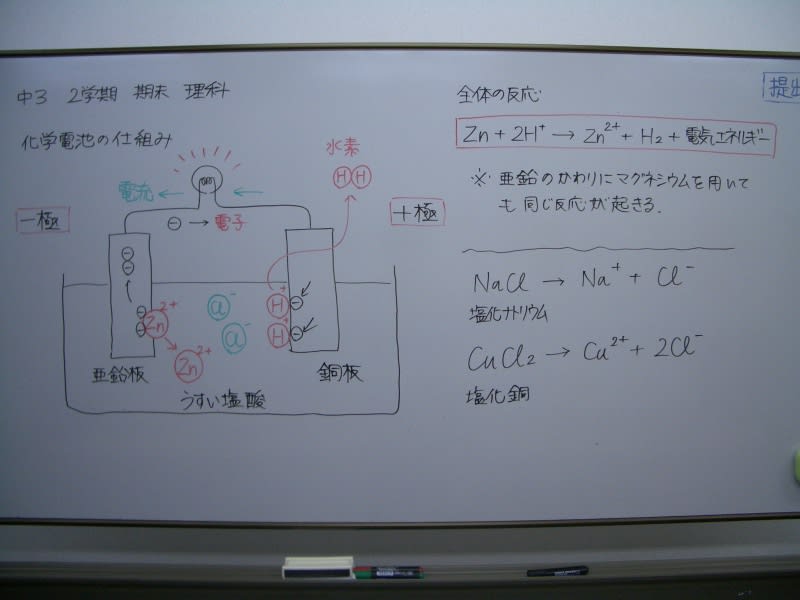
写真は、その中でも化学電池の問題です。
ちなみに、W・ボードに描かれている絵は、問題用紙にありません。
自分で覚えている、絵に描けるようにしておくべきものです。
これを覚えていないと、描けないと、問題を解くのは難しい★
一方の金属が、電子を失ってイオンになります。
その電子が導線を移動することによって、電流が生じます。
これを化学電池といいます。
問題は、以下のようなものです。
● 亜鉛板とその周辺で起こっていることはなにか
● 銅板とその周辺で起こっていることはなにか
● 銅板と亜鉛版、どちらが+極になっているか
ザックリですが、このような問題が出題されています。
W・ボードの絵が描ければ、すべて正解するでしょう。
亜鉛板に電子を残して、亜鉛がイオン「Zn2+」になります。
電子を導線に送り出すので、こちらが「-極」になります。
電子は導線を通って、銅板に移動します。
うすい塩酸(HCl)は・・・。
水素イオン「H+」と、塩素イオン「Cl-」に分かれています。
「H+」は、銅板から電子をもらいます。
すると「H+」は、水素原子「H」になります。
電子を受け取るので、こちらが「+極」になります。
さらに、水素原子2つがドッキング、「2H」の水素分子になります。
そして、銅板から気体(水素)として発生することになります。
亜鉛版のほうが「-極」、銅板のほうが「+極」です。
この流れの各部分が、そのまま解答になりますよ♪
全体の反応としては・・・。
「Zn + 2H+ → Zn2+ + H2 + 電気エネルギー」です。
ただ、この式までは問題にありませんでした。
電気がつくこと、電流の流れなどもありませんね。
「ビジュアル化できる」というのは、どんな教科にも使えます。
別のところには、実際に図で解答する問題もありましたよ。
それは、塩化銅(CuCl2)を水に溶かしたときのモデルです。
とにかく、絵を描けるようにしておくと理解が深まるでしょう☆