今回のキーワードは,オミクロン株では嗅覚障害の合併は少ない,オミクロン株はデルタ株よりlong COVIDが24~50%低いが感染者数が多いため罹患者は今後増加する,long COVID神経症状を認める患者では神経損傷や炎症マーカーの事前の上昇を認める,long COVID患者の血漿から,長ければ1年後までスパイク蛋白が検出される,VITT の既往がある患者がCOVID-19に感染しても再発はない,免疫介在性炎症性疾患患者における2週間のメトトレキサートの中断はワクチン接種後の抗体反応の増強につながる,です.
オミクロン株感染の特徴を過去の変異株と比較する研究が報告され,嗅覚障害やlong COVIDをきたす頻度が低いことが示されました.しかしオミクロン株では感染者が圧倒的に多いので,とくにlong COVID罹患者は今後必然的に増加するものと考えられます.そのlong COVIDの診断バイオマーカーとして,中枢神経傷害のバイオマーカーとして知られるGFAPや炎症性サイトカイン・ケモカイン(IL6,TNFα,MCP1)が見出され,さらに驚くべきことに感染から長ければ1年後までウイルススパイク蛋白が検出され(体内に留まる),これもバイオマーカーになるものと考えられます.関節リウマチ等に対して使用される免疫抑制剤メトトレキサートの2週間の中断は,ワクチン接種の際,検討すべきと思われます.
◆オミクロン株では嗅覚障害の合併は少ない.
嗅覚障害の出現には宿主の遺伝的背景,嗅上皮炎症,局所ACE2発現,嗅覚受容体のダウンレギュレーションの関与が指摘されているが,ウイルス側要因については不明である.ブラジルから軽症COVID-19患者の嗅覚障害について,ウイルス亜種ごとの後方視的な検討が報告された.2020年3月16日~12月22日がオリジナル株,2021年3月1日~6月30日がガンマ株,2021年8月2日~11月10日がデルタ株,2022年1月4日~3月28日がオミクロン株感染を主として認めた.軽症COVID-19患者6053名のうち,2650人が嗅覚障害を呈した.嗅覚障害の有病率は,オリジナル株期では52.6%,ガンマ株期では27.5%,デルタ株期では42.1%,オミクロン株期では5.8%であった.オリジナル株期と比較して,ガンマ株期(調整オッズ比0.48,P < .001)およびオミクロン株期(0.07,P < .001)で低かった.以上より,ウイルス株のタイプは嗅覚障害に影響する.
JAMA. June 24, 2022(doi.org/10.1001/jama.2022.11006)
◆オミクロン株はデルタ株よりlong COVIDが24~50%低いが感染者数が多いため罹患者は今後増加する.
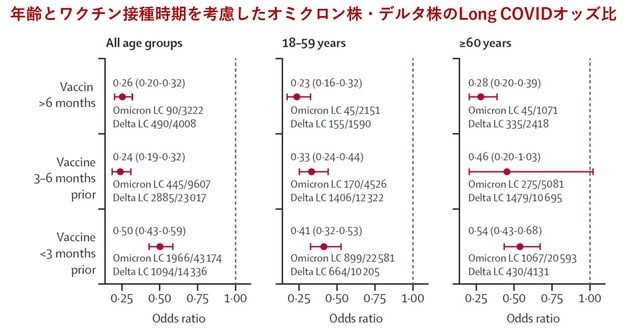
英国においてオミクロン株とデルタ株感染におけるlong COVID(急性期後4週間以上経過してから新たな,または継続する症状があると定義)の相対確率を明らかにすることを目的とした症例対照研究が報告された.Zoe社が開発したスマホアプリの使用者から集めた情報を使用した.2021年6月1日~11月27をデルタ株期,2021年12月20日~2022年3月9日をオミクロン株期とした(期間内にオミクロン株ないしデルタ株が70%以上を占める).結果としてlong COVIDは,デルタ株期で10.8%(4469/41361人),オミクロン株期で4.5%(2501/56003人)で,オミクロン株で少なかった.ワクチンの接種時期を考慮するとオミクロン株ではデルタ株よりオッズ比で24~50%低い結果であった(図1).年齢を考慮してもオミクロン株では少なかった.しかし感染者がオミクロン株で圧倒的に多いことを考慮すると,long COVIDはオミクロン株期以降,必然的に増加する.
Lancet. June 18, 2022(doi.org/10.1016/S0140-6736(22)00941-2)
◆long COVID神経症状を認める患者では神経損傷や炎症マーカーの事前の上昇を認める.
中枢神経症状を呈するLong COVID(PASC)患者におけるバイオマーカー研究が米国から報告された.対象は感染後約4カ月において,自己申告で症状を認めた121名のlong COVID 患者である.うち52名が中枢神経症状あり,69名がなしであった.この中枢神経症状の有無で,血漿の神経学的損傷マーカー(GFAPとNfL)および免疫活性化マーカー(サイトカイン,ケモカイン)を比較した.結果としては,回復初期(感染から90日未満)には中枢神経症状あり群でGFAPの上昇を認めたが(平均比1.3倍,p = 0.02),NfLの上昇はなかった(平均比1.06倍,p = 0.54;図2).また回復後期(感染から90日以上)ではGFAP,NfLとも差はなかった.免疫活性化マーカーについては,中枢神経症状あり群で,IL6(回復初期に48%,回復後期に38%上昇),MCP1(回復初期に19%上昇),TNFα(回復初期に19%,回復後期に13%上昇)の上昇を認めたが,IFNgamma,IL10,IP10に差はなかった.GFAPとNfLは,回復初期にはいくつかの免疫活性化マーカーと相関を示したが,回復後期には弱まった.以上より感染後約4カ月の中枢神経症状は,それ以前の神経損傷や炎症マーカーと関連し,これらはバイオマーカーになる可能性がある.またいくつかの炎症経路がlong COVIDの発症に関与していると考えられ,治療標的になる可能性がある.
Neurol Neuroimmunol Neuroinflamm. June 14, 2022(doi.org/10.1212/NXI.0000000000200003)

◆long COVID患者の血漿から,長ければ1年後までスパイク蛋白が検出される.
COVID-19患者コホート63名(うちPASCが37人)から採取した血漿を分析し,循環ウイルス抗原と炎症マーカーを定量化したHarvardからの未査読論文が報告された.ウイルス抗原として,スパイク蛋白(S),S1蛋白(S1:スパイク蛋白のS1サブユニット),ヌクレオカプシドタンパク質(N)を測定した.PASC患者の多くは女性であった.驚くべきことに,SARS-CoV-2陽性診断から数ヶ月後でも,PASC患者のほぼ65%でS,S1,Nのいずれかが検出された(Sは60%で検出)(図3).PASC患者のうち,12人の患者で複数回抗原が検出され,抗原の持続的循環が示唆された.一方,long COVIDを免れた6人のCOVID-19患者では,COVID-19の診断後すぐに高いレベルの抗原を示したが,まもなく検出不可能なレベルまで減少した.以上より,long COVIDではCOVID-19の診断から12ヵ月後までウイルスのリザーバー(体内貯蔵庫)が持続的に存在すること,ならびにスパイク蛋白はPASCのバイオマーカーであることが示された.
medRxiv. June 16, 2022(doi.org/10.1101/2022.06.14.22276401)

◆VITT の既往がある患者がCOVID-19に感染しても再発はない.
ワクチン誘発性免疫性血小板減少症(VITT)は,ウイルスベクターワクチン(アストラゼネカおよびJ&J)による副反応である.VITTは血小板第4因子(PF4)とワクチンにより誘導されるスパイクタンパク質に対する免疫反応の交差反応によって生じるという懸念がある.つまりVITT生存者がその後,COVID-19を罹患した場合,PF4抗体が増加し,VITTを再発するおそれがある.ドイツからVITTの既往を持つ患者69人を検討した研究が報告された.24人はその後COVID-19ワクチンの接種を受けず,残りの45人はその後mRNAワクチンが接種された(31人は2回接種,14人は3回接種).69人のうち11人(16%)がCOVID-19に感染したが,いずれも症状は軽く,またmRNAワクチンを接種した患者ではウイルスベクターワクチンのみの患者より感染は少なかった(29%対9%,P=0.04).つまりVITTの既往のある患者に対して,mRNAワクチン接種を行うことが支持される.一方,感染2週間後の検討でPF4抗体濃度は感染前のサンプル値よりも低く,血小板減少症や血栓症を認めた患者もいなかった.以上よりスパイク蛋白とPF4に対する免疫反応は別個のものであることが示唆される.これらはVITTの既往を持つ患者におけるカウンセリングに役立つ情報となる.
New Engl J Med. June 27, 2022(doi.org/10.1056/NEJMc2206601)
◆免疫介在性炎症性疾患患者における2週間のメトトレキサートの中断はワクチン接種後の抗体反応の増強につながる.
免疫療法はCOVID-19ワクチン誘発免疫を抑制してしまう.英国26の病院から,免疫介在性炎症疾患患者(関節リウマチ,乾癬±関節炎,脊椎関節炎,アトピー性皮膚炎,リウマチ性多発筋痛症,SLE)において,ブースター接種直後の2週間のメトトレキサート(MTX)治療(週25mg以下)の中断が,中断しなかった場合と比較して抗体誘発を改善するかを検討した.MTX継続群127名とMTX中断群127名を比較した.女性61%,関節リウマチが130名(51%),乾癬±関節炎が86名(34%)であった.4週間後の幾何平均スパイク蛋白のS1受容体結合ドメイン(S1-RBD)抗体価は,MTX中断群で22750 U/mL,継続群で10798 U/mLで,幾何平均比は2.19(p<0.0001)であった(図4).この抗体反応の増加は,MTXの用量,投与経路,原疾患の種類,年齢,SARS-CoV-2感染歴等,いずれを考慮しても一貫して認められた.以上より,免炎症性疾患患者における2週間のMTXの中断はワクチン接種後の抗体反応の増強につながる.この介入は簡単で低コストであるため,ワクチン効果および防御期間の向上につながるものと考えられる → 日本でも関節リウマチ患者等において積極的に検討すべき.
Lancet Respir Med. 2022 Jun 27:S2213-2600(22)00186-2(doi.org/10.1016/S2213-2600(22)00186-2)

オミクロン株感染の特徴を過去の変異株と比較する研究が報告され,嗅覚障害やlong COVIDをきたす頻度が低いことが示されました.しかしオミクロン株では感染者が圧倒的に多いので,とくにlong COVID罹患者は今後必然的に増加するものと考えられます.そのlong COVIDの診断バイオマーカーとして,中枢神経傷害のバイオマーカーとして知られるGFAPや炎症性サイトカイン・ケモカイン(IL6,TNFα,MCP1)が見出され,さらに驚くべきことに感染から長ければ1年後までウイルススパイク蛋白が検出され(体内に留まる),これもバイオマーカーになるものと考えられます.関節リウマチ等に対して使用される免疫抑制剤メトトレキサートの2週間の中断は,ワクチン接種の際,検討すべきと思われます.
◆オミクロン株では嗅覚障害の合併は少ない.
嗅覚障害の出現には宿主の遺伝的背景,嗅上皮炎症,局所ACE2発現,嗅覚受容体のダウンレギュレーションの関与が指摘されているが,ウイルス側要因については不明である.ブラジルから軽症COVID-19患者の嗅覚障害について,ウイルス亜種ごとの後方視的な検討が報告された.2020年3月16日~12月22日がオリジナル株,2021年3月1日~6月30日がガンマ株,2021年8月2日~11月10日がデルタ株,2022年1月4日~3月28日がオミクロン株感染を主として認めた.軽症COVID-19患者6053名のうち,2650人が嗅覚障害を呈した.嗅覚障害の有病率は,オリジナル株期では52.6%,ガンマ株期では27.5%,デルタ株期では42.1%,オミクロン株期では5.8%であった.オリジナル株期と比較して,ガンマ株期(調整オッズ比0.48,P < .001)およびオミクロン株期(0.07,P < .001)で低かった.以上より,ウイルス株のタイプは嗅覚障害に影響する.
JAMA. June 24, 2022(doi.org/10.1001/jama.2022.11006)
◆オミクロン株はデルタ株よりlong COVIDが24~50%低いが感染者数が多いため罹患者は今後増加する.
英国においてオミクロン株とデルタ株感染におけるlong COVID(急性期後4週間以上経過してから新たな,または継続する症状があると定義)の相対確率を明らかにすることを目的とした症例対照研究が報告された.Zoe社が開発したスマホアプリの使用者から集めた情報を使用した.2021年6月1日~11月27をデルタ株期,2021年12月20日~2022年3月9日をオミクロン株期とした(期間内にオミクロン株ないしデルタ株が70%以上を占める).結果としてlong COVIDは,デルタ株期で10.8%(4469/41361人),オミクロン株期で4.5%(2501/56003人)で,オミクロン株で少なかった.ワクチンの接種時期を考慮するとオミクロン株ではデルタ株よりオッズ比で24~50%低い結果であった(図1).年齢を考慮してもオミクロン株では少なかった.しかし感染者がオミクロン株で圧倒的に多いことを考慮すると,long COVIDはオミクロン株期以降,必然的に増加する.
Lancet. June 18, 2022(doi.org/10.1016/S0140-6736(22)00941-2)

◆long COVID神経症状を認める患者では神経損傷や炎症マーカーの事前の上昇を認める.
中枢神経症状を呈するLong COVID(PASC)患者におけるバイオマーカー研究が米国から報告された.対象は感染後約4カ月において,自己申告で症状を認めた121名のlong COVID 患者である.うち52名が中枢神経症状あり,69名がなしであった.この中枢神経症状の有無で,血漿の神経学的損傷マーカー(GFAPとNfL)および免疫活性化マーカー(サイトカイン,ケモカイン)を比較した.結果としては,回復初期(感染から90日未満)には中枢神経症状あり群でGFAPの上昇を認めたが(平均比1.3倍,p = 0.02),NfLの上昇はなかった(平均比1.06倍,p = 0.54;図2).また回復後期(感染から90日以上)ではGFAP,NfLとも差はなかった.免疫活性化マーカーについては,中枢神経症状あり群で,IL6(回復初期に48%,回復後期に38%上昇),MCP1(回復初期に19%上昇),TNFα(回復初期に19%,回復後期に13%上昇)の上昇を認めたが,IFNgamma,IL10,IP10に差はなかった.GFAPとNfLは,回復初期にはいくつかの免疫活性化マーカーと相関を示したが,回復後期には弱まった.以上より感染後約4カ月の中枢神経症状は,それ以前の神経損傷や炎症マーカーと関連し,これらはバイオマーカーになる可能性がある.またいくつかの炎症経路がlong COVIDの発症に関与していると考えられ,治療標的になる可能性がある.
Neurol Neuroimmunol Neuroinflamm. June 14, 2022(doi.org/10.1212/NXI.0000000000200003)

◆long COVID患者の血漿から,長ければ1年後までスパイク蛋白が検出される.
COVID-19患者コホート63名(うちPASCが37人)から採取した血漿を分析し,循環ウイルス抗原と炎症マーカーを定量化したHarvardからの未査読論文が報告された.ウイルス抗原として,スパイク蛋白(S),S1蛋白(S1:スパイク蛋白のS1サブユニット),ヌクレオカプシドタンパク質(N)を測定した.PASC患者の多くは女性であった.驚くべきことに,SARS-CoV-2陽性診断から数ヶ月後でも,PASC患者のほぼ65%でS,S1,Nのいずれかが検出された(Sは60%で検出)(図3).PASC患者のうち,12人の患者で複数回抗原が検出され,抗原の持続的循環が示唆された.一方,long COVIDを免れた6人のCOVID-19患者では,COVID-19の診断後すぐに高いレベルの抗原を示したが,まもなく検出不可能なレベルまで減少した.以上より,long COVIDではCOVID-19の診断から12ヵ月後までウイルスのリザーバー(体内貯蔵庫)が持続的に存在すること,ならびにスパイク蛋白はPASCのバイオマーカーであることが示された.
medRxiv. June 16, 2022(doi.org/10.1101/2022.06.14.22276401)

◆VITT の既往がある患者がCOVID-19に感染しても再発はない.
ワクチン誘発性免疫性血小板減少症(VITT)は,ウイルスベクターワクチン(アストラゼネカおよびJ&J)による副反応である.VITTは血小板第4因子(PF4)とワクチンにより誘導されるスパイクタンパク質に対する免疫反応の交差反応によって生じるという懸念がある.つまりVITT生存者がその後,COVID-19を罹患した場合,PF4抗体が増加し,VITTを再発するおそれがある.ドイツからVITTの既往を持つ患者69人を検討した研究が報告された.24人はその後COVID-19ワクチンの接種を受けず,残りの45人はその後mRNAワクチンが接種された(31人は2回接種,14人は3回接種).69人のうち11人(16%)がCOVID-19に感染したが,いずれも症状は軽く,またmRNAワクチンを接種した患者ではウイルスベクターワクチンのみの患者より感染は少なかった(29%対9%,P=0.04).つまりVITTの既往のある患者に対して,mRNAワクチン接種を行うことが支持される.一方,感染2週間後の検討でPF4抗体濃度は感染前のサンプル値よりも低く,血小板減少症や血栓症を認めた患者もいなかった.以上よりスパイク蛋白とPF4に対する免疫反応は別個のものであることが示唆される.これらはVITTの既往を持つ患者におけるカウンセリングに役立つ情報となる.
New Engl J Med. June 27, 2022(doi.org/10.1056/NEJMc2206601)
◆免疫介在性炎症性疾患患者における2週間のメトトレキサートの中断はワクチン接種後の抗体反応の増強につながる.
免疫療法はCOVID-19ワクチン誘発免疫を抑制してしまう.英国26の病院から,免疫介在性炎症疾患患者(関節リウマチ,乾癬±関節炎,脊椎関節炎,アトピー性皮膚炎,リウマチ性多発筋痛症,SLE)において,ブースター接種直後の2週間のメトトレキサート(MTX)治療(週25mg以下)の中断が,中断しなかった場合と比較して抗体誘発を改善するかを検討した.MTX継続群127名とMTX中断群127名を比較した.女性61%,関節リウマチが130名(51%),乾癬±関節炎が86名(34%)であった.4週間後の幾何平均スパイク蛋白のS1受容体結合ドメイン(S1-RBD)抗体価は,MTX中断群で22750 U/mL,継続群で10798 U/mLで,幾何平均比は2.19(p<0.0001)であった(図4).この抗体反応の増加は,MTXの用量,投与経路,原疾患の種類,年齢,SARS-CoV-2感染歴等,いずれを考慮しても一貫して認められた.以上より,免炎症性疾患患者における2週間のMTXの中断はワクチン接種後の抗体反応の増強につながる.この介入は簡単で低コストであるため,ワクチン効果および防御期間の向上につながるものと考えられる → 日本でも関節リウマチ患者等において積極的に検討すべき.
Lancet Respir Med. 2022 Jun 27:S2213-2600(22)00186-2(doi.org/10.1016/S2213-2600(22)00186-2)