成人発症の孤発性脊髄小脳変性症の代表はMSA-Cであるが,もう一つは近年,SAOA(Sporadic adult-onset ataxia of unknown etiology)と呼ばれるようになった分類で,この概念の背景については,過去に当ブログにおいてご紹介した.
孤発性脊髄小脳変性症の分類はどうあるべきか ーSAOAという考え方ー
自律神経障害を認めない点でMSA-Cと鑑別されるが,一部のSAOA症例は,その経過中にMSA-Cに表現型が変化しうる(phenoconversion).しかしSAOAの臨床像や重症度,遺伝子変異の関与についてはほとんど不明であった.これを解明するために,ヨーロッパにて成人発症の孤発性脊髄小脳変性症の患者レジストリーであるSPORTAXが結成され,その結果が報告されたのでご紹介したい.
対象は進行性失調症,40歳以降の発症,家族内類症や血族結婚なし,後天的な失調の原因なし,という4項目を満たす症例とした.重症度はSARAで検討し,遺伝子診断は脊髄小脳変性症特異的遺伝子スクリーニングパネルと次世代シークエンサーを用いた.上述の通り,SAOAの一部はMSA-Cにphenoconversionすることから10年間以上,表現型に変化がなかった症例をSAOAと定義した.
さて結果であるが,249名が対象となった.83名がMSA-C probableのGilman分類の診断基準を登録時に満たし,さらに経過観察中に12名が診断基準を満たした(計95名).小脳失調の重症度(SARA高値)を決定する因子は,多変量解析にて,MSA-Cの診断基準を満たすこと,および罹病期間が長いことであった.一方,SAOAと診断されたのは48名であった.MSA-Cと比較してこれらの症例は,小脳失調の重症度が低く(SARA:13.6±6.0 vs 16.0±5.8,P=0.0200),年間の進行速度も遅かった(SARA:1.1±2.3 vs 3.3±3.2,P=0.0013).臨床像に関しては,MSA-CはSAOAと比較して,筋強剛,排尿障害,腱反射亢進が有意に多かった.
遺伝子診断を行った194名中11名(6%)に病因と考えられる遺伝子変異を認めた.具体的には確定的な遺伝子変異は劣性がATM 1名,SPG7 2名,優性がCACNA1A 2名,TRPC3/SCA41 1名,ほぼ確実な遺伝子変異は劣性がADCK3 1名,POLG 1名,SNX14 1名,優性がCACNA1A 1名,OPA1 1名であった.またATM,POLG,CACNA1A遺伝子変異を持つ症例はMSA-C probableの診断基準を満たした.
以上の結果より,SAOAに関して以下の点がわかった.
1)SAOAはMSA-Cと比較して,小脳性運動失調は軽度で,かつその進行も遅い.
2)劣性遺伝および優性遺伝を呈する複数の脊髄小脳変性症の遺伝子が,SAOAの原因になりうる.
3)MSA-Cの原因遺伝子として報告されているCOQ2の変異は認めなかったが,これと異なる3つの遺伝子変異が認められた.しかし,MSAの診断を病理的に確認していないため,これらの遺伝子がMSAを引き起こすとは言えない.むしろphenocopy(表現型模写:通常と異なる表現型が出現)の可能性がある.
さらに本論文は以下の意味でも重要であろう.
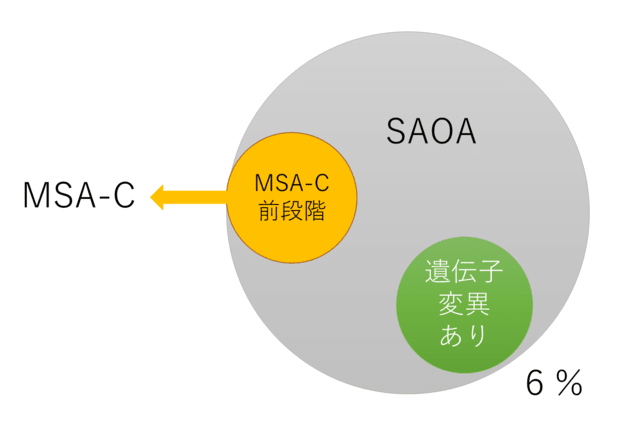
1)SAOAの一部がMSAである,もしくは遺伝子変異を持つことがわかったが,残りの症例の病態がまだ不明である(図).変性疾患だけではなく,おそらく治療可能な免疫性,炎症性,代謝性失調等さまざまな疾患が含まれているものと予想される.
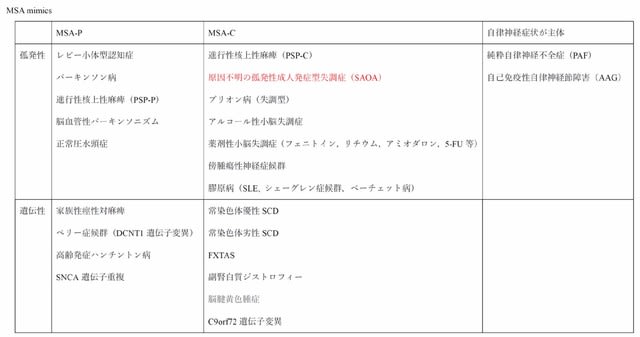
2)MSA-Cの病態修飾療法を行う際に,MSA mimicsを除外する必要があるが,SAOAはPSP-Cなどとともに鑑別に挙がる.最後に個人的に使用しているMSAの鑑別診断のリストを提示する(表).厳密にmimicsを否定することはなかなか難しいことが分かるだろう.
Giordano I, et al. Clinical and genetic characteristics of sporadic adult-onset degenerative ataxia. Neurology. 2017 Aug 9. pii: 10.1212/WNL.0000000000004311.
孤発性脊髄小脳変性症の分類はどうあるべきか ーSAOAという考え方ー
自律神経障害を認めない点でMSA-Cと鑑別されるが,一部のSAOA症例は,その経過中にMSA-Cに表現型が変化しうる(phenoconversion).しかしSAOAの臨床像や重症度,遺伝子変異の関与についてはほとんど不明であった.これを解明するために,ヨーロッパにて成人発症の孤発性脊髄小脳変性症の患者レジストリーであるSPORTAXが結成され,その結果が報告されたのでご紹介したい.
対象は進行性失調症,40歳以降の発症,家族内類症や血族結婚なし,後天的な失調の原因なし,という4項目を満たす症例とした.重症度はSARAで検討し,遺伝子診断は脊髄小脳変性症特異的遺伝子スクリーニングパネルと次世代シークエンサーを用いた.上述の通り,SAOAの一部はMSA-Cにphenoconversionすることから10年間以上,表現型に変化がなかった症例をSAOAと定義した.
さて結果であるが,249名が対象となった.83名がMSA-C probableのGilman分類の診断基準を登録時に満たし,さらに経過観察中に12名が診断基準を満たした(計95名).小脳失調の重症度(SARA高値)を決定する因子は,多変量解析にて,MSA-Cの診断基準を満たすこと,および罹病期間が長いことであった.一方,SAOAと診断されたのは48名であった.MSA-Cと比較してこれらの症例は,小脳失調の重症度が低く(SARA:13.6±6.0 vs 16.0±5.8,P=0.0200),年間の進行速度も遅かった(SARA:1.1±2.3 vs 3.3±3.2,P=0.0013).臨床像に関しては,MSA-CはSAOAと比較して,筋強剛,排尿障害,腱反射亢進が有意に多かった.
遺伝子診断を行った194名中11名(6%)に病因と考えられる遺伝子変異を認めた.具体的には確定的な遺伝子変異は劣性がATM 1名,SPG7 2名,優性がCACNA1A 2名,TRPC3/SCA41 1名,ほぼ確実な遺伝子変異は劣性がADCK3 1名,POLG 1名,SNX14 1名,優性がCACNA1A 1名,OPA1 1名であった.またATM,POLG,CACNA1A遺伝子変異を持つ症例はMSA-C probableの診断基準を満たした.
以上の結果より,SAOAに関して以下の点がわかった.
1)SAOAはMSA-Cと比較して,小脳性運動失調は軽度で,かつその進行も遅い.
2)劣性遺伝および優性遺伝を呈する複数の脊髄小脳変性症の遺伝子が,SAOAの原因になりうる.
3)MSA-Cの原因遺伝子として報告されているCOQ2の変異は認めなかったが,これと異なる3つの遺伝子変異が認められた.しかし,MSAの診断を病理的に確認していないため,これらの遺伝子がMSAを引き起こすとは言えない.むしろphenocopy(表現型模写:通常と異なる表現型が出現)の可能性がある.
さらに本論文は以下の意味でも重要であろう.
1)SAOAの一部がMSAである,もしくは遺伝子変異を持つことがわかったが,残りの症例の病態がまだ不明である(図).変性疾患だけではなく,おそらく治療可能な免疫性,炎症性,代謝性失調等さまざまな疾患が含まれているものと予想される.
2)MSA-Cの病態修飾療法を行う際に,MSA mimicsを除外する必要があるが,SAOAはPSP-Cなどとともに鑑別に挙がる.最後に個人的に使用しているMSAの鑑別診断のリストを提示する(表).厳密にmimicsを否定することはなかなか難しいことが分かるだろう.
Giordano I, et al. Clinical and genetic characteristics of sporadic adult-onset degenerative ataxia. Neurology. 2017 Aug 9. pii: 10.1212/WNL.0000000000004311.

















