小脳性運動失調症に加え,ニューロパチー,両側性前庭障害を呈するCANVAS(Cerebellar ataxia with neuropathy and vestibular areflexia syndrome)を代表とするRFC1遺伝子関連スペクトラム障害(Brain Nerve 2022年11月号に特集号)は本邦でも少なからず存在し注目されています.今回,ヨーロッパからの報告で,その鑑別診断として,線維芽細胞増殖因子14(FGF14)遺伝子のGAAリピート伸長によるSCA27B(MIM: 620174)が重要であることが報告されました.ちなみにSCA27BはSCA50として報告されましたが,同じFGF14遺伝子のミスセンス変異などの遺伝子変異がSCA27と報告されていたことから,SCA27BとMIMに登録されました.
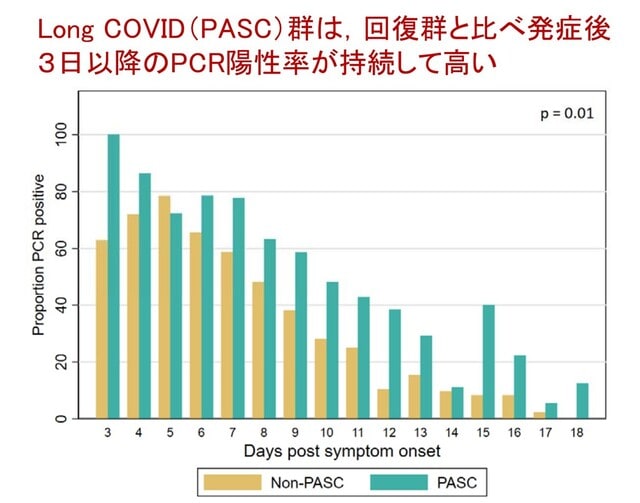
論文では,小脳性運動失調症に加えてニューロパチーおよび/または両側前庭障害を認めるRFC1遺伝子GAAリピート伸長(-)患者をヨーロッパの7施設から45人集積し,GAAリピートを調べました.この結果,GAAリピート伸長の頻度は,コホート全体で38%(17/45),小脳性運動失調+ニューロパチーのサブグループで38%(5/13),小脳失調症+両側前庭障害のサブグループで43%(9/21),3つの特徴をすべて有するサブグループで27%(3/11)でした(図左).両側前庭障害(ベッドサイド頭部インパルス検査またはビデオ頭部インパルス検査(vHIT)による両側前庭眼反射の低下として確認:vHITは47%(21/45例で実施))はGAAリピート伸長患者の75%(12/16)で認められました.またニューロパチーはGAAリピート伸長患者の75%(6/8)で軽度の感覚・運動混合型ニューロパチーを認めました(sensorimotor axonal neuropathy).運動失調の家族歴は,GAAリピート伸長患者で有意に頻度が高く(59% vs 15%;p=0.007),永続的な小脳性構音障害はGAAリピート伸長患者で有意に頻度が低いという特徴がありました(12% vs 54%;p=0.009).発症時年齢はリピート数と逆相関していました(R2=0.45; p=0.0031).
以上より,SCA27Bは,ニューロパチーおよび/または両側前庭障害を伴う小脳性運動失調症の稀ではない原因であり,CANVASおよびRFC1遺伝子関連スペクトラム障害の鑑別診断と考えられました.両者の鑑別点して,以下が挙げられます(図右).
1)SCA27BではRFC1遺伝子関連スペクトラム障害でしばしば認められる慢性咳嗽はまれ.
2)RFC1遺伝子関連スペクトラム障害では,運動神経障害は通常ないか,あってもまれであるが,SCA27Bでは75%(6/8人)に感覚・運動軸索ニューロパチーがみられた.
3)エピソード症状がSCA27Bでは10/17例と高頻度に認められたが,RFC1遺伝子関連スペクトラム障害ではまれ.
4)SCA27Bは常染色体顕性遺伝であり,RFC1遺伝子関連スペクトラム障害では常染色体潜性遺伝であるため,家族歴がその鑑別に役立つ.しかしSCA27Bでは孤発例がコホートによっては15〜50%と多く,一見,潜性遺伝にみえることがある.
Pellerin D, et al. Intronic FGF14 GAA repeat expansions are a common cause of ataxia syndromes with neuropathy and bilateral vestibulopathy. J Neurol Neurosurg Psychiatry. 2023 Jun 30:jnnp-2023-331490.

論文では,小脳性運動失調症に加えてニューロパチーおよび/または両側前庭障害を認めるRFC1遺伝子GAAリピート伸長(-)患者をヨーロッパの7施設から45人集積し,GAAリピートを調べました.この結果,GAAリピート伸長の頻度は,コホート全体で38%(17/45),小脳性運動失調+ニューロパチーのサブグループで38%(5/13),小脳失調症+両側前庭障害のサブグループで43%(9/21),3つの特徴をすべて有するサブグループで27%(3/11)でした(図左).両側前庭障害(ベッドサイド頭部インパルス検査またはビデオ頭部インパルス検査(vHIT)による両側前庭眼反射の低下として確認:vHITは47%(21/45例で実施))はGAAリピート伸長患者の75%(12/16)で認められました.またニューロパチーはGAAリピート伸長患者の75%(6/8)で軽度の感覚・運動混合型ニューロパチーを認めました(sensorimotor axonal neuropathy).運動失調の家族歴は,GAAリピート伸長患者で有意に頻度が高く(59% vs 15%;p=0.007),永続的な小脳性構音障害はGAAリピート伸長患者で有意に頻度が低いという特徴がありました(12% vs 54%;p=0.009).発症時年齢はリピート数と逆相関していました(R2=0.45; p=0.0031).
以上より,SCA27Bは,ニューロパチーおよび/または両側前庭障害を伴う小脳性運動失調症の稀ではない原因であり,CANVASおよびRFC1遺伝子関連スペクトラム障害の鑑別診断と考えられました.両者の鑑別点して,以下が挙げられます(図右).
1)SCA27BではRFC1遺伝子関連スペクトラム障害でしばしば認められる慢性咳嗽はまれ.
2)RFC1遺伝子関連スペクトラム障害では,運動神経障害は通常ないか,あってもまれであるが,SCA27Bでは75%(6/8人)に感覚・運動軸索ニューロパチーがみられた.
3)エピソード症状がSCA27Bでは10/17例と高頻度に認められたが,RFC1遺伝子関連スペクトラム障害ではまれ.
4)SCA27Bは常染色体顕性遺伝であり,RFC1遺伝子関連スペクトラム障害では常染色体潜性遺伝であるため,家族歴がその鑑別に役立つ.しかしSCA27Bでは孤発例がコホートによっては15〜50%と多く,一見,潜性遺伝にみえることがある.
Pellerin D, et al. Intronic FGF14 GAA repeat expansions are a common cause of ataxia syndromes with neuropathy and bilateral vestibulopathy. J Neurol Neurosurg Psychiatry. 2023 Jun 30:jnnp-2023-331490.