方法としては,胸腺摘出術を受けた成人患者の死亡,がん,自己免疫疾患のリスクを,類似の心臓胸部手術を受けた,胸腺摘出術の経験のない対照と比較しています.患者のサブグループで,T 細胞産生量(新たに発生した胸腺T細胞におけるTCR再配列の副産物として形成されるシグナル接合T細胞受容体(TCR)切除円の頻度で評価)と血漿中サイトカイン濃度も比較しています.
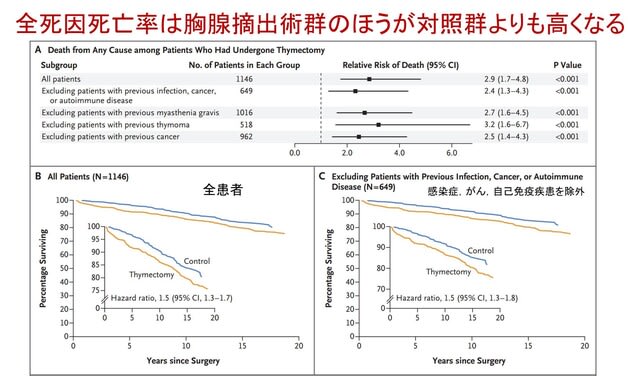
さて結果ですが,胸腺摘出術を受けた1420 例と対照6021 例が研究に組み入れられ,このうち胸腺摘出術を受けた1146 例が対照とマッチし検討が行われました.術後 5 年の時点で,全死因死亡率は胸腺摘出術群のほうが対照群よりも高く(8.1% 対 2.8%,相対リスク 2.9)(図),がんも同様の結果でした(7.4% 対 3.7%,相対リスク 2.0).自己免疫疾患については2群間で有意差はありませんでしたが(相対リスク 1.1),術前に感染症,がん,自己免疫疾患を認めた患者を解析から除外すると,有意差が認められました(12.3% 対 7.9%,相対リスク 1.5).マッチした対照の有無を問わず追跡期間が 5 年を超える全例を対象に解析を行うと,全死因死亡率は胸腺摘出術群のほうが米国の一般集団よりも高く(9.0% 対 5.2%),がん死亡率も同様でした(2.3% 対 1.5%).
T 細胞産生量と血漿中サイトカイン濃度を測定した胸腺摘出術群 22 例と対照群 19 例(術後の追跡期間は平均 14.2 年)の検討では,胸腺摘出術群はCD4 陽性リンパ球と CD8 陽性リンパ球の新生量が少なく,逆に血中炎症性サイトカイン濃度が高いことが分かりました.具体的には,胸腺摘出術群で15種類のサイトカイン値が有意に変化し,炎症性サイトカインのIL-23,IL-33,トロンボポエチン,thymic stromal lymphopoietinのレベルは対照群の10倍以上でした.つまり胸腺摘出術群患者の免疫環境は,免疫調節異常と炎症を引き起こすことが知られるサイトカイン環境にシフトしていました.Editorialでは「胸腺は,成熟T細胞のこの臓器への生理的再循環を通して,T細胞機能を調節しているのではないかと推測したくなる」と述べられています.
重症筋無力症(MG)では,胸線摘出術の有効性を検討したMGTX研究の結果に基づき,現在は「胸線摘除の有効性が期待でき,その施行が検討される非胸腺腫MGは,50歳未満の発症で,発症早期のAChR抗体陽性過形成胸線例である(重症筋無力症診療ガイドライン 2022)」とされ,以前と比べその適応患者は限定されていますが,上記患者であっても,今回の新しいエビデンスを提示し,shared decision makingにより治療方針を決定する必要があります.また今後のMG患者においても今回の論文と同様の検討が必要であると思われます.
N Engl J Med 2023; 389 : 406-17.

















