医療者であれば脳神経疾患罹患後に筋力が低下することに異議を唱える人は少ないように思います.これは長期臥床による廃用萎縮(筋肉を動かさないことによる萎縮)と説明されてきました.ワシントン大学からScience Immunol誌に報告された論文を読むと,意外なことに単なる廃用ではなく,「脳内で起きた炎症シグナルが筋肉に伝わってミトコンドリア障害をきたす」という驚くべきことが生じていることが分かります.
結論が図にまとまっているのでこれを用いて解説したいと思います.論文によると感染症(細菌感染,COVID-19)や神経変性疾患(アルツハイマー病)のあとに筋障害が生じる経路は2つあり,①神経変性を介する筋障害経路,②炎症シグナルを介する筋障害経路になります.
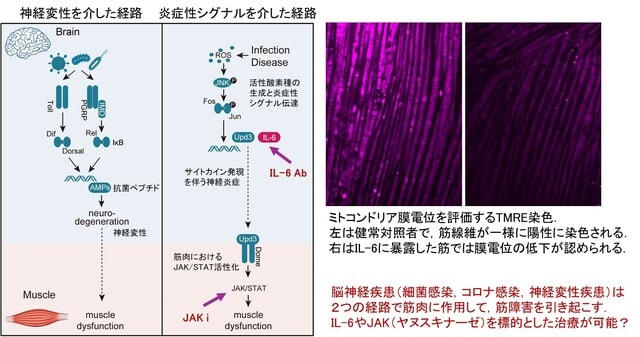
①神経変性を介した筋障害経路(図1左)
病原体の脳内侵入→Toll受容体とPGRP(ペプチドグリカン)受容体の活性化→転写因子Dorsal およびRel の核移行→抗菌ペプチド(AMPs)の生成→神経細胞の炎症とこれに伴う神経変性→神経系の機能低下→結果的に筋機能障害の発生
②炎症性シグナルを介した筋機能障害(図1右)
感染または慢性神経疾患→活性酸素種(ROS)の脳内での生成・蓄積→炎症性シグナル伝達(JNK経路の活性化.FosとJunを介してUpd3*(哺乳類ではIL-6)の発現を誘導→Upd3/IL-6の血液循環への放出と筋への到達→IL6受容体の活性化とJAK/STAT経路の活性化→リン酸化STATの核移行→ミトコンドリア機能障害(ATP産生↓)→筋障害
* Upd3(Unpaired 3):ショウジョウバエにおけるマウスIL6のオルソログ
図2はミトコンドリア膜電位を評価するためのTMRE染色(tetramethyl rhodamine ethyl ester)染色
つまりbrain-muscle axisというシグナル経路が存在すること(脳-筋連関)をショウジョウバエ・モデルとマウス・モデルで確認し,さらにヒトにおいてもCOVD-19後遺症である筋痛性脳脊髄炎/慢性疲労症候群(ME/CFS)やアルツハイマー病(Aβ42)をモデルに確認を行っています(COVID-19後のサイトカインストームにおいてIL-6は,IL1βやTNFαなどとともに重要なサイトカインです).もしこれが正しければIL6に対するモノクローナル抗体や,JAL阻害剤が脳神経疾患後の筋障害に有効ということになります.もちろん高額な薬剤を多くの脳神経疾患に予防的に使用することはハードルが高いですが,まずトシリズマブ(IL6抗体薬)などの治療を受けた患者さんの筋障害がどうであったのかなど臨床におけるデータの検証が必要になるものと思います.
Yang S, et al. Infection and chronic disease activate a systemic brain-muscle signaling axis. Sci Immunol. 2024 Jul 12;9(97):eadm7908.(doi.org/10.1126/sciimmunol.adm7908)
結論が図にまとまっているのでこれを用いて解説したいと思います.論文によると感染症(細菌感染,COVID-19)や神経変性疾患(アルツハイマー病)のあとに筋障害が生じる経路は2つあり,①神経変性を介する筋障害経路,②炎症シグナルを介する筋障害経路になります.

①神経変性を介した筋障害経路(図1左)
病原体の脳内侵入→Toll受容体とPGRP(ペプチドグリカン)受容体の活性化→転写因子Dorsal およびRel の核移行→抗菌ペプチド(AMPs)の生成→神経細胞の炎症とこれに伴う神経変性→神経系の機能低下→結果的に筋機能障害の発生
②炎症性シグナルを介した筋機能障害(図1右)
感染または慢性神経疾患→活性酸素種(ROS)の脳内での生成・蓄積→炎症性シグナル伝達(JNK経路の活性化.FosとJunを介してUpd3*(哺乳類ではIL-6)の発現を誘導→Upd3/IL-6の血液循環への放出と筋への到達→IL6受容体の活性化とJAK/STAT経路の活性化→リン酸化STATの核移行→ミトコンドリア機能障害(ATP産生↓)→筋障害
* Upd3(Unpaired 3):ショウジョウバエにおけるマウスIL6のオルソログ
図2はミトコンドリア膜電位を評価するためのTMRE染色(tetramethyl rhodamine ethyl ester)染色
つまりbrain-muscle axisというシグナル経路が存在すること(脳-筋連関)をショウジョウバエ・モデルとマウス・モデルで確認し,さらにヒトにおいてもCOVD-19後遺症である筋痛性脳脊髄炎/慢性疲労症候群(ME/CFS)やアルツハイマー病(Aβ42)をモデルに確認を行っています(COVID-19後のサイトカインストームにおいてIL-6は,IL1βやTNFαなどとともに重要なサイトカインです).もしこれが正しければIL6に対するモノクローナル抗体や,JAL阻害剤が脳神経疾患後の筋障害に有効ということになります.もちろん高額な薬剤を多くの脳神経疾患に予防的に使用することはハードルが高いですが,まずトシリズマブ(IL6抗体薬)などの治療を受けた患者さんの筋障害がどうであったのかなど臨床におけるデータの検証が必要になるものと思います.
Yang S, et al. Infection and chronic disease activate a systemic brain-muscle signaling axis. Sci Immunol. 2024 Jul 12;9(97):eadm7908.(doi.org/10.1126/sciimmunol.adm7908)












 (プリオン病に関するモノグラフとしては現在最良)
(プリオン病に関するモノグラフとしては現在最良)