感染症がアルツハイマー病などの認知症の発症と関連することが注目されていますが,そのメカニズムは不明です.最新号のNature Aging誌に以下を示した研究が報告されています.
◆感染症ごとに特定の部位に脳体積の減少が生じること
◆その脳体積の減少は認知症リスクと関連すること
◆感染症ごとの免疫プロテオームの変化,遺伝的素因が認知症に関連すること
対象は主に英国UK Biobank(49万5896人)とフィンランドの複数のコホート(FPS,HeSSup,STW)(27万3132人)のデータが使用されました.脳画像データはボルチモア長寿研究(BLSA)から得られたもので,特定の感染症が脳体積に与える影響を平均5.3年追跡し,平均3.4回のMRIを施行しました.対象となる感染症は6種類で,インフルエンザ,ヘルペスウイルス,その他のウイルス感染症,上気道感染症(URTI),下気道感染症(LRTI),皮膚・皮下感染症です.COVID-19は含まれていません.
【脳の体積と認知機能への影響】
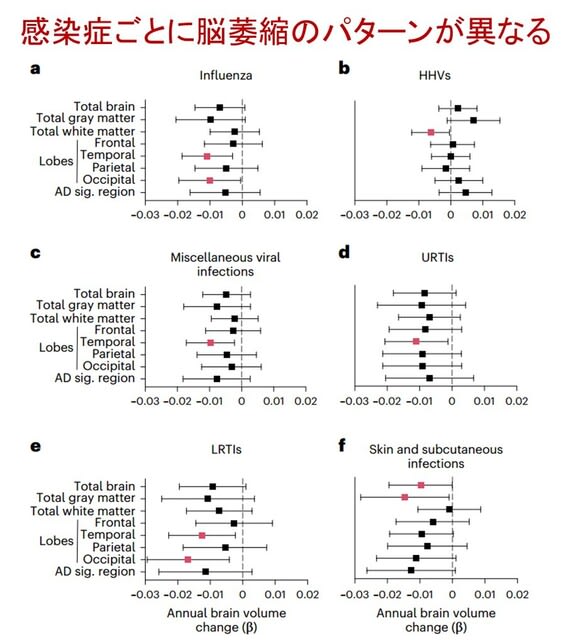
特に側頭葉の灰白質および白質領域において,脳体積の減少を加速させることが確認されました(図1).
①インフルエンザ:側頭葉および後頭葉の灰白質の体積減少
②ヘルペスウイルス(HHV):側頭葉の白質の体積の減少
③種々のウイルス感染症:側頭葉の灰白質の体積の減少
④上気道感染症(URTI):側頭葉全体の体積減少
⑤下気道感染症(LRTI):側頭葉の白質と後頭葉の灰白質および白質の体積減少
⑥皮膚・皮下感染症:側頭葉および後頭葉の灰白質の体積減少
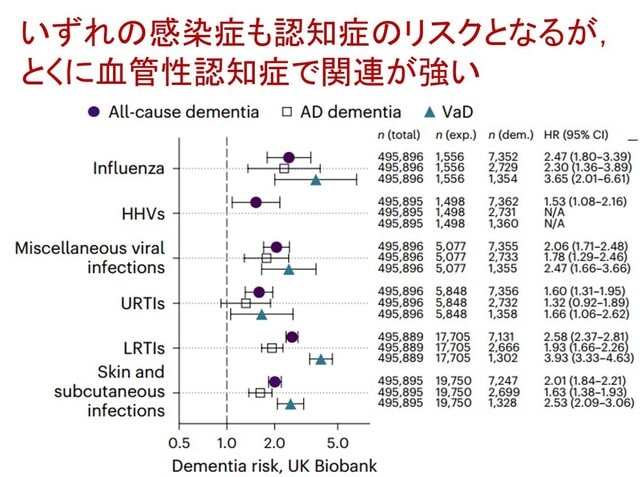
またいずれの感染症も,認知症リスクを増加させました(図2).とくに血管性認知症との関連が強く,ついで認知症(全原因),アルツハイマー病のリスクが増加しました.これらの感染症が脳の血管系に対して影響を及ぼし,血管性病変(BBB破綻)を通じて認知症リスクを高める可能性を示唆しています.さらに全身性の感染症では認知症リスクが高いことが示唆されました.
【プロテオミクス分析による関連するタンパク質と遺伝学的素因】
プロテオミクス分析ではそれぞれの感染症に特徴的なプロテオームの変化が認められました.
①インフルエンザ:
MME(ネプリライシン),DEFB4A,RAG1など
MMEはアミロイドβの分解酵素で,その発現低下はアミロイドβの蓄積を引き起こす.DEFB4AやRAG1は免疫応答に関連し,その活性化は神経炎症を促進する.
②ヘルペスウイルス(HHVs): TREM2,GFAP,NfLなど
TREM2はミクログリアにおける重要な受容体である.
TREM2増加は過剰なミクログリア活性化を引き起こし,神経炎症を促進する.GFAPやNfLは神経損傷の指標である.
③下気道感染症(LRTIs):MASP1,ITGB6,PACSIN2など
MASP1は補体系の活性化に関与し,炎症反応を強化する.ITGB6は細胞接着に関連するタンパク質で,炎症応答の制御に関与する.PACSIN2は神経細胞におけるシグナル伝達に関与する.
④上気道感染症(URTIs):IFIT3,FOXP3など
IFIT3はウイルス感染に応答する抗ウイルスタンパク質で,強力な免疫応答が引き起こされる.FOXP3は免疫抑制に関与するタンパク質.
⑤複数の感染症に共通するタンパク質:260種類のタンパク質が少なくとも1つの感染症と関連し,うちの35種類が脳体積の変化と関連した.PIK3CG,PACSIN2,PRKCBなどが含まれており,これらは認知機能低 下やアルツハイマー病の血漿バイオマーカー(Aβ42/40比,GFAP,NfL,pTau-181)とも関連した.
またITGB6とTLR5の遺伝子変異は,それぞれ側頭灰白質および全脳体積の減少と関連していました.
【病態機序モデル】
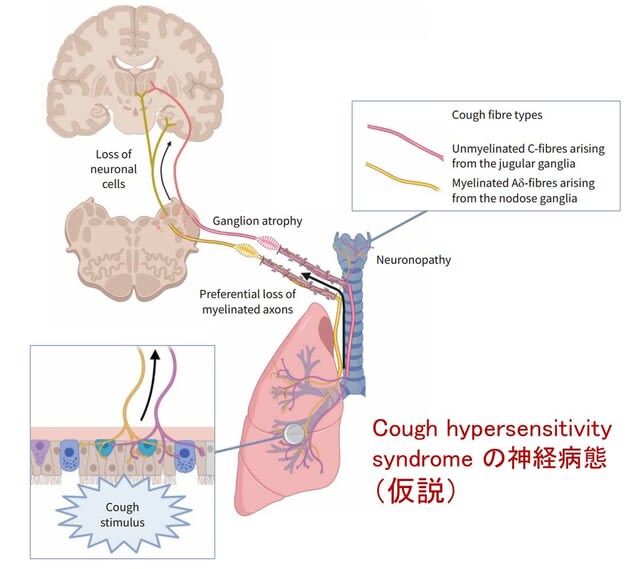
感染後に血漿中で発現が増加した病原性タンパク質(pathogenic proteins)と,減少した保護性タンパク質(protective proteins)が特定されました(図3).
これらのタンパク質の変化が,免疫プロテオームの変化,血液脳関門の破壊,遺伝的要因,アルツハイマー病関連タンパクへの影響を介して,脳の萎縮や認知機能の低下に寄与する可能性が示されました.

この研究はおそらくUKバイオバンク研究で,COVID-19が脳萎縮をもたらし認知症を招くことがきっかけとなり,その他の感染症ではどうなるかを検討したものと思います.そして世界中の最善と考えられるデータ・サンプルを駆使して明確な結論を導いた点に研究の凄みを感じました.
Duggan MR, et al. Proteomics identifies potential immunological drivers of postinfection brain atrophy and cognitive decline. Nat Aging. 2024 Aug 14.(
doi.org/10.1038/s43587-024-00682-4)