2025年5月のメディカルミステリーです。
Breathlessness, nausea, a cough and a mass suggested cancer. But was it?
息切れ、吐き気、咳、腫瘍は悪性腫瘍を示唆していた。しかし本当にそうだったのか?
A young woman endured alarming symptoms, a biopsy that nearly killed her and radical surgery before getting answers.
若い女性は憂慮すべき症状、危うく命を落としかけた生検、そして根治手術に耐えたあと答えを得た。

(Bianca Bagnarelli/For The Washington Post)
2023年8月、Chelsea Cresencia(チェルシー・クレセンシア)さんはボーイフレンドの Allen Nguyen(アレン・グエン)さんとともに California(カリフォルニア)から New York City(ニューヨーク)へ飛んだ。計画された“楽しい旅行”は彼女にとって初めての東海岸への訪問であり、ニューヨークの Chelsea district(チェルシー地区)やそこの有名な市場を散策するなど、おいしい食べ物や観光客向けのものが満載の旅だったが、そこに決めたのは「私の名前が入っているからです」と彼女は言う。
しかし到着してまもなく Cresencia さんは食事後ほぼ毎回嘔吐がみられるようになり、2018年から彼女を悩ませていた息切れが増悪、休まなければ10分以上歩くのがむずかしくなった。またひっきりなしに咳がみられるようになった。
「私たちは食中毒だと思って無視していましたが、連日、1度か2度は嘔吐していました」現在27歳の Cresencia さんは言う。彼女は user experience manager(顧客体験マネージャー)として健康保険会社にリモートで働いている。
「彼女はまた少量の血液も喀出していました」そう思い起こすのは ソフトウェアエンジニアをしている 現在28歳の Nguyen さんである。「私はビビりました」と彼は言う。

Chelsea Cresencia さんと彼女のボーイフレンドの Allen Nguyen さん、2024年5月撮影(Chelsea Cresencia さん提供)
それでも彼らは旅行を続けたが活動性や食事を制限しながら週末には自宅に帰った。San Diego(サンディエゴ)に戻ると、「症状は多少治まったようで数日間は嘔吐することなく過ごせるようになり呼吸も改善しました。ニューヨークに何かあったに違いないと自分に言い聞かせていました」と Cresencia さんは言う。しかし、数週間後、Nguyen さんを訪ねて San Francisco Bay Area(サンフランシスコ・ベイエリア)に滞在中、彼女に突然気がかりな新たな症状が出現した:両足の著明な腫脹である。「痛くはありませんでした。ただ液体が貯まっていたのです」と彼女は思い起こす。
Nguyen さんが彼女を緊急診療施設に連れて行くと医師らは一連の検査を行った。そのうち CT 検査で彼女の心臓に腫瘍が認められたが、これは若い人にとっては衝撃的な発見だった。彼女は恐怖に襲われた。「気持ちが落ち込み、耳が熱くなりました」そう彼女は思い起こす。「どうしてできたの?癌なの?何か悪いことをした?」
この発見を皮切りに、その腫瘍の正体を突き止めるための数ヶ月に及ぶ苦難に満ちた試練が始まった。その間には、危うく命を落としかけた生検や、彼女の命を救うことになり彼女をこれほどまでに病ませた原因を明らかにすることができた根治手術が行われた。
「もっと早く健康診断を受けていればよかったと思う一方で、過去にそれほどとらわれず今を楽しむことに焦点を合わせている自分に気づきました」と彼女は言う。
From urgent care to the hospital 緊急診療から病院まで
Cresencia さんは数年前から息切れに悩まされていた。主に坂道を歩いて上るときに息切れがしたが、わざわざ医者にかかるには“微妙”だと思い無視していた。しかし今回のニューヨークへ旅行がそれを変えた。「いつもよりひどかったのです」と彼女は言う。吐き気と血の混じった咳の発作は初めてだったからだ。
緊急診療所では、医師たちはCTスキャンで見られた腫瘍について明らかに心配しCresencia さんに病院に行くよう促した。二人は San Francisco Bay Area(サンフランシスコのベイエリア)にある Nguyen さんの自宅近くの小さな地域病院に行った。待つこと6時間、ようやく医師が診察し、すぐに彼女を入院させた。
翌日、もっと詳しく見たいと、その病院の医師は transesophageal echocardiogram(経食道心エコー検査)を行った。これは超音波を使って心臓とその周囲の構造を詳細に画像化する検査である。その結果、左心房(心臓の上方にある2つの部屋のうちの1つ)に大きな腫瘍があることがわかり、医師たちはそれが彼女の症状の根本的な原因であることはほぼ間違いないと告げた。もっと大きな病院で特別な治療を受けるよう勧められ、1週間後、San Diego で2番目の病院の医師によって追加検査が行われ、腫瘍を確認、さらに「肺に穴が開いている」ようだと告げられたと彼女は言う。
医師は彼女に、おそらく心肺移植が必要になるだろうと告げ、La Jolla(ラ・ホヤ)にあるUC San Diego Health(UCサンディエゴ・ヘルス)の Jacobs Medical Center(ジェイコブスメディカルセンター)に彼女を送った。そこはそのような手術を行えるこの地域における唯一の病院である。
そこで、心臓専門医は Cresencia さんに、肺に穴は開いていないが、心臓の angiosarcoma(血管肉腫)であると考えていると告げた。これは血管の内膜から発生し予後不良な稀な悪性の癌である。「もしまさにその通りであれば、見た目も悪いだろうと言われました。私は恐怖に襲われました。死ぬことも恐ろしかったし、Allen や家族を失うのが怖くて、何度も泣きました」と彼女は言う。
血管肉腫の治療法は腫瘍の大きさや部位によって異なり、手術と化学療法の両方が行われる。それでも予後は非常に悪く、生存期間は2年未満であることが多い。
彼女の担当となった UC San Diego の心臓移植と cardiac amyloidosis(心臓アミロイドーシス)の責任者である UC San Diego の心臓専門医 Marcus Urey(マーカス・ウレイ)氏は、最も適切な治療法、例えば化学療法を開始するかどうかを決める前に、推定診断を確定する必要があると考え、医師たちは生検を試みた。しかし、必要な細胞を採取するためのプローブが腫瘍の外縁を通過できず、この処置は失敗した。
2度目の試みはさらに悪い結果となった:腫瘍は肺から心臓の左側に血液を運ぶ静脈を塞いでおり、肺動脈の血圧が高くなる肺高血圧症を引き起こしていた。Cresencia さんの右側の心臓は既に負担がかかっていたが、麻酔下で心不全と循環虚脱、いわゆるショックが引き起こされた。ショック状態では、循環系は体の組織に酸素と栄養を供給できなくなる。
Cresencia さんを救命するため、医師たちは患者の呼吸と心臓の機能を代行する生命維持装置に彼女をつないだ。彼女は10日間、ECMO(extracorporeal membrane oxygenation、体外膜酸素供給装置)につながれ、挿管され、鎮静剤を投与されながら、ようやく状態が安定したが、その間医師たちは何をすべきかを議論した。
正確に腫瘍が何であるかがわからないとしても可能な限り腫瘍を摘出する以外に選択肢はないと彼らは結論づけた。心不全が悪化していることを考えると「腫瘍をできる限り多く取り除こうとする以外に選択肢はありませんでした。手術をしなければ、彼女の予後は末期的と考えたのです」と Urey 氏は言う。
「私は外科医に、もし何もしなければ彼女は死ぬと伝えました」そう Urey 氏は振り返る。そして彼女の家族に伝えたところ「誰もが同じ考えでした。もし肉腫が見つかれば彼女は死ぬ危険性が高いが、何もしなければ死の確率は100パーセントでした。誰もが挑戦したいと思ったのです。」
すぐに手術が予定された。
CresenciaさんにはECMOを受けていた時の記憶も、手術に臨んだ時の記憶もない。しかし、ある時、Cresencia さんが Nguyen さん、両親、5人の兄弟の腕に油性マジックで“ I love you(愛してる)”と落書きしたことを、彼女の医師と Nguyen さんは覚えている。手術前夜、Cresencia さんは執刀医の Victor Pretorius(ビクター・プレトリウス)氏に fist bump(グータッチ)をし、彼女が書いたメモを彼に手渡した:“ You got this!(あなたならできる!)」。Pretorius 氏は彼女の不安を振り返る。「彼女の目には恐怖が浮かんでいました。彼女は本当に勇気があり、家族に別れを告げようとしていました。とても辛いことでした」。
手術は10時間近くかかり、外科医2人、麻酔科医3人、看護師4人、技師2人の11人体制で行われた。Crecensia さんをECMOにつないだ状態で Pretorius 氏は心臓を摘出、体外に出した状態で腫瘍を切除し、人工のブタの組織を用いて患部の左心房を再建した。また、4本ある肺静脈のうち3本の瘢痕組織を切除して再開通させた。彼によると4本目は瘢痕が強くうまく再開できなかったという。その後、医師らは彼女の心臓を体内に戻した。
Pretorius 氏によれば、摘出した腫瘍は「血管肉腫とは似ても似つかぬものでした。硬くて革のようでした。それが何なのかはわかりませんでした。組織の一部を採取して迅速診断のため病理医に送りました。1時間以内に電話がかかってきて、悪性細胞は見られないと言われたのです」。つまり、彼らが恐れていたような悪性の血管肉腫ではなかった。しかし、病理医は histiocytes(組織球)というタイプの白血球を確認、そしてそれによって彼女の病気の原因についての初めての真の手がかりが得られた。
The pathology report 病理報告書
最終的に病理報告がもたらされたが、解析の結果この腫瘍は組織球の増殖でできていることがわかった。組織球の増殖は、Rosai-Dorfman disease(ロサイ・ドルフマン病)として知られる非常にまれな疾患の特徴であり、小児、10代、および若年成人に最も多くみられる疾患である。Cleveland Clinic(クリーブランド・クリニック)によれば、20万人に1人しか発症しないという。免疫系の白血球の過剰な増殖が引き起こされ、多くの場合リンパ節で過度の腫大がみられる一方、それより頻度は低いが体内の他の部位にも発生することがある。
「ほとんどの医師がそれについて聞いたことがないのです」と UC San Diego の血液内科医で、現在彼女の観察を行っている Aaron Goodman(アーロン・グッドマン)氏は言う。「多くの医師がこの病気が何なのか知らないし見たこともないのです。そもそも信じられないほど稀な病気であり、彼女の場合は非常に稀な病気が非常に稀な形式で発症したのです。それは悪い場所にあり、死に至っていた可能性もありました」。
患者によっては、ステロイド、免疫系を抑える薬が用いられ、時には化学療法などの治療が行われる。しかしCresencia さんの場合、医師は腫瘍をすべて摘出したと考えているので「経過観察以外にすることはありません」と Goodman 氏は言う。
再発がないことを確認するために Cresencia さんは定期的にMRI検査を受けているが、今のところ再発は起こっていない。Goodman 氏によれば、再発する可能性はあるが、患者の何パーセントが再発するかは専門家でもわからないという。Cresencia さんの4月の直近の検査は完璧だった。
Cresencia さんは自分の試練については幸運に感じており、原因を解明してくれたことだけでなく“心からの親切”に対して UC San Diego の医師たちに“とても感謝している”と言う。
2月、バレンタインデーを含む週に、現在ベイエリアで一緒に暮らしている Cresencia さんと Nguyenさんは再びニューヨークを訪れた。彼女によればそれは「redemption trip(取り戻しの旅行)」とのことで、そこで彼らは毎日市内を歩いて探索したが何ら問題はなかったという。
「経験することができたすべての“初めて”を心からありがたいと思っています。その中にはこの街での最初の夜に降った雪も含まれている。「生粋のカリフォルニア人として、歩道を覆い、まつ毛をかすめるようなそんな雪を見たことがありませんでした。その夜、私は初めて雪玉を投げたんです!」
本例はきわめてまれな病気がきわめてまれな部位に発生した特殊なケースなので
ここでは Rosai-Dorfman disease(RDD、ロサイ・ドルフマン病)について
紹介する。
詳細については
JLSG(日本ランゲルハンス細胞組織球症研究グループ)のサイト
をご参照いただきたい。
本疾病は、1965年に Destombes が首のリンパ節の腫れと副鼻腔炎がある4症例を
報告したのが最初で、1969年に Rosai と Dorfman が同じ特徴のある患者34例を
まとめて報告している。
かつては反応性の病変とされてきたが
WHO分類では『組織球性腫瘍/樹状細胞性腫瘍』に分類されている。
RDD は20歳前後の黒人に多く、米国では20万人に1人の頻度でみられ、
年間約100例が新たに診断されている。
やや男性に多く発症年齢中央値は 20.6才。
本邦においては診断例は少なく年間10例以下と推定されている。
原因:
骨髄の造血前駆細胞(白血球、赤血球、および血小板の元になる細胞)に
遺伝子変異が起こり異常な組織球ができてしまうことが原因の一つと
考えられており、
約半数の患者に遺伝子変異が確認される(RAS と MEK1 が多い)。
自己免疫疾患、糸球体腎炎、リンパ腫などに合併することもある。
病型:
①リンパ節型
RDDの60%がこのタイプで両側の頸部のリンパ節の腫脹がみられる。
その他、脇の下や足の付け根、胸部のリンパ節の腫大をみることがある。
発熱、寝汗、体重減少などがみられる。
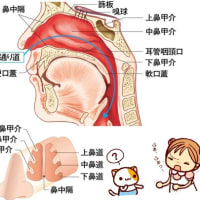
②リンパ節外型
RDDの40%を占める。発生部位では、皮膚、鼻腔、眼窩病変が10%、
骨病変が 5~10%、脳・脊髄病変が 5%、腎臓病変が 4%、肺病変が 2%、
胃腸病変が 1% となっている。
その他きわめてまれであるが本記事の患者のように、心腔内、肺動脈内、
心外膜など心血管に発生する例も報告されている。
20% の患者では複数の臓器に病変がみられる。
脳病変では頭痛、けいれん、手足の麻痺がみられることがある。
診断:
CT、MRI検査で病変を同定する。PET 検査を行うこともある。
血液検査では、白血球増多、炎症反応(CRP上昇・血沈亢進)、
γグロブリンの高値がみられる。
確定診断は病変の一部を採取した病理検査で確定する。
S100・CD14・CD68・CD163・OCT2 陽性の大型の組織球の増生を認める。
CD1a・CD207 は陰性となることが多い。
組織球の細胞質内に消化されない無傷のリンパ球・形質細胞などが取り込まれている
細胞内細胞陥入現象(emperipolesis、エンペリポレシス)が10%を超えて見られれば
診断が確定する。
治療:
病変数の少ないリンパ節型や皮膚病変のみの場合には無治療で軽快することがある。
多臓器病変がある例では副腎皮質ステロイド療法や
化学療法(ビンブラスチン/メソトレキセート、クラドリビン、クロファラビン)が
行われる。
摘出可能な病変については手術で切除する。
約70%の患者では治療により症状が改善するが、長期間にわたって
症状の悪化と軽快を繰り返すことがある。
遺伝子変異が確認されたケースでは変異している遺伝子の働きを抑える
分子標的療法が期待される。
2023年には、標準的な治療が困難な BRAF 遺伝子変異を有する進行・再発の
組織球症に BRAF 阻害薬である dabrafenbib(ダブラフェニブ)と
MEK 阻害薬である trametinib(トラメチニブ)の併用療法が承認されている。
ステロイドや抗がん剤治療に反応しないBRAFV600E変異のあるケースでは
本分子標的療法の有効性が期待される。
ただし、BRAFV600E変異は RDD 患者の中でも少ない(5%未満)ため、
その恩恵を受ける患者さんは少数に限られる。
本疾患全体では死亡率は10%前後であるが、
特に肺・腎・消化管・肝病変のある例では命に関わる経過をとることがある。
若年者にみられる病気のようであるが、最初から本疾患を鑑別診断に挙げるのは
無理なように思われる。






















※コメント投稿者のブログIDはブログ作成者のみに通知されます