研究者 齋藤 一樹 金 載勲
研究実施機関 科学技術振興事業団 創造科学技術推進事業
理化学研究所 ゲノム科学総合研究センター
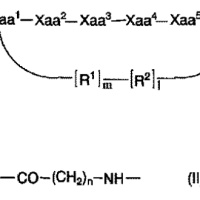
報告概要 非天然アミノ酸の1つである3-ヨードチロシンがリン酸化を受けた際に,そのリン酸化部位に特異的に結合するアダプタータンパク質の作製を検討した。すでに構造の解かれているGrb2のSH2ドメインとリン酸化チロシンを含むペプチドとの複合体の構造をもとに,リン酸化3-ヨードチロシンを結合するGrb2 SH2ドメインの変異体を設計した。チロシンの水酸基の隣に導入されたヨウ素原子を効率よく受容するためには,SH2ドメインの96位のセリン残基の側鎖を短くすることが必須と思われた。実際,セリン残基の側鎖(-CH2OH)をアラニン(-CH3),グリシン(-H)と小さくして行くと,グリシンまで小さくなったところで,リン酸化3-ヨードチロシンを含むペプチドの方をよく結合するようになった。 J-Store >> 研究報告コード R013000513
研究実施機関 科学技術振興事業団 創造科学技術推進事業
理化学研究所 ゲノム科学総合研究センター
報告概要 非天然アミノ酸の1つである3-ヨードチロシンがリン酸化を受けた際に,そのリン酸化部位に特異的に結合するアダプタータンパク質の作製を検討した。すでに構造の解かれているGrb2のSH2ドメインとリン酸化チロシンを含むペプチドとの複合体の構造をもとに,リン酸化3-ヨードチロシンを結合するGrb2 SH2ドメインの変異体を設計した。チロシンの水酸基の隣に導入されたヨウ素原子を効率よく受容するためには,SH2ドメインの96位のセリン残基の側鎖を短くすることが必須と思われた。実際,セリン残基の側鎖(-CH2OH)をアラニン(-CH3),グリシン(-H)と小さくして行くと,グリシンまで小さくなったところで,リン酸化3-ヨードチロシンを含むペプチドの方をよく結合するようになった。 J-Store >> 研究報告コード R013000513