がんの予防や治療における漢方治療の存在意義を考察しています。がん治療に役立つ情報も紹介しています。
「漢方がん治療」を考える
408)間質細胞をターゲットにするがん治療:膠原病の治療とがん治療の接点
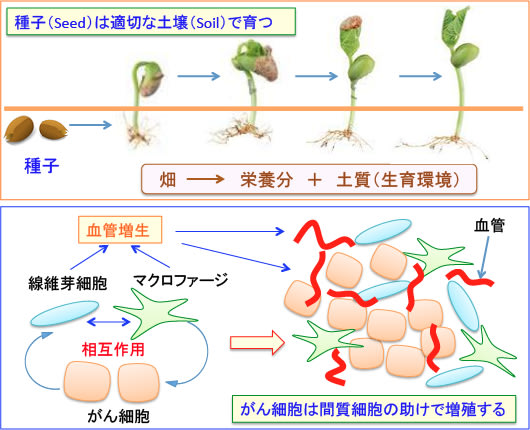
図:植物の種子(seed)が発芽して育つためには畑の土(soil)からの栄養分や土質(生育環境)の条件が重要。栄養分が不足し生育環境が悪ければ、植物は育たない。同様に、がん細胞も間質の炎症細胞(マクロファージなど)や線維芽細胞や血管によって生存や増殖が維持され刺激されている。がん細胞と間質細胞は密接に相互作用を行うことによってがん組織は増大する。したがって、がん治療においてより効果的な抗腫瘍効果を得るためには、がん細胞と同時に、間質の細胞もターゲットにすることが重要。
408)間質細胞をターゲットにするがん治療:膠原病の治療とがん治療の接点
【低用量の抗がん剤が膠原病の治療に使われる理由】
慢性関節リュウマチの治療薬にメトトレキサート(Methotrexate)という抗がん剤が使用されます。メトトレキサートは葉酸代謝拮抗薬で、DNA合成を阻害することによって抗がん作用を示します。
がん治療の場合は1回に数100mg、場合によっては数1000mgを投与してがん細胞を死滅させることを目標にします。
一方、リュウマチの治療には、1週間に数mgの投与です。つまり、がん治療に使われる量の100分の1程度しか使われません。
この場合は、免疫細胞や炎症細胞の働きを抑制して、リュウマチの慢性炎症を引き起こしている免疫グロブリンや炎症性サイトカイン(インターロイキンなど)の産生を抑制したり、滑膜組織や軟骨組織の破壊にかわるコラゲナーゼの産生抑制、異常な血管新生や滑膜増生を抑制する作用などによって、効果を発揮します。
リュウマチ治療薬としては免疫抑制剤に分類されますが、有効性が高く、関節リュウマチの治療に最も多く使用されています。
また、シクロホスファミドという抗がん剤も慢性関節リュウマチなどの様々な膠原病(自己免疫疾患)の治療に用いられます。
シクロホスファミドはナイトロジェンマスタードの流れをくむアルキル化剤で、DNAをアルキル化してがん細胞(分裂している細胞)を死滅させます。
がん治療の場合は、1日100~200mgの服用で、自己免疫疾患の場合は1日50mg程度の低用量を服用します。
低用量の場合は、免疫細胞や炎症細胞の働きを抑制して炎症反応を抑える作用(抗炎症作用)によって自己免疫疾患を治療します。
シクロホスファミドとメソトレキサートは、自己免疫疾患に使用されるのとほぼ同じ服用量が、がんのメトロノミック・ケモテラピーでも使用されています。
メトロノミック・ケモテラピーではがん細胞を死滅させるのではなく、がん間質の細胞に作用して炎症性サイトカインの産生や血管新生を阻害することによって抗腫瘍効果を得ることを目標にしています。
つまり、自己免疫疾患(膠原病)の治療に炎症細胞や血管内皮細胞や線維芽細胞の働きを抑制することが有効なのと同様に、がん組織に存在する炎症細胞や血管内皮細胞や線維芽細胞の働きを抑制するとがん細胞自体の増殖や転移も抑制できることが明らかになっているのです。
【がんは治ることのない創傷】
がん細胞は増殖や生存に関連する遺伝子の異常によって、増殖の制御が壊れたために「無制限に増殖する」ようになった細胞です。がん細胞は無限の「自律増殖能」を持つのが特徴であるため、がん細胞だけで増殖や転移が可能と思われるかもしれません。しかし、がん細胞だけでは生存も増殖も転移もできません。
がん細胞が生存し増殖していくためには、がん細胞に酸素や栄養を与える血管や、生存や増殖を支持する因子を産生する線維芽細胞や炎症細胞の存在が必要です。転移するためには、ケモカインやケモカイン受容体や増殖因子などの働きが必要です。(406話、407話参照)
がん組織は、がんの実質細胞である「がん細胞」とそのがん細胞を養う「間質組織」の相互作用によって成り立ちます。間質組織には血管やマクロファージなどの炎症細胞や結合組織を作る線維芽細胞などが存在し、これらの細胞ががん細胞の生存や増殖を維持するために様々な働きを行っています。
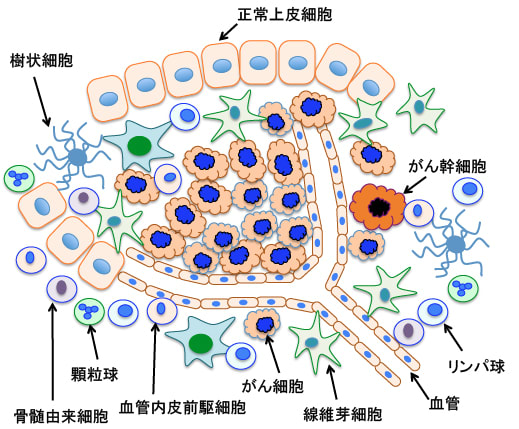
図:がん組織はがん細胞だけでなく、間質に存在する様々な正常細胞から構成されている。がん細胞の増殖や転移は、がん細胞と間質細胞の相互作用によって決められる。がん細胞だけでは増殖も転移もできない。血管内皮細胞や炎症細胞や線維芽細胞や骨髄由来細胞など様々な細胞ががん細胞の増殖や浸潤や転移に関わっている。血管新生の阻害、免疫細胞の活性化、炎症細胞や線維芽細胞の働きの阻害、結合組織によるがん細胞の封じ込めなど、正常細胞をターゲットにした様々な治療法を併用することによってがんの治療効果を高めることができる。(参考:Transl Cancer Res. 2013 August 1; 2(4): 309–319のFig1)
正常組織もがん組織も上皮細胞と間質細胞の相互作用によって形態や機能が維持されています。
がん細胞は様々なケモカインや増殖因子を分泌して、血管内皮細胞や炎症細胞や線維芽細胞などの間質細胞をがん組織に動員しています。一方、動員された線維芽細胞やマクロファージやリンパ球も様々な因子を産生・分泌してがん細胞の増殖や浸潤や転移を促進しています。つまり、がん組織内ではがん細胞と間質の細胞の相互作用によって増大や転移が制御されているのです。
がん組織におけるがん細胞と間質細胞の関係は、種子(seed)と土壌(soil)の関係に似ています。種子は土壌の条件が良くなければ育ちません。同様に、がん細胞は間質の条件が悪ければ増殖も転移もできません。(トップの図参照)
植物がよく育つように畑を耕したり肥料をやるのと同様に、がん組織の間質の細胞はがん細胞が育つように環境を整える働きをしているのです。
本来は宿主のためにがん細胞に立ち向かわなければならないのに、がん細胞に操られて、がん細胞の味方になっていると言えます。これが、間質細胞をターゲットにしたがん治療が有効な理由です。
正常組織は異物や病原菌の侵入を受けると炎症反応を起こして異物や病原菌を排除し、ダメージを修復すると、炎症反応は収束します。
自己免疫疾患(膠原病)の場合は、免疫系の異常によって自己の成分を自分の免疫細胞が攻撃するため、炎症反応が慢性化し、その結果、組織のダメージが持続し、さらに炎症が悪化するという悪循環を形成しています。そのため、自己免疫疾患の治療は、基本的には免疫抑制作用のある薬や抗炎症作用のある薬が主体になります。
がんは「治ることのない創傷」(Tumors are “wounds that do not heal.”)という考えがあります。がん細胞は正常組織を浸潤してダメージを与え、組織修復と炎症反応が持続し、いつまでたっても収束しない状況です。慢性炎症と同様に、炎症が収束せず、永遠に創傷治癒過程(=炎症反応)が続いている状態と同じということです。
がん細胞は正常な間質細胞を自分の都合の良いように操るハッカー(他人のコンピューターに侵入して制御したり破壊する人)だという考え方もあります。つまり、がん細胞自身の増殖や生存を維持するために正常細胞を動員してがん細胞の増殖に有利な間質組織を作っています。
したがって、がん細胞が消滅するまで、間質細胞のがん細胞支配は続きます。しかし、このがん組織の間質における慢性炎症状態を正常化すると、あるいはがん細胞と間質細胞の相互作用を断つと、がん細胞の増殖や生存を阻害できる可能性があります。
つまりこれが、自己免疫疾患のような慢性炎症の治療ががん治療に使える理由になります。
【メトロノミック・ケモテラピーの実際例】
通常の抗がん剤治療は、副作用が耐えられる最大量(最大耐用量)を投与してがん細胞を短期間で死滅させる方法が基本になっています。
メトロノミック・ケモテラピー(Metronomic Chemotherapy)とは、メトロノームのように規則的に低用量の抗がん剤を頻回に投与していく抗がん剤治療法です。メトロノミック・ケモテラピーについては397話で解説しています。
メトロノミック・ケモテラピーには様々な抗がん剤が使われていますが、その基本は副作用のでない低用量を継続して投与することです。
ここではシクロホスファミドやメトトレキセートを使った報告の幾つかを紹介しておきます。
① Long-term complete response in a patient with liver metastases from breast cancer treated with metronomic chemotherapy.(メトロノミック・ケモテラピーで治療した乳がんの肝臓転移の患者における長期間の完全奏功)Tumori. 100(3):79e-82e.2014年 doi: 10.1700/1578.17238.
肝臓転移のある62歳の乳がん患者の症例報告です。
シクロホスファミド(50mg/日、経口)とメソトレキセート(2.5mg x 2回/日、週2日)で治療を行い、開始してから6ヶ月後のCT検査で完全奏功を認め、60ヶ月経過しても完全奏功の状態を維持しています。
② Low-dose "metronomic chemotherapy" with oral cyclophosphamide and methotrexate in metastatic breast cancer: a case report of extraordinarily prolonged clinical benefit.(転移性乳がん患者における経口のシクロホスファミドとメトトレキセートによる低用量メトロノミック・ケモテラピー:顕著な長期間の臨床的有効性を認めた1例)Ecancermedicalscience. 2012;6:275. doi: 10.3332/ecancer.2012.275. Epub 2012 Oct 18.
34際女性の骨転移のある乳がん患者で、シクロホスファミド(50mg/日、経口)とメソトレキセート(2.5mg x 2回/日を週の第1日目と4日目の週2日投与)で治療を行い、3.5年間の奏功(腫瘍縮小)を認めています。
治療法は①の症例と同じ方法ですが、治療を行った施設は異なります。
③ Metastatic primary duodenal adeno-carcinoma responding to metronomic oral cyclophosphamide chemotherapy.(経口シクロフォスファミドによるメトロノミック・ケモテラピーが奏功した転移のある十二指腸腺がん)Indian J Palliat Care. 2014 Sep;20(3):239-42. doi: 10.4103/0973-1075.138402.
52歳女性で十二指腸原発の中分化腺がんです。肝臓や鎖骨上リンパ節や脊椎などに転移を認め、全身状態は不良です(パーフォーマンス・ステータスは40: 動けず、適切な医療および看護が必要な状態)。
脊椎部の放射線治療と並行して1日50mgのシクロホスファミドの内服とビタミン補充などの保存的治療を受けました。
治療開始から2週後には症状の改善を認め、12週後の検査で原発巣と転移巣の完全奏功(目で見える大きさの腫瘍の消失)を認め、32週間の無増悪生存期間を得られました。
④ Oral metronomic cyclophosphamide with and without methotrexate as palliative treatment for patients with metastatic breast carcinoma.(転移した乳がん患者における緩和治療としての経口低用量シクロホスファミド±メトトレキセート)Anticancer Res. 32(2):529-36. 2012年
ホルモン療法に耐性になり、さらに抗がん剤治療にも抵抗性になっている61例の進行した乳がん患者を対象に、22例は1日50mgのシクロホスファミドをがんが進行するまで内服、39例は1日50mgのシクロホスファミドと週2回2.5mgのメトトレキセートを服用しています。
平均6ヶ月間の部分奏功が18%、平均5ヶ月間の病状安定が35%に認められ、病状コントロール率は52%でした。症状の改善は54%に認められました。
副作用は極めて軽微で容易に制御できました。グレード3以上の血液学的な副作用は認めず、20例(33%)でトランスアミナーゼの上昇(肝機能障害)が主にメトトレキセートを併用した群で認められました。
通常の治療(ホルモン療法と抗がん剤治療)を受けて効果が出なくなった乳がん患者に対して、低用量のシクロフォスアミド±メトトレキセートのメトロノミック・ケモテラピーは有効な治療と言えるという結論です。
標準治療による抗がん剤が効かなくなり、がんが増殖している状況で、半数以上の症例に半年間程度の症状の改善と腫瘍の増殖停止あるいは縮小を認めたということです。
⑤ Low-dose oral methotrexate and cyclophosphamide in metastatic breast cancer: antitumor activity and correlation with vascular endothelial growth factor levels.(転移した乳がんにおける低用量の経口メトトレキセートとシクロフォスファミド治療:抗腫瘍効果と血管内皮増殖因子の血中レベルとの関連)Annals of Oncology 13: 73-80, 2002年
この論文は、上記の①~④の論文のシクロフォスファミドとメトトレキセートを使ったメトロノミック・ケモテラピーの方法の基になった報告です。この論文の要旨を日本語に訳しています。
【要旨】
研究の背景:抗がん剤治療はがん細胞に対する直接的な細胞毒性によって効果を発揮すると考えられている。シクロホスファミドやメトトレキセートやアントラサイクリン系薬剤やタキサン系薬剤など幾つかの常用されている抗がん剤には血管新生阻害作用による抗腫瘍効果も指摘されている。
対象患者と方法:転移を有する乳がん患者を対象に低用量の経口メトトレキセートとシクロホスファミドによるメトロノミック・ケモテラピーの臨床的な抗腫瘍効果と血管内皮増殖因子(VEGF)の血中濃度への効果を検討した。
メトトレキセートは週の第1日目と2日目に2.5mgを2回(1日5mg)、シクロホスファミドは1日50mgを連日服用した。
結果:64例が登録し、63例が解析された。ECOG(Eastern Cooperative Oncology Group)のパフォーマンスステータスはグレード0(無症状で社会活動ができ、制限を受けることなく、発症前と同様に振舞える。)かグレード1(軽度の症状があり、肉体労働は制限を受けるが、歩行、軽労働、座業はできる)であった。
50例では2ヶ所以上の転移があり、51例では治験参加時にがんの進行を認めた。
32例は1つのレジメン(治療方式)による抗がん剤治療を受け、20例は2つ以上のレジメンでの抗がん剤治療を受けていた。
治療効果を評価できた63例のうち、完全奏功(腫瘍が目で見えないレベルに縮小)が2例、部分奏功が10例、全体の奏功率は19%であった。臨床的有効性(完全奏功+部分奏功+24週以上の病状安定)の率は31.7%(95%信頼区間:20.6~44.7%)であった。
グレード2以上の白血球減少は13例で認められた。VEGFの血中濃度の中央値は、治療前の315 pg/ml (95% 信頼区間: 245 ~ 435 pg/ml)から、メトロノミック・ケモテラピー開始2ヶ月後は正常者の基準値のレベルである248 pg/ml (95% 信頼区間:205 ~ 311 pg/ml)に統計的有意に減少していた(P <0.001)。腫瘍が縮小した患者も縮小しなかった患者も同程度の血中VEGF値の減少を認めた。治療を継続している患者の6ヶ月後のVEGFの血中濃度の中間値は195 pg/ml (95%信頼区間: 96 ~ 355)で基準値の中央値よりも有意に低い値を示した(P = 0.001)。
結論:シクロホスファミドとメトトレキセートの低用量の継続投与によるメトロノミック・ケモテラピーは毒性(副作用)が軽微で、高度に抗がん剤治療を受けてきた進行した乳がん患者においても有効な抗腫瘍効果が認められた。この治療によって血清VEGF濃度の低下を認め、メトロノミック・ケモテラピーの抗腫瘍効果のメカニズムとして、がん細胞に対する直接的な抗腫瘍効果よりも、血管新生阻害作用の可能性が示唆された。
【メトロノミック・ケモテラピーに他の治療を併用して抗腫瘍効果を高める】
前述のように、標準的な抗がん剤治療を繰り返し受け、もう効果が得られないという「匙を投げられた」状況になっても、シクロホスファミドとメトトレキサートを併用したメトロノミック・ケモテラピーは半数程度の例で症状の改善や6ヶ月程度の延命効果が得られ、中には長期の生存例も認められるという結果が得られています。
メトロノミック・ケモテラピーは乳がんだけでなく、前立腺がんや肺がんや大腸がんなど多くの腫瘍で報告されています。
私自身も低用量のシクロホスファミドやメトトレキサートなどを用いたメトロノミックケモテラピーを行っていますが、効果に限界を感じることも多々あります。そこで、このようなメトロノミック・ケモテラピーに、さらにがん細胞の増殖阻害や、間質細胞からのケモカインや増殖因子の産生を抑えるような治療を併用すると抗腫瘍効果を高めることができます。
実際に、駆虫薬のメベンダゾール(Mebendazole)やシクロオキシゲナーゼ-2阻害薬のセレコキシブ(celecoxib)や、その他抗炎症作用のあるサプリメントや医薬品を併用した治療が検討されています(405話参照)。
いろんな薬を組み合わせると費用は増えていきますが、有効性は高まります。
【医療費を減らすインセンティブとは】
今週のネットの情報によると、「2012年度に病気やけがの治療で全国の医療機関に支払われた医療費の総額(国民医療費)が、前年度比6267億円増(1.6%増)の39兆2117億円だった」と厚生労働省が発表したそうです。
国民1人当たりでは30万7500円で、いずれも6年連続で過去最高を更新しています。医療費が国民所得に占める割合は11.17%だと言うことです。
高齢化に加え、医療技術の高度化や薬の高額化で費用が膨らんだことが主な要因だと言っています。薬剤費が25%を占めているそうです。
国によって医療の事情は異なりますが、その大きな原因は経済状況です。
米国や日本のような経済大国では、価格の高い新薬を多く使うことができます。一方、所得水準が低い国では、薬価が高いという理由だけで新薬が認可されない状況にあります。このような国では、医療費を抑えるために安価な薬を使って効果を高めるようなインセンティブ(動機づけ)が働きます。(先進国でも英国のように薬価の高い薬は保険で認めない国も増えている)
「インセンティブ」とは「人や組織の意欲を引き出すための刺激や誘因」のことで、「費用の高い薬を使えない」という国内事情があると、必然的に「安価な薬を工夫して治療を行おう」ということになります。
日本は、国民皆保険制度や高額療養費制度などによって、1ヶ月に何十万円もする抗がん剤治療でも自己負担は数万円ですむので、気兼ねなく高額な新薬が使用されています。しかし、経済的に厳しい国では、高額な新薬を使うことはできません。
そこで、安価で有効な薬を見つけたり、薬の使い方や組合せを工夫して効果を高めようとする研究のインセンティブが働きます。残念ながら日本ではそのようなインセンティブは働きません。新しく開発された高額な薬をどんどん使うのが患者のためだと考えているので、高額な抗がん剤を多く使うのが医療レベルを上げると考えています。利益追求をインセンティブとする製薬産業の言いなりになって、高額な医薬品を何の躊躇もなく使う傾向が強いのが日本のがん治療の現状です。
抗がん剤に関しては「効く、効かない」という議論が主体ですが、「費用対効果」の観点からの議論も重要です。苦しい副作用を伴った数ヶ月の延命のために何十万円、何百万円の医療費を使うことが本当に意味があるのかの議論が必要です。
既存の医薬品から抗がん剤をスクリーニングする「医薬品再開発(Drug Repositioning):
400話参照」や、安価な抗がん剤を使って有効性を高める「メトロノミック・ケモテラピー(397話参照)」は、医療費を減らす目的で多くの国で研究が行われていますが、日本ではほとんど注目されていません。そのような研究を行う理由もインセンティブもないからです。新薬を多く使う方が患者さんのためだと考えるからです。
がんの治療を自由診療で行っていると、健康保険も高額療養費制度の恩恵も受けません。したがって、安価で有効性の高い治療を追求せざるを得ません。後進国が安価な費用でがん治療の有効性を高めるにはどうしたらよいかを検討するのと同じインセンティブが働きます。このブログで既存の医薬品や漢方薬やサプリメントを利用した「安価ながん治療」を考察するのはそのような理由があります。
さて、医療の費用対効果を評価する指標にQALY(質調整生存率、Quality-adjusted Life Year)があります。これは「生活の質を調整した生存年」のことで「生活の質 x 生存年数」で決められます。生活の質についてはEQ-5Dという5項目からなる患者さんへのアンケート結果を数値化したものを使います。
簡単に言うと、生活の質を低下させずに1年間延命すれば1QALYになります。生活の質が半分になっても2年間延命すれば1QALYになります。
英国の保険制度では、QALY(生活の質を落とさずに1年間延命)あたり2万~3万ポンド(現在の為替レートで340~510万円程度)を目安にして、それ以上の高額な(費用対効果が悪い)医薬品は保険で償還しないというルールがあります。
例えば、英国のNICE(国立医療技術評価機構:National Institute for Health and Clinical Excellence)は大腸癌治療剤であるアービタックス、アバスチン、ベクティビックスの3剤について、保険償還しない判断を下しています。それぞれの薬のQALYがNICEの規定した3万ユーロの3倍以上だったためです。
分子標的薬など最近の抗がん剤の新薬は極めて高額です。6ヶ月間の延命効果があっても、その費用が1000万円を超えるのが普通です。
例えば、副作用の多い最大耐用量を投与する抗がん治療で、生活の質が半分になって6ヶ月の延命効果がある薬の場合、QALYは0.25であるため、この治療での6ヶ月間の薬剤費が7500ポンド(約130万円)を超えると保険で償還されないことになります。
このようなルールは患者さんが新薬の恩恵を得られないという問題がありますが、医療費高騰を避けるためには、仕方ないという考えです。
そのため、日本で普通に使われているような分子標的薬が、英国ではかなりの数が保険償還が承認されていません。いずれ日本もそのような状況になると思われます。そうなれば、製薬会社にも、費用対効果のよい医薬品を開発するインセンティブが増加するかもしれません。
シクロホスファミドやメトトレキセートを使ったメトロノミックケモテラピーは1ヶ月当たりの薬剤費は数千円です。生活の質を落とさずに平均6ヶ月の延命効果があったとして、数万円/QALYになります。
このような安価な抗がん剤治療の効果を高める方法を研究した方が、将来的には役にたつように思います。
画像をクリックするとサイトに移行します。
| « 407)ケモカイ... | 409)カフェイ... » |





