がんの予防や治療における漢方治療の存在意義を考察しています。がん治療に役立つ情報も紹介しています。
「漢方がん治療」を考える
330)ケトン食で頭が良くなる?(2):記憶とヒストンアセチル化
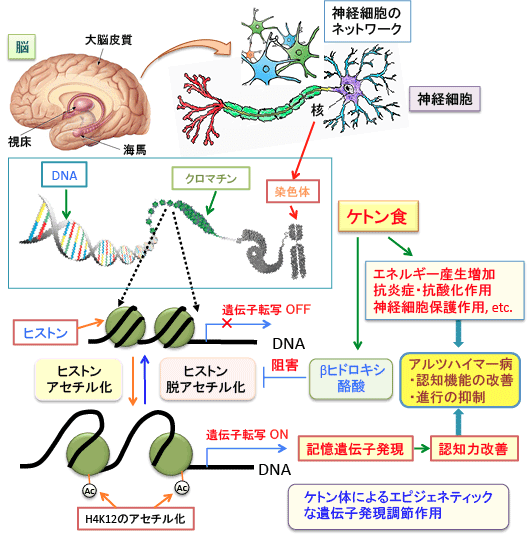
図:ケトン食は、神経細胞におけるエネルギー産生の改善や抗炎症・抗酸化作用やアポトーシスを阻止する作用など様々なメカニズムによって、神経細胞を変性や細胞死から保護する作用がある。さらに、βヒドロキシ酪酸はヒストン脱アセチル化酵素を阻害することによって、エピジェネティックは遺伝子発現調節作用によって認知機能や長期持続記憶を改善する可能性が指摘されている。これらの総合的な作用によってケトン食はアルツハイマー病の認知機能の改善や病気の進行を抑制する作用が期待できる。これらの作用機序はアルツハイマー病以外の多くの神経変性疾患(パーキンソン病、筋萎縮性側索硬化症、ハンチントン病など)に対する有効性も示唆されている。
330)ケトン食で頭が良くなる?②:記憶とヒストンアセチル化
【ヒストンのアセチル化は記憶力を高める】
ケトン食がアルツハイマー病(認知症)の治療に有効であることは327話で紹介しました。
ケトン食で産生が高まるβヒドロキシ酪酸がヒストン脱アセチル化酵素を阻害してヒストンのアセチル化を亢進することは322話で紹介しました。
ケトン体はグルコースが枯渇したときに肝臓で脂肪酸が燃焼しての産生されます。ケトン体は血液脳関門を通過し、拡散あるいはモノカルボン酸トランスポーターによって神経細胞内に入り、神経細胞のエネルギー源となります。グルコースの代替エネルギー源となる以外に、以下のような様々なメカニズムで神経細胞を傷害から守る作用があります。
①ケトン体は神経細胞のミトコンドリアを増やし、ケトン体自体がエネルギー源となって神経細胞におけるエネルギー産生を増やす、
②ケトン体は抗炎症作用があり、さらにミトコンドリアにおける活性酸素の産生を減らし酸化障害を軽減する、
③ケトン体はアポトーシスの過程を阻害することによって神経細胞死を抑制する、
④ケトン体はヒストンアセチル化を亢進して認知機能を高める、
など様々な機序が報告されており、恐らく、これら全ての機序が総合的に作用して効果を発揮していると考えられます。ここでは④の「ケトン体による遺伝子発現のエピジェネティックな発現調節作用の関与」について考察します。
さて、記憶のメカニズムには神経細胞におけるヒストンのアセチル化が関与していることが最近の研究で明らかになっています。最近の論文で以下のような総説があります。
The potential of HDAC inhibitors as cognitive enhancers.(認知力増強剤としてのヒストン脱アセチル化酵素阻害剤の可能性)Annu Rev Pharmacol Toxicol. 53:311-30. 2013年
【要旨】
ヒストンのアセチル化は、中枢神経系における遺伝子発現を調節しているエピジェネティックな修飾である。遺伝子の転写は長期持続性記憶(long-lasting forms of memory)において重要な役割を果たしており、一般的に、ヒストンのアセチル化は長期持続性記憶に有利に働き、一方ヒストン脱アセチル化は長期持続性記憶を妨げる働きをする。
ヒストンのアセチル化はヒストン脱アセチル化酵素阻害剤の使用によって薬理学的に調整が可能であるため、ヒストンのアセチル化は認知力を高めるために治療のターゲットとして特に注目されている。
ヒストンのアセチル化は普遍的に存在するので、ヒストン脱アセチル化酵素阻害剤は、神経発達障害や神経変性疾患における認知障害の治療だけでなく、健常人に対する認知力増強の方法としても効果が期待できる。
この総説では、認知治療や認知増強剤としてのヒストン脱アセチル化酵素阻害剤野状況をまとめ、その”エピジェネティック・プライミング(epigenetic priming)”という作用機序の新しい考え方を紹介し、その多大なる有望性にもかかわらず、その使用に際しての注意点も解説する。
この論文は、米国のマサチューセッツ工科大学(MIT)の脳と認知科学部門(Department of Brain and Cognitive Sciences)のピカワー学習・記憶研究所(Picower Institute for Learning and Memory)からの報告(総説)です。
MITのピカワー学習・記憶研究所は利根川進博士(1987年にノーベル生理学・医学賞受賞)が1994年に設立し2006年まで所長を勤めていた研究所で、脳科学や認知科学の研究では世界でトップレベルの研究所です。
この論文の著者の一人のLi-Huei Tsai博士はこの研究所の現在の所長です。
Tsai博士らの研究グループは、アルツハイマー病のマウスの実験モデルを用いた研究で、神経細胞が大量に死滅した状態においても、ヒストン脱アセチル化酵素阻害剤を投与すると、シナプス形成や神経細胞の樹状突起の成長が促進され、学習機能が維持され、長期維持記憶が回復することを報告しています。
この実験結果は、神経細胞の死滅や変性が高度に起こった状況でも(つまり、認知症がかなり進行した状態になっても)、ヒストンのアセチル化とクロマチンの再形成というエピジェネティックなメカニズムによって、学習や記憶の増強に効果が期待できることを示唆しています。
そして、ヒストン脱アセチル化酵素阻害剤がアルツハイマー病の治療に有効であることを強く示唆しています。
ヒストン脱アセチル化酵素(Histone Deacetylase:HDAC)はクロマチン構造において主要な構成因子であるヒストンの脱アセチル化を行う酵素で、遺伝子の転写制御において重要な役割を果たしています。HDACファミリーの分子は現在HDAC1~11まで同定されていますが、記憶や学習に関連しているのはHDAC2であることが報告されています。
(参考文献:HDAC2 negatively regulates memory formation and synaptic plasticity(HDAC2は記憶の形成とシナプス可塑性を負に調節する)Nature 459, 55-60, 2009年)
マウスのアルツハイマー病のモデルや人間のアルツマイハー病患者の脳組織にはHDAC2の発現量が増加していることが報告されています。そして、マウスのアルツハイマー病の実験モデルでHDAC2のレベルを正常化すると、高度の神経細胞変性の状態であっても認知機能が回復することが報告されています。
ただし、HDAC1やNAD+依存性脱アセチル化酵素のSIRT1は神経細胞保護的に作用するので、単純にヒストンのアセチル化(つまり、ヒストン脱アセチル化酵素の阻害)が全てに良いわけではないので、問題は複雑です。
ただし、アルツハイマー病などの認知障害や長期維持記憶の回復にHDAC2の阻害剤は効果が期待されています。
ケトン食で血中に増加するβヒドロキシ酪酸がクラスIヒストン脱アセチル化酵素であるHDAC1とHDAC2を阻害する作用があることは島津忠広博士のScienceの論文で報告されています(322話参照)
Tsai博士らの研究結果によるとヒストン脱アセチル化酵素2(HDAC2)の阻害は認知機能の増強につながるが、HDAC1の阻害はHDAC1の神経細胞保護作用を阻害してしまう可能性があります。しかし、ケトン食ではヒストンアセチル化というエピジェネティックな作用機序の他に、抗炎症、抗酸化、抗アポトーシスなどの機序による神経細胞保護作用が報告されています。したがって、ケトン体によるヒストン脱アセチル化酵素2(HDAC2)の阻害作用は、アルツハイマー病の治療に対する有効性(認知機能の回復と増強)を強く期待させると思います。
アルツハイマー病でなくても、高齢になってくると記憶力が低下します。老化に伴う短期記憶力の低下に対しても、ヒストンアセチル化酵素の阻害剤によって改善することがマウスを使った実験で示されています。
Altered histone acetylation is associated with age-dependent memory impairment in mice.(ヒストンアセチル化の状態の変化はマウスにおける加齢による記憶力低下と関連している)Science. 328(5979):753-6. 2010年
この論文はドイツの欧州神経科学研究所(European Neuroscience Institute)からの報告です。
16ヶ月齢(実験用マウスの平均寿命は800~900日程度のため人間では40~50歳程度)の中年マウスは、若い(3ヶ月齢や8ヶ月齢)と比べて海馬依存的な短期記憶力が著しく低下しています。この中年マウスと若年マウスを用いて記憶実験の前後における脳内のヒストンの状態を比較しています。
若年マウスでは学習訓練後1時間でヒストンH4のリジン12(H4K12)のアセチル化が顕著に促進されたのに対し,中年マウスではそのような変化は認められませんでした。さらに、若年マウスでは訓練前後で2,229個の遺伝子発現に差があったのに対し,中年マウスではわずか6遺伝子しか差がなく、若年マウスで発現量の変化した遺伝子のうち,1,539個が記憶学習に関連することが知られている遺伝子であったということです。
つまり、年を取ると学習しても記憶遺伝子の発現が起こりにくくなっているので、学習能力が低下するということです。そして、記憶遺伝子の発現亢進に関わっているのがヒストンのアセチル化によるエピジェネティックな調節によるもので、高齢になるとこのようなエピジェネティックな遺伝子発現の調節がうまくいかないので、記憶力を低下するということです。
そして、中年マウスの海馬にヒストン脱アセチル化酵素阻害剤を注入すると、学習訓練後のヒストンH4K12のアセチル化が促進され、記憶関連遺伝子の発現も誘導され,さらに学習記憶試験の成績も有意に向上したという結果を報告しています。
海馬における神経細胞のヒストンH4K12のアセチル化を促進するようなヒストン脱アセチル化酵素阻害剤を使えば、老化に伴う記憶力低下を防止することも可能という結果です。
ケトン食でヒストンH4K12のアセチル化が亢進するかどうかの研究はまだ報告がありませんが、動物実験や臨床試験でケトン食は記憶力を亢進しているので、その可能性は高いかもしれません。つまり、ケトン食によるアルツハイマー病の認知機能の改善にケトン体によるエピジェネティックは遺伝子発現調節作用が関与している可能性が強く示唆されます。
【超高齢者はがんとアルツハイマー病の発症率が低い】
超高齢者ではがんの発症率もがんによる死亡率も低下することは315話で解説しました。
一般的には、がん細胞は遺伝子変異の蓄積と免疫力の低下によって発生するので、がんの発生率は加齢とともに上昇すると考えられていますが、実際は、発がん率は80歳代をピークにして、以後は年齢とともに急速に減少することが明らかになっています。その理由として、100歳以上の超高齢まで生きるような人は、がんに対する抵抗力が高い体質を持っていることが示唆されています。つまり、抗酸化力や免疫力やストレスに対する抵抗力が高い遺伝的素因をもっているから、超高齢まで生存し、そのような人はがんにもなりにくい体質や遺伝的素因を持っているという考えです。
アルツハイマー型認知症の発症についても同様の現象が認められています。
認知症が神経細胞の変性や脱落で発生するなら、年齢が高くなるほど認知症の発症率は増えるはずです。しかし、100歳を超えるような人では、80歳代の人に比べて認知症の発症率が低い、あるいは発症しても遅れて発症することが報告されています。
例えば、100歳以上の人の15~25%は認知機能は正常で、100歳で何らかの認知障害がある人でも、その発症年齢の平均が92歳で、認知症の発症が明らかに遅くなっているという報告があります。つまり、100歳を超えるような人は、認知症に対する抵抗力が高い可能性が示唆されています。
(参考:Centenarians who avoid dementia.(認知症のない百寿者)Trends Neurosci 27(10): 633-6, 2004年)
両親が長寿だとアルツハイマー病になりにくいという報告もあります。
Exceptional parental longevity associated with lower risk of Alzheimer's disease and memory decline.(例外的な親の長寿は、アルツハイマー病や記憶力低下の発症リスクの低下と関連している)
J Am Geriatr Soc. 58(6):1043-9. 2010年
この論文では、米国のニューヨークのBronxに在住の424人(75歳から85歳でスタート時に認知症にかかっていない)を対象に1980年にスタートし、12~18ヶ月おきに神経学的な検査を行いながら23年間の追跡調査を行っています。
両親のうち一人以上が85歳以上まで生きた人の群と、両親のどちらも85歳より若く亡くなっている人の群の2群に分けて、アルツハイマー病や認知障害の発症頻度を比較しています。
便宜的に、前者の群(親の一人以上が85歳以上まで生存)を長寿家系とし、後者(両親のどちらも85歳未満で死亡)を非長寿家系とすると、424人のうち長寿家系は149人(35%)、非長寿家系は275人(65%)で、調査開始時の平均年齢はどちらも79歳でした。
非長寿家系の人に比べて、長寿家系の人にアルツハイマー病が発症するリスクのハザード比は0.57(95%信頼区間:0.35-0.93)でした。長寿家系の人は非長寿家系の人に比べて、記憶力の低下の速度が遅いという結果も得られています。
つまり、長寿の家系の人はアルツハイマー病の発症や記憶力が低下する速度が遅く、長寿に関連する因子と認知症の発症を予防する因子が共通する可能性が示唆されています。
長寿日本一や世界一の人の話がニュースになることがありますが、確かに、このような超長寿の人は認知機能が保たれていることが多いように感じます。
長寿とアルツハイマー病に対する抵抗性の両方に共通する因子を活性化する薬や食品成分や食事療法が見つかれば、認知症にならずに長寿を達成できることになります。(多分、このような因子はがん予防にも効果があるはずです)
【ケトン食はアルツハイマー病の改善に効果が認められている】
食事内容によって、アルツハイマー型認知症の発症リスクが異なることは多くの研究結果が支持しています。例えば、地中海式ダイエットをしている人にはアルツハイマー型認知症の発症が少ないことはよく知られています。野菜や魚の摂取がアルツハイマー型認知症の発症を減らす可能性が指摘されています。
ケトン食がアルツハイマー型認知障害を軽減することは複数の臨床試験で報告されています。以下のような報告があります。
Effects of beta-hydroxybutyrate on cognition in memory-impaired adults.(記憶力に障害のある成人の認知力に対するβヒドロキシ酪酸の効果)Neurobiol Aging. 25(3):311-4. 2004年
この論文は、アルツハイマー病あるいは軽度の認知障害をもった20人の成人を対象にした臨床研究で、日を改めて、中鎖脂肪酸を摂取した場合と、プラセボを摂取した場合で、認知力を比較しています。
中鎖脂肪酸を投与すると90分後には血中のβヒドロキシ酪酸のレベルが著明に上昇し、この時点で認知機能を測定しています。その結果、ケトン体の量が多いほど、認知機能の改善が認められました。
つまり、「アルツハイマー病の患者に中鎖脂肪酸を投与すると記憶力の改善が認められ、その改善の程度はβヒドロキシ酪酸のレベルと相関する」という結論です。
米国では中鎖脂肪酸トリグリセリド(中鎖脂肪酸中性脂肪)のカプリル酸トリグリセリドがアルツハイマー病の治療に有効な医療食( medical food) として認可されています(2009年3月にFDAが認可)。
カプリル酸(caprylic acid)は炭素数8個の中鎖脂肪酸です。分子式はC8H16O2です。
神経細胞はグルコース(ブドウ糖)とケトン体しかエネルギー源として利用できないのですが、アルツハイマー病ではグルコースの取り込みや利用に障害があり、そのため中鎖脂肪酸を摂取してケトン体の産生を増やすと神経組織のエネルギー産生が改善して症状が良くなると考えられています。その他にも、前述のようなエピジェネティックな遺伝子発現調節作用の関与や、抗炎症・抗酸化・抗アポトーシスの機序による神経細胞保護作用も関与していると思われます。
Dietary ketosis enhances memory in mild cognitive impairment.(食事性ケトーシスは軽度認知障害の記憶力を増強する)Neurobiol Aging 33(2):425.e19 – 425.e27, 2012年
この論文では軽度の認知障害のある23人(男性10人、女性13人:平均年齢70.1±6.2)を対象に、高糖質食と低糖質食の2群に分けて6週間の食事療法を行っています。その結果、低糖質食のグループでは、言語記憶能力の統計的有意な改善を認め、さらに、体重、腹囲、空腹時血糖、空腹時インスリン値の統計的有意な減少が認められました。
記憶力の変化は、摂取カロリーやインスリン値や体重とは相関を認めませんでしたが、血中ケトン値は記憶力の改善と正の相関が認められました。つまり、ケトン体の濃度が高いほど、記憶力が良くなったということです。
この研究の結果は、アルツハイマー病の発症リスクの高い軽度認知障害をもつ高齢者に対して、6週間という短期間の食事(低糖質食)の介入だけで、記憶力の改善ができることを示しています。
その作用機序として、高インスリン血症の改善(アルツハイマー病を引き起こすアミロイドβを分解するのがインスリン分解酵素であるため、インスリンが増えるとアミロイドβが増えるという説)、ケトン体による抗炎症作用や神経細胞のエネルギー代謝の改善作用などが示唆されています。
ラットを使った実験でもケトン体が認知機能を高めることが報告されています。以下のような報告があります。
Diet-induced ketosis improves cognitive performance in aged rats.(食事によるケトン症は高齢ラットにおける認知機能を良くする) Adv Exp Med Biol 662: 71-75, 2010年
ラットを2群に分けて、標準的な餌とケトン食の餌で3週間飼育し、ラットの認知機能をT-迷路法や物体認識テストなどで認知機能を測定しています。ケトン食で飼育した群の方が認知機能が良かったという結果です。この実験結果は、食事によるケトン症が神経変性疾患の改善に効果があることを示しています。
現在、アルツハイマー型認知症の治療薬は「コリンエステラーゼ阻害薬」と言われる薬くらいしかありません。この薬はアルツハイマー型認知症で低下しているアセチルコリンという神経伝達物質を分解する酵素(コリンエステラーゼ)を阻害してアセチルコリンの量を増やして認知症の症状を緩和するものですが、その効果には限界があります。
その他にも多くの薬が開発中ですが、最近ではファイザーやイーライリリー社が治験を行っていた「脳内のβアミロイド」に対する抗体薬の2種類は有効性が認められないという結果で開発中止になっています。アルツハイマー病の新薬はまだ当分は出てきそうもありません。
西洋医学は「病気は薬で治すもの」と考えています。食事で治すという発想はほとんどありません。糖尿病はアルツハイマー病のリスクファクターであり、糖質制限やケトン食がアルツハイマー病の治療や予防に効果が期待できます。しかし、まだ臨床的な研究が少ないためか、ほとんど注目されていません。ケトン食が認知力を高めるという実験結果や軽度認知障害にケトン食が有効という小規模な臨床試験の結果がある程度です。しかし、若年性のアルツハイマー病など悲惨な病気に罹っている人は試してみる価値はあると思います。他の有効な方法が無いからです。
【ケトン食は様々な神経変性疾患に効果が期待できる】
ケトン食はアルツハイマー型認知症だけでなく、様々な神経変性疾患に対する有効性が示唆されています。
ケトン体自体に神経をダメージから守る作用があり、さらに抗炎症作用などによって神経変性性疾患の治療に効果を発揮する可能性があるからです。
脳卒中(脳出血や脳梗塞)、パーキンソン病、筋萎縮性側索硬化症、ハンチントン病などにも効果があることが報告されています。
神経変性疾患とは、様々な原因により脳内の様々な部位で神経細胞が病的に死滅してしまうために生じる疾患の総称です。
疾患ごとに障害を受けやすい神経細胞の種類がある程度決まっており、障害される神経細胞の働きにより疾患の症状が決まります。
アルツハイマー型認知症は記憶を担当する神経細胞(海馬など)の障害であり、筋萎縮性側索硬化症(ALS)は運動を担当する神経細胞(運動ニューロン)の障害です。
パーキンソン病は運動を調節する神経細胞のうちドパミン神経の障害で、脊髄小脳変性症は運動を調節する神経細胞のうち小脳などの障害です。
ハンチントン病(ハンチントン舞踏病)は、大脳中心部にある線条体尾状核の神経細胞が変性・脱落することにより進行性の不随意運動(舞踏様運動)、認識力低下、情動障害等の症状が現れる常染色体優性の遺伝病です。
ケトン食は元来は難治性てんかんに対する食事療法として開発され、その有効性は確立されています。
アルツハイマー病に関しては、臨床試験でその有効性が強く示唆されています。まだ動物実験のレベルですが、筋萎縮性側索硬化症やハンチントン病やパーキンソン病などの神経変性疾患の治療効果も示唆されています。筋萎縮性側索硬化症やハンチントン病はまだ有効な治療法が無い難病ですが、中鎖脂肪ケトン食を試してみる価値はありそうです。
また、認知障害を予防したり、記憶力を高めるために中鎖脂肪ケトン食を実践する有用性はあるように思います。私自身、中鎖脂肪酸を多めに使ったケトン食を実践するようになってから、このブログを書くために文献を読んだりそれらをまとめるスピードが早くなったような気がします。つまり、少しは頭が良くなったかもしれません。
ブドウ糖を絶てばがん細胞は死滅する
今あるがんが消えていく「中鎖脂肪ケトン食」
 (詳しくはこちらへ)
(詳しくはこちらへ)
| « 329) 甘い果物... | 331)がんとア... » |





