がんの予防や治療における漢方治療の存在意義を考察しています。がん治療に役立つ情報も紹介しています。
「漢方がん治療」を考える
701)糖尿病治療薬メトホルミンはレニン・アンジオテンシン系をターゲットにしてCOVID-19の重症化を予防する
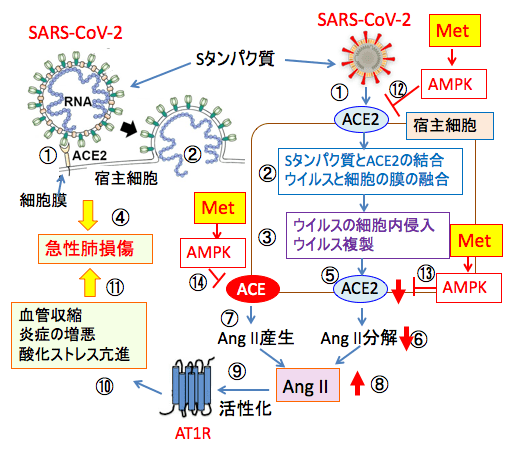
図:新型コロナウイルス(SARS-CoV-2)のスパイク(S)のタンパク質(S タンパク質)と宿主細胞の細胞膜に存在するアンジオテンシン変換酵素2(ACE2)が結合して(①)、両方の細胞膜が融合してウイルスRNAが宿主細胞に侵入し(②)、ウイルスを複製する(③)。ACE2は肺や心臓や血管に多く発現しているので、これらの組織にウイルスの感染が起こりやすい。SARS-CoV-2感染によって急性肺損傷が起こる(④)。ウイルス感染によって細胞のACE2は減少し(⑤)、アンジオテンシンIIの分解が減少する(⑥)。アンジオテンシン変換酵素(angiotensin converting enzyme:ACE)によってアンジオテンシン-II(AngII)が産生される(⑦)。その結果、AngIIの濃度が上昇し(⑧)、アンジオテンシンII受容体タイプ1(AT1R)を活性化する(⑨)。AT1Rは血管を収縮して血圧を上昇し、炎症を増悪させ、酸化ストレスを亢進して(⑩)急性肺損傷を増悪する(⑪)。糖尿病治療薬のメトホルミン(Met)はAMP活性化プロテインキナーゼ(AMPK)を活性化する機序によってACE2のリン酸化でSARS-CoV-2との結合を阻害し(⑫)、ACE2の発現低下を阻止し(⑬)、ACEの発現と活性を阻害して(⑭)、AT1Rの活性化を阻害し、急性肺損傷を軽減する。
701)糖尿病治療薬メトホルミンはレニン・アンジオテンシン系をターゲットにしてCOVID-19の重症化を予防する
【アンジオテンシンIIはがんと老化を促進する】
アンジオテンシンIIは血圧や体液量の調節に重要な働きを担っており、体の恒常性維持に必要な生理活性物質です。
しかし、がんと老化の研究領域ではアンジオテンシンIIは悪役として扱われています。
アンジオテンシンIIは血圧制御やナトリウムと水分の保持といった全身作用の他に、局所において、活性酸素の産生を増やし、炎症を増悪させ、ラパマイシン標的タンパク質(mTOR)経路を活性化する作用が知られています。その結果、哺乳動物における老化と加齢関連疾患の発生と進展を促進します。
多くの動物実験で、アンジオテンシンIIの阻害剤はがん予防と寿命延長の効果が示されています。
レニン・アンジオテンシン系を阻害する医薬品としてアンジオテンシン変換酵素(ACE)の活性を阻害するACE阻害剤(一般に'-prils'という名称がつく)とアンジオテンシンII 受容体タイプ1(AT1R)を阻害するアンジオテンシン受容体阻害剤(一般に'-sartans'という名称がつく)が数多く販売され、高血圧や心疾患の治療薬として使用されています。

図:肝臓で作られるアンジオテンシノーゲン(AGT)が(①)、腎臓から分泌されるレニンで分解されて(②)、10個のアミノ酸からなるアンジオテンシン-I(AngI)が産生され(③)、さらにアンジオテンシン変換酵素(angiotensin converting enzyme:ACE)によって(④)8個のアミノ酸からなるアンジオテンシン-II(AngII)が産生される(⑤)。AngIIは2種類の7回膜貫通型のGタンパク質共役型受容体を介して作用を発揮する(⑥)。タイプ1(AT1R)は血管を収縮して血圧を上昇し、アルドステロンの分泌を促進し、ナトリウムと水分を保持する働きがある(全身作用)(⑦)。さらにAT1Rは組織局所において、活性酸素の産生を増やして酸化ストレスを亢進し、炎症を増悪し、mTORC1活性を亢進する(⑧)。その結果、老化を促進し、がんを含めた様々な加齢関連疾患の発症と進展を促進し、寿命を短縮する方向で作用する(⑨)。ACE阻害薬(⑩)やAT1Rの働きを阻害するAT1R遮断薬(⑪)が高血圧や心臓疾患の治療に用いられており、抗がん作用や寿命延長作用が注目されている。
【AngII/Ang1-7比の増大は急性肺損傷を増悪する】
肝臓で産生されたアンジオテンシノーゲンはレニンによってアンジオテンシンIになり、さらにアンジオテンシン変換酵素(ACE)でアンジオテンシンIIに変換されます。
アンジオテンシン-IIは2種類の7回膜貫通型のGタンパク質共役型受容体を介して作用を発揮します。
タイプ1(AT1R)は血管を収縮して血圧を上昇し、アルドステロンの分泌を促進し、ナトリウムと水分を保持する働きがあります(全身作用)。さらにAT1Rは組織局所において、活性酸素の産生を増やして酸化ストレスを亢進し、炎症を増悪し、mTORC1活性を亢進します。その結果、老化を促進し、がんを含めた様々な加齢関連疾患の発症と進展を促進し、寿命を短縮する方向で作用します。
アンジオテンシンIIはアンジオテンシン変換酵素2(ACE2)によって分解され。Ang1-7を産生します。
Ang1-7のレベルの上昇は、内皮細胞に広く存在するMas受容体の活性化を介して血管拡張作用、抗炎症作用、および抗線維化作用を発揮します。
ACEは、肺、腸、腎臓、脳、大動脈、および副腎髄質で発現する膜貫通型糖タンパク質です。Ang Iから2つのアミノ酸を切断してAng IIを生成します。
ACE2は膜アンカー型カルボキシペプチダーゼで、Ang IIから単一のアミノ酸を切断して、Ang1–7を生成します。
ACE2は、II型肺胞細胞、食道上皮細胞、腸細胞、胆管細胞、心筋細胞、腎臓近位尿細管細胞、膀胱尿路上皮細胞などに広く発現しています。
新型コロナウイルス(SARS-CoV-2)感染症のCOVID-19の急性肺損傷において、アンジオテンシンII(AngII)は肺損傷を悪化させ、Ang1-7は肺損傷を抑制することが知られています。
このように、ACE/AngII/AT1R経路は古典的レニン・アンジオテンシン経路(Classical RAS arm)と呼ばれ、血圧上昇や体液保持の全身作用のほか、局所作用としては血管収縮、炎症促進、酸化ストレス亢進の作用を示します。
一方、ACE2/Ang1-7/MasR経路は保護的経路(Protective arm)と呼ばれ、血管拡張、炎症抑制、酸化ストレス軽減作用など、組織を保護する作用を発揮します。

図:新型コロナウイルス(SARS-CoV-2)感染症のCOVID-19では急性肺損傷が起こる(①)。肝臓で作られるアンジオテンシノーゲン(AGT)が、腎臓から分泌されるレニンで分解されて10個のアミノ酸からなるアンジオテンシン-I(AngI)が産生され(②)、さらにアンジオテンシン変換酵素(Angiotensin Converting Enzyme: ACE)によってアンジオテンシン-II(AngII)が産生される(③)。AngIIはアンジオテンシンII受容体タイプ1(AT1R)を活性化する(④)。AT1Rは血管を収縮して血圧を上昇し、炎症を増悪させ、酸化ストレスを亢進し(⑤)、新型コロナウイルス感染症(COVID-19)で引き起こされる急性肺損傷を増悪させる(⑥)。アンジオテンシン変換酵素2(ACE2)はアンジオテンシンIIを分解して減少させることによってCOVID-19による急性肺損傷を抑制する(⑦)。さらにACE2で産生されるAng1-7は(⑧)、内皮細胞に広く存在するMas受容体(⑨)の活性化を介して血管拡張作用、抗炎症作用、抗線維化作用を発揮し(⑩)、急性肺損傷を軽減する(⑪)。ACE/AngII/AT1R経路は古典的レニン・アンジオテンシン経路(Classical RAS arm)と呼ばれ(⑫)、ACE2/Ang1-7/MasR経路は保護的経路(Protective arm)と呼ばれている(⑬)。COVID-19の急性肺損傷は、ACE/AngII/AT1R経路を遮断し、ACE2/Ang1-7/MasR経路を活性化すると軽減できる。
人間の肺では、Ang II / Ang1–7比が高いほど、血管透過性と肺胞外液の蓄積が促進され、急性肺損傷を増悪させます。逆に、肺組織でのAng1-7のレベルの上昇は、肺を損傷から保護する作用を発揮します。
多くの動物実験で、ACE2の発現や活性を増やすと、肺の炎症が抑制されることが示されています。
ACE2活性化剤の投与は、喘息ラットモデルにおけるサイトカインストーム(IL-1β、IL-6、TNF-αなど炎症性サイトカインの過剰発現)を阻止することが報告されています。
タバコの煙に慢性的に曝露されたラットの肺は、ACE2発現の大幅な減少とACEの増加を示しました。これは、喫煙者でCOVID-19が重症化しやすい理由の一つである可能性を示唆しています。
COVID-19患者の血漿サンプルでAng IIのレベルが著しく増加していることが報告されています。Ang IIレベルがより悪い臨床転帰に関連していることを示すことも指摘されています。
SARS-CoV-2の呼吸器系に対するウイルス親和性は、アンジオテンシン変換酵素2(ACE2)への付着によって維持されます。 ACE2は、気道上皮細胞およびタイプIおよびIIの肺胞上皮細胞に高度に発現され、SARS-CoV-2が細胞に侵入するときの受容体であることが確立されています。
すなわち、SAR2-CoV-2のスパイクの糖タンパク質がACE2に結合して、両方の細胞膜が融合してウイルスRNAが宿主細胞内に入ります。(下図)

図:新型コロナウイルス(SARS-COV-2)のエンベロープの糖タンパク質(S glycoprotein)と宿主細胞の細胞膜に存在するアンジオテンシン変換酵素2(ACE2)が結合して両方の細胞膜が融合してRNAが宿主細胞に侵入して感染する。ACE2は肺や心臓や血管に多く発現しているので、これらの組織のダメージが起こりやすい。(出典 : https://ecanews.org/blog/what-role-can-crystallography-play-in-the-fight-against-covid-19/)
アンジオテンシン変換酵素(ACE)阻害剤やアンジオテンシン受容体遮断薬(拮抗薬)が、ACE2の発現を増やす作用があるという動物実験の報告があるので、これらの薬の使用がCOVID-19に対する感受性と重症度を高める可能性が指摘されました。ACE2が増えるとSARS-CoV-2ウイルスの肺への感染を促進するかもしれないという懸念です。
しかし、「ACE阻害剤やアンジオテンシン受容体遮断薬の使用がCOVID-19の感染や重症化を促進することは無い」というのが、専門家の最近のコンセンサスになっています。
むしろ、コロナウイルス感染後のACE2の発現低下が肺損傷を促進することの重要性が認識されています。
アンジオテンシンIIは肺胞上皮細胞の細胞死(アポトーシス)を誘導することが知られており、ロサルタンなどのアンジオテンシン受容体拮抗薬でこれを阻害すると、COVID-19感染の急性呼吸窮迫症候群による死亡率が低下する可能性が指摘されています。(700話参照)
塩酸やRSウイルスやインフルエンザウイルスによる肺損傷モデルの動物実験ではACE2に肺の保護作用があることが報告されています。
中国からの報告では、高血圧のCOVID-19入院患者1128人の解析で、ACE阻害剤 / アンジオテンシン受容体拮抗薬の使用は、非使用者と比較して、全死因死亡のリスクの有意な低下が認められています(調整後ハザード比=0.42、95%信頼区間;0.19-0.92、P = 0.03)。
つまり、SARS-CoV-2感染において、ACE2は「敵か味方か」という議論において、「ACE2は味方」というのが専門家のコンセンサスになっています。
肺組織において、アンジオテンシンIIの作用を阻害し、ACE2の発現と活性を亢進してAng1-7のレベルを高めることが、SARS-CoV-2による急性肺損傷を軽減することになると考えられています。(下図)

図:新型コロナウイルス(SARS-COV-2)のスパイク(S)の糖タンパク質(S タンパク質)と宿主細胞の細胞膜に存在するアンジオテンシン変換酵素2(ACE2)が結合して(①)、両方の細胞膜が融合してRNAが宿主細胞に侵入し(②)、ウイルスを複製する(③)。ACE2は肺や心臓や血管に多く発現しているので、これらの組織にウイルスの感染が起こりやすい。SARS-CoV-2感染によって急性肺損傷が起こる(④)。ウイルス感染によって細胞のACE2は減少し(⑤)、アンジオテンシンIIの分解が減少する(⑥)。アンジオテンシン変換酵素(angiotensin converting enzyme:ACE)によってアンジオテンシン-II(AngII)が産生される(⑦)。その結果、AngIIの濃度が上昇し(⑧)、アンジオテンシンII受容体タイプ1(AT1R)を活性化する(⑨)。AT1Rは血管を収縮して血圧を上昇し、炎症を増悪させ、酸化ストレスを亢進して(⑩)急性肺損傷を増悪させる(⑪)。
【急性呼吸窮迫症候群(ARDS)はびまん性の肺胞傷害で起こる】
肺は鼻と気管支を通して肺胞に空気を取り込み、空気中の酸素を体内に取り込んだり老廃物の二酸化炭素を排出する「呼吸」を行う器官です。
気管支は分岐を繰り返して無数の細気管支になり、細気管支の先端に肺胞がぶどうのように密集しています。この肺胞でガス交換が行われます。肺胞から取り込んだ酸素は間質(結合組織)にある毛細血管の中の赤血球に取り込まれて全身に酸素が運ばれます。
間質とは血管やリンパ管や神経などがある結合組織です。
肺の場合、気管支粘膜の上皮細胞や肺胞上皮細胞を支持する結合組織(線維芽細胞やコラーゲン線維や血管やリンパ管や神経などが存在する)です。(下図)

図:細気管支の先端に肺胞がぶどうのように密集しており、この肺胞でガス交換が行われる。肺胞から取り込んだ酸素は間質(結合組織)にある毛細血管の中の赤血球に取り込まれて全身に酸素が運ばれる。間質には血管やリンパ管や神経や免疫細胞や線維芽細胞やコラーゲン線維などが存在する。
肺炎(pneumonia)とは肺の炎症性疾患の総称です。気管支に細菌感染などで炎症が起こると「気管支炎」と呼ばれ、肺胞に細菌や真菌などが感染すると「肺胞性肺炎」になります。
肺の間質組織に炎症を来す疾患を「間質性肺炎(interstitial pneumonia)」あるいは「間質性肺臓炎(interstitial pneumonitis)」と言い、間質性肺炎が進行して結合組織が増えて線維化した状態を「肺線維症(pulmonary fibrosis、lung fibrosis)」と言います。
ウイルス感染によって肺胞に炎症が起こると、肺胞上皮にダメージが起こって血管の透過性が亢進し、肺胞内に浸出液が溜まり、肺水腫が起こります。
さらに経過すると、間質には線維芽細胞を主体に細胞増殖が生じ、膠原線維などの細胞外基質の沈着が起こります。
このような肺胞や間質に炎症による水腫や線維化が起こるとガス交換機能が大きく障害されるので、呼吸困難(息切れ)が起こります。
ARDSの発症から 3~4 週間以降で膠原線維の増生等によって肺胞組織の改築が進行し、肺胞腔内には膠原線維が沈着し、空気血液関門間の肥厚が顕著となり呼吸不全に進行します。
肺胞の表面を覆う上皮には2種類があります。I型肺胞上皮細胞は非常に薄く扁平な細胞で、毛細血管内皮細胞と基底板を介して接着し、血液空気関門を形成します。この部位で肺胞内の酸素と血液中の二酸化炭素とのガス交換が行われます。
II型肺胞上皮細胞は細胞表面には微絨毛が存在し、細胞質内にはリン脂質に富む分泌顆粒が存在します。肺サーファクタントの分泌を担っています。
肺サーファクタント(Pulmonary surfactant、肺表面活性物質)は、肺胞の空気が入る側へと分泌されている界面活性剤で、単一の成分ではなく、リン脂質を主成分とした混合物です。
肺サーファクタントは肺呼吸をするに当たって、肺胞を広げるのに必要なエネルギーを少なくする働きがあります。
肺胞の炎症によってII型肺胞上皮細胞がダメージを受けて肺サーファクタントが減少すると、肺胞が潰れやすくなって、呼吸困難を増悪します。
II型肺胞上皮細胞はACE2の発現が多いので、コロナウイルスも感染しやすく、ウイルスが増殖すると細胞がダメージを受けてびまん性肺胞傷害が起こると、サーファクタントが産生されなくなり、肺胞が潰れやすくなります。その結果、急速に呼吸不全を起こします。

図:正常な肺胞はI型とII型の2種類の肺胞上皮細胞で覆われ、表面にはサーファクタントが存在して肺胞が広がりやすくしている(①)。肺胞内にはマクロファージも常在する。ウイルスが感染すると免疫応答が起こり、活性化したマアクロファージ(②)やウイルスが感染した肺胞上皮細胞から炎症性サイトカイン(TNF-α, IL-6, IL-1βなど)やケモカインの産生・分泌が亢進する(③)。肺胞内は好中球やマクロファージなどの炎症細胞が増え、炎症細胞から産生される活性酸素などによって肺胞上皮細胞は傷害され、浸出液によって肺胞水腫が発生し、肺胞上皮表面には硝子膜(血漿成分が固まったもの)が形成され、びまん性肺胞傷害が起こる(④)。
重症急性呼吸器症候群コロナウイルス2(Severe acute respiratory syndrome coronavirus 2:SARS-CoV-2)感染で死亡する場合は、肺と全身で重度の炎症反応が起こって、急性肺損傷、急性呼吸窮迫症候群、敗血症、多臓器不全が起こることが主な原因と考えられています。
急性呼吸窮迫症候群(Acute Respiratory Distress Syndrome:ARDS)は、肺炎や敗血症などがきっかけとなって、重症の呼吸不全をきたす病気です。さまざまな原因によって肺の血管透過性(血液中の成分が血管を通り抜けること)が進行した結果、血液中の成分が肺胞腔内に移動して肺水腫を起こします。
COVID-19の病状悪化にはサイトカインストームが関与していると考えられています。
COVID-19で死亡した患者はフェリチンとIL-6の上昇が認められており、ウイルスによって誘発された過剰炎症による可能性を示唆しています。
体内に細菌やウイルスが侵入すると、体に備わった免疫システムが、これらの病原菌を排除するために働きます。このとき、サイトカインやケモカインというタンパク質が免疫細胞や炎症細胞から産生され、免疫細胞が活性化され、病原菌を排除します。敵が打倒されれば、免疫システムは自らオフになるように制御する仕組みがあります。
しかし、一部の人では、炎症反応や免疫応答が過剰に発現し、サイトカインが過剰に産生され、そうしたサイトカインがあやまって肺や肝臓など複数の臓器を傷害し、急性呼吸窮迫症候群(ARDS)や多臓器不全を引き起こします。
このようにサイトカインが過剰に産生される状態がサイトカイン・ストーム(cytokine storm)です。ストーム(Storm)は嵐という意味です。

図:ウイルスは肺胞上皮細胞(①)や肺胞内のマクロファージ(②)に感染し、細胞内で増殖して数を増やし放出される(③)。感染した上皮細胞からサイトカインやケモカインが産生される(④)。マクロファージはT細胞にウイルス抗原を提示し(⑤)、活性化されたT細胞(⑥)や活性化したマクロファージ(⑦)からも炎症性サイトカインやケモカインが産生される。このような炎症応答が過剰に起こりサイトカイン産生抑制の制御が不能な状態になるとサイトカインストームが起こる(⑧)。サイトカインストームは、敗血症や急性呼吸窮迫症候群(ARDS)を引き起こす(⑨)。
また、COVID-19の死因の一つとして血栓症が問題になっています。COVID-19では静脈系や動脈系ともに、血管の炎症、血小板活性化、内膜機能不全、血流停滞などによる血栓症が死因に直結する症例が多く見られることが報告されています。
脳梗塞は若い人には稀ですが、COVID-19感染患者では、若い人の脳梗塞の発症例が多く観察されているようです。肺血栓が起これば致命的になります
症状の軽い人が急変して突然死する場合は肺血栓や心筋梗塞など血栓症の可能性も指摘されています。
COVID-19は新型コロナウイルス(SARS-CoV-2)感染が誘発因子となって、全身性の過剰炎症(サイトカインストーム)と血栓形成による循環障害が起こる全身性疾患と言えます。
新型コロナウイルス(SARS-CoV-2)感染に続くウイルス増殖や急性肺損傷の段階で進行を阻止できれば、軽症で治すことができます。
しかし、びまん性肺胞傷害が重症化し、急性呼吸窮迫症候群(ARDS)や多臓器不全や凝固障害(血栓形成)が起こると、治療は極めて困難になり、死亡率が高くなります。
つまり、急性肺損傷の重症化を阻止することが、COVID-19で死なないために重要と言えます。
【糖尿病治療薬メトホルミンはCOVID-19の重症化を阻止する】
糖尿病はCOVID-19が重症化する重要なリスクの一つです。
糖尿病があるからといって必ずしもCOVID-19の感染リスクが高くなるわけではないようです。COVID-19の感染者における糖尿病患者の率は、一般住民の糖尿病罹患率と差がないというデータが報告されています。
しかし、COVID-19に感染したとき、糖尿病患者は重症化するリスクが高いという結果が報告されています。
米国疾病対策センター(CDC)のデータによると、COVID-19と診断された人のうち糖尿病患者の占める割合は10%程度で、これは米国の糖尿病有病率とほぼ同じです。
しかし、入院した患者の糖尿病罹患率は24%で、集中治療室(ICU)への入院を必要とした患者の糖尿病罹患率は30%を超えています。つまり、糖尿病患者はCOVID-19が重症化しやすいことを意味しています。
日本を含め、その他の国の研究でも、肥満や糖尿病や高血圧や心疾患の存在はCOVID-19の重症化のリスクを高めることが報告されています。
糖尿病の治療薬のメトホルミンがCOVID-19の重症化を阻止する可能性が報告されています。
メトホルミン(metformin)は、世界中で1億人以上の2型糖尿病患者に使われているビグアナイド系経口血糖降下剤です。ビグアナイド剤は、中東原産のマメ科のガレガ(Galega officinalis)から1920年代に見つかったグアニジン誘導体から開発された薬です。
ガレガは古くから糖尿病と思われる病気(口渇や多尿)の治療に経験的に使われ有効性が認められており、その関係でこのガレガから血糖降下作用のあるビグアナイドが発見されました。
メトホルミンはがんの補完・代替医療でも広く使われています。抗がん剤感受性を高めたり、がんの発生を予防したり、がん患者の生存期間を延ばす効果などが報告されています。
新型コロナウイルスの予防や治療にもメトホルミンが役立つ可能性が報告されています。
以下のようなレターの論文があります。
Metformin and COVID-19: A Novel Deal of an Old Drug(メトホルミンとCOVID-19:古い薬の新しい取引)J Med Virol. 2020 Apr 29. doi: 10.1002/jmv.25958. Online ahead of print. https://onlinelibrary.wiley.com/doi/pdf/10.1002/jmv.25958
以下はこの論文(レター)の抜粋です:
COVID-19は、重症急性呼吸器症候群コロナウイルス2(severe acute respiratory syndrome coronavirus 2 :SARS-CoV-2) により引き起こされる世界的なパンデミック感染症である。最近の報告によると肥満はCOVID-19の死亡率を増加させる原因となる可能性がある。この点に注目して、COVID-19の死亡率を下げるための新しい提案を行う。
メトホルミンは1940年代に抗マラリア薬の探索中に発見され、血糖降下作用を検討する臨床試験中にインフルエンザの治療にも有効であることが証明されている。
メトホルミンは1995年に経口血糖降下薬として米国食品医薬品局(FDA)によって承認され、世界で最も日常的に処方されている抗糖尿病薬の1つであり、さらに様々な薬効が発見され、他の疾患の治療薬としての可能性が提案されている。
近年、いくつかの研究により、多嚢胞性卵巣症候群、がん、老化、心血管疾患、メタボリックシンドローム、神経疾患の治療に有望な薬剤としてのメトホルミンの潜在的な有効性が報告されている。さらに、米国では体重減少のために適応外使用されている。
最近の研究は、自己免疫疾患の治療におけるメトホルミンの新規作用およびマクロファージのサイトカイン合成を減少させる作用を明らかにしている。
その上、メトホルミンはインスリン感受性を高めることにより、ウイルスを抑制する効果がある可能性があることが示唆されている。
米国で2002年から2012年にかけて肺炎で入院した65歳以上の高齢患者および糖尿病の既往歴のある患者を対象に実施されたコホート研究によると、メトホルミンの服用は死亡率の大幅な低下と関連していた
さらに、糖尿病と喘息のある23,920人を対象とした最近のコホート研究によると、メトホルミン治療の開始が早いほど喘息増悪のハザード比(0.92)が低く、喘息悪化に起因する救急外来診察のハザード比(0.81)および入院のハザード比(0.67)も低かった。
実質的に、高齢者は若い年齢の者よりもCOVID-19に感染しやすい傾向がある。 COVID-19の高齢患者の死亡率は、若年および中年患者の死亡率よりも高い。
体重と肺炎の軽減を通じて高齢者、肥満者、糖尿病患者のCOVID-19の死亡率を低下させるために、メトホルミンをCOVID-19の補助療法として使用できるように、FDA(米国食品医薬品局)がメトホルミンの適応疾患を変更することが求められる。
メトホルミンは糖尿病治療薬ですが、糖尿病が無くても服用できます。
インスリン感受性を高める作用のため、血糖が正常な人が服用しても低血糖を起こすことは稀です。
がん予防や抗老化や体重減少や寿命延長の目的で服用している人はかなりいます。私もがん予防と抗老化と健康寿命延長の目的で10年くらい前から服用しています。
このブログではメトホルミンの抗がん作用と抗老化作用に関する記事は216話で最初に解説しています。(2011年1月15日:「糖尿病治療薬メトホルミンの抗がん作用と抗老化作用」)
このブログ(漢方がん治療を考える)で最も多くのページがヒットする検索ワードが「メトホルミン」だと思います。がんの予防や治療や抗老化の領域においてメトホルミンは「魔法の薬」と言われるくらい多彩な作用を発揮します。
メトホルミンは、ミトコンドリアの呼吸鎖の最初のステップである呼吸酵素複合体I を阻害することが明らかになっています。その結果、ミトコンドリアでのATP産生が減少し、AMP:ATPの比が上昇し、AMP活性化プロテインキナーゼ(AMPK)が活性化されます。活性化したAMPKは、肝臓の糖新生を抑制し、解糖を亢進し、骨格筋でのグルコース利用を促進して血糖を低下させます。
すなわち、メトホルミンの血糖降下作用はミトコンドリアにおけるATP産生の阻害によって体内のATP量が減少するためです。体はATPを増やすために、グルコースの分解(異化)を促進し、糖新生(同化)を抑制するので、血糖が低下します。
最近の研究では、メトホルミンはミトコンドリアのグリセロールリン酸脱水素酵素(mitochondrial glycerol-phosphate dehydrogenase: mGDP)を阻害することも報告されています(下図)。

図:メトホルミンは有機カチオン輸送体1(organic cation transporter 1 :OCT1)によって細胞内に入り、ミトコンドリアに集積する(①)。ミトコンドリアでは呼吸酵素複合体IとmGDP(ミトコンドリア・グリセロールリン酸脱水素酵素)を阻害してNADH酸化を阻害する(②)。呼吸鎖活性の低下はミトコンドリアでのATP産生を低下し(③)、AMP活性化プロテインキナーゼ(AMP)シグナル伝達系を亢進する。(参考:BMC Biol. 2014; 12: 82.)
すなわち、メトホルミンの血糖降下作用はミトコンドリアにおけるATP産生の阻害によって体内のATP量が減少するためです。体はATPを増やすために、グルコースの分解(異化)を促進し、糖新生(同化)を抑制するので、血糖が低下します。
さらに脂肪酸の分解(β酸化)を促進します。
このような効果は運動やカロリー制限と同じです。つまり、運動やカロリー制限をせずに体重を減らせます。
肥満がCOVID-19の重症化にリスクを高めることは多くの研究で指摘されています(697話参照)。
メトホルミンは体重減量にも役立つので、COVID-19の治療に役立つという提案です。

図:AMP活性化プロテインキナーゼ(AMPK)は細胞のエネルギー代謝を調節する因子として重要な役割を担っている。AMPKは低グルコースや低酸素や虚血など細胞のATP供給が枯渇させるようなストレスに応答して活性化される(①)。AMPKは触媒作用を持つαサブユニットと、調節作用を持つβサブユットとγサブユニットから構成されるヘテロ三量体として存在する(②)。γサブユニットにはATPが結合しているが、ATPが枯渇してAMP/ATP比が上昇すると、γサブユニットに結合していたATPがAMPに置き換わる(③)。その結果、アロステリック効果(酵素の立体構造が変化すること)によってこの複合体は中等度(2~10倍程度)に活性化され、上流に位置する主要なAMPKキナーゼであるLKB1に対して親和性が高くなり、LKB1によってαサブユニットのスレオニン-172(Thr-172)がリン酸化されると、酵素活性は最大に活性化される(④)。 LKB1はセリン・スレオニンキナーゼで、AMP活性化プロテインキナーゼ(AMPK)をリン酸化して活性化する(⑤)。活性化AMPKはインスリン感受性亢進、筋肉・脂肪組織のグルコースの取込み亢進、肝臓の糖新生抑制によって血糖を低下させる(⑥)。さらに、脂肪酸合成を阻害し、脂肪酸の酸化を亢進する(⑦)。メトホルミンは、ミトコンドリアの呼吸酵素複合体Iを阻害し、ミトコンドリアでのATP産生を減少し、AMP:ATPの比を高める効果とLKB1の活性化によってAMPKを活性化する(⑧)。
【メトホルミンはレニン・アンジオテンシン系に作用して細胞保護的に働く】
COVID-19に対するメトホルミンの効果は、レニン・アンジオテンシン系に対する作用の関与が大きいようです。以下のような総説論文があります。
Metformin in COVID-19: A Possible Role Beyond Diabetes(COVID-19におけるメトホルミン:糖尿病を超えた可能な役割。)Diabetes Res Clin Pract. 2020 Apr 30 : 108183.
以下は、論文の一部の訳です。
1.メトホルミン:歴史的な再利用と多面性
メトホルミンがもともと抗インフルエンザ薬として導入されたことと、血糖降下がその副作用の1つにすぎなかったことはあまり知られていない事実である。 メトホルミンの多くの多面的効果と今日の医学におけるその広範な有用性により、科学者たちはメトホルミンを「21世紀のアスピリン」と呼んでいる。
COVID-19に対する有効な治療薬が無い現状では、既存の医薬品の転用が主要な対策となっている。新型コロナウイルスと戦う薬物の1つとしてメトホルミンを使用することを推奨する。
2.メトホルミン:分子レベルでの作用メカニズム
メトホルミンは、肝細胞におけるAMP活性化プロテインキナーゼ(AMPK)をリン酸化して活性化する。 これは、メトホルミンがグルコースと脂質の代謝に好ましい効果をもたらす主なメカニズムである。
2.1. メトホルミン-AMPK-ACE2-SARS-CoV-2
新型コロナウイルスのSARS-CoV-2は、アンジオテンシン変換酵素2(ACE2)を使用して細胞内に侵入する。SARS-CoV-2のスパイクタンパク質(S1)とACE2のN末端領域の間の相互作用を通じて人体に侵入する。
ウイルスの受容体結合ドメイン(RBD)は、ACE2受容体のプロテアーゼドメイン(PD)と結合し、RBD-PD複合体を形成する。
メトホルミンはAMPKの活性化を介して作用し、ACE2のリン酸化を引き起こす。理論的にはこのリン酸基(PO4-3)の追加がACE2受容体の構造的および機能的な変化をもたらすと考えられている。これは、大きなサイズのPO4 -3分子の追加による立体障害のため、ACE2とSARS-CoV-2 RBDとの結合の減少につながる可能性がある。
ウイルスが細胞内に入ると、ACE2受容体の発現減少が起こる。これは、レニン-アンジオテンシン-アルドステロン系(RAS)の不均衡を引き起こし、炎症と線維化を促進し、さらに致命的な心肺合併症を引き起こす。
ACE2の発現を亢進することにより、レニン・アンジオテンシン系の不均衡を回避できる。
したがって、メトホルミンは、SARS-CoV-2の侵入を防止するだけでなく、AMPKシグナリングを介してACE2の活性化を引き起こすことによって有害な影響を防止する。
(以下略)
メトホルミンはAMPK(AMP活性化プロテインキナーゼ)を活性化し、ACE2をリン酸化してSARS-CoV-2とACE2の結合を阻害し、さらにACE2を活性化して、ACE2/Ang1-7/Mas受容体の保護的経路(Protective arm)を促進して、急性肺損傷を軽減する効果が発揮するという可能性を指摘しています。
レニン・アンジオテンシン系は、ACE/AngII/AT1R経路の古典的レニン・アンジオテンシン経路(Classical RAS arm)と、ACE2/Ang1-7/MasR経路の保護的経路(Protective arm)のバランスで制御されており、ACE/AngII/AT1R経路は炎症や細胞増殖を促進し、ACE2/Ang1-7/MasR経路は炎症や細胞増殖を抑制する役割があります。
AMP活性化プロテインキナーゼ(AMPK)の活性化はレニン・アンジオテンシン系の平衡をProtective armの方にシフトする作用があります。
つまり、AMPKはレニン・アンジオテンシン系の平衡器として作用し、メトホルミンはAMPKを活性化することによってレニン・アンジオテンシン系をACE2/Ang1-7/MasR経路にシフトすることによって、炎症を抑制し、COVID-19における急性肺損傷を抑制すると考えられています。
メトホルミンはAMPKを活性化するので、ACE2/Ang1-7/MasR経路を活性化して細胞を保護する作用を発揮すると言えます。

図:レニン・アンジオテンシン系(RAS)は、ACE/AngII/AT1R経路の古典的レニン・アンジオテンシン経路(Classical RAS arm)と(②)、ACE2/Ang1-7/MasR経路の保護的経路(Protective arm)のバランスで制御されている(③)。ACE/AngII/AT1R経路は炎症や細胞増殖や線維化やインスリン抵抗性を促進する(④)。一方、ACE2/Ang1-7/MasR経路は炎症や細胞増殖や繊維化やインスリン抵抗性を抑制する(⑤)。AMP活性化プロテインキナーゼ(AMPK)の活性化はRASの平衡をProtective armの方にシフトする作用がある(⑥)(参考:AMPK: a balancer of the renin–angiotensin system. Biosci Rep. 2019 Sep 30; 39(9): BSR20181994.)
SARs-CoV-2感染は、ウイルスが細胞に侵入する際の細胞側受容体となるACE2(アンジオテンシン変換酵素2)の存在が鍵を握っています。
肺胞上皮におけるACE2の発現を低下させれば、コロナウイルスの感染を減らせると考えられます。
しかし、健康な個人では、ACE2はAng1-7の産生を通じて、肺組織を保護し、肺機能の恒常性を促進しています。
SARS-CoV-2感染は肺胞上皮のACE2の発現量を低下させ、相対的にアンジオテンシンIIの活性が強くなると、タイプ1のアンジオテンシンII受容体(AT1R)の活性亢進によって、肺損傷を増悪させることになります。
したがって、ACE2の発現を増やす作用は、ウイルスによるACE2の減少を打ち消して、肺における防御メカニズムの強化に繋がります。
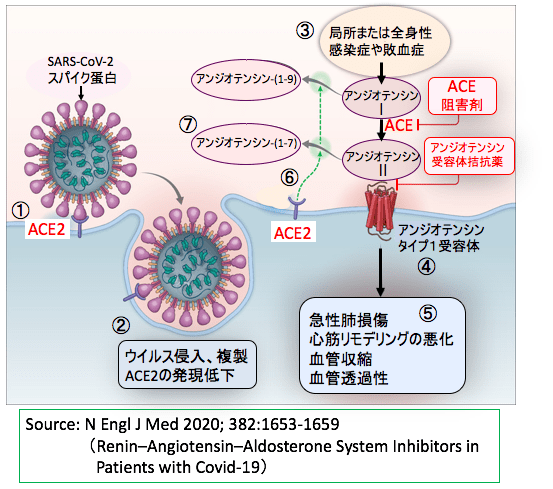
図:アンジオテンシン変換酵素2(ACE2)は新型コロナウイルス(SARS-CoV-2)のスパイクのタンパク質の受容体となり(①)、ウイルスの細胞内侵入と複製を促進し、その過程で細胞のACE2の量は減少する(②)。局所または全身性の感染症や敗血症(③)は、レニン・アンジオテンシン系を刺激してアンジオテンシンIIの産生を増やして、アンジオテンシンタイプ1受容体を活性化する(④)。アンジオテンシンタイプ1受容体の活性化は急性肺損傷を促進し、心筋リモデリングを悪化させ、血管収縮や血管透過性を亢進する(⑤)。ACE2はアンジオテンシンIIを分解して減らし、アンジオテンシン-(1-7)を増やす(⑥)。アンジオテンシン-(1-7)はMas受容体の活性化などの機序で、細胞保護的に働く(⑦)。その結果、ACE2の発現量を増やすことは急性肺損傷を軽減する効果がある。(参考 : Renin–Angiotensin–Aldosterone System Inhibitors in Patients with Covid-19 N Engl J Med 2020; 382:1653-1659)
以上から、メトホルミンはAMPKを活性化することによって、レニン・アンジオテンシン系のバランスを、保護的経路(ACE2/Ang1-7/MasR)優位にシフトさせることによってCOVID-19における急性肺損傷を抑制し、重症急性呼吸器症候群(SARS: severe acute respiratory syndrome)や呼吸不全や多臓器不全への移行を阻止する効果が期待できると言えます。(トップの図参照)
メトホルミンはがん予防効果や抗老化作用があり、またがん治療においても補助療法として有用な作用が認められています。抗がん剤治療の抗腫瘍効果増強や再発予防や生存率向上効果が報告されています。(685話参照)
がん治療中の患者さんはCOVID-19に感染すると重症化しやすいことが報告されています。
したがって、がん患者さんが、がん治療とCOVID-19重症化予防の両方の目的でメトホルミンを服用することはメリットがあると思います。
私は、がん治療においてメトホルミンを併用することを推奨し、私自身もがん予防と抗老化の目的で服用しています。しかし、薬は全て副作用が出る場合もあるので、このような目的(適応外)での使用は全て自己責任になります。
| « 700)アンジオ... | 702)ビタミンD... » |



