2009年10月にサーバリックスが承認される前に、GSKが医薬品医療機器総合機構に提出した書類には、サーバリックスのMPLが細胞性免疫作用があることが記載されていました。承認に先立つ審議会でも庵原先生と溝口先生が細胞性免疫作用について質問しており、細胞性免疫作用があることが重要なポイントになっていると考えられます。
では、GSKは実際にどのようにしてMPLに細胞性免疫作用があるのかどうかを確かめたのでしょうか。GSKのAS04に関する論文を調べたところ、MPLの細胞性免疫作用に最初に言及したのは、その4で紹介した2009年の論文でした。この論文には、MPLに関して以下のように記載されています。
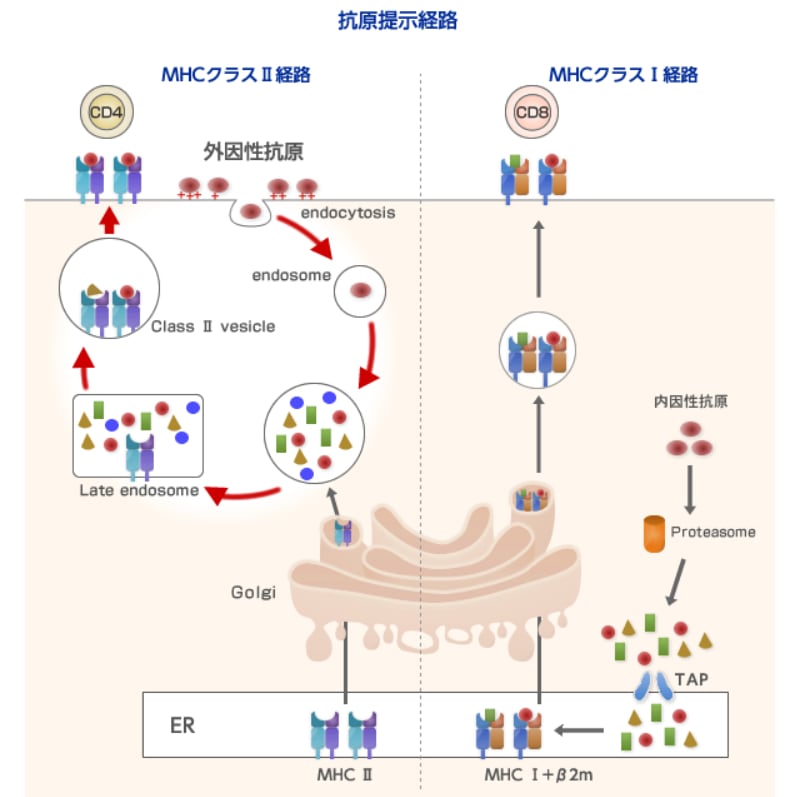
「MPLがTLR4に結合して、NF-kBを活性化して、TNFαやIL6などの炎症性サイトカインを産生し、制御性T細胞の活性を阻害しながら、抗原提示細胞を成熟させることで、獲得免疫応答を向上させる。
MPLは抗原特異的CD4+T細胞によりIFNγの生産を促進し、免疫応答をTh1プロファイルへと偏らせていると一般に報告されている。
Th1免疫応答は、細胞の中の病原体に対する効果的保護作用(攻撃作用)に必要とされる。」
MPLが細胞性免疫作用がある根拠に使用した、「MPLは抗原特異的CD4+T細胞によりIFNγの生産を促進し、免疫応答をTh1プロファイルへと偏らせていると一般に報告されている」の文にある、報告とは、以下の論文です(オープンアクセス)。
内毒素の利用:安全で効果的なワクチンアジュバントとしてのMPL
この論文の中で、MPLの細胞性免疫作用あるいはIFNγについて述べている部分を挙げてみます。
『アラムは過去70年以上使用されており、全ワクチンの80%に含まれ、既に数億回以上使用されている。
このように広範囲に使用されていることは、アラムが安全で副作用が少ないことを示している。
しかしながら、アラムは主にTh2型抗体応答を促進し、IgG4とIgEを産生する。
これらの抗体は、病原体が感染した宿主細胞を殺したり貪食するよりもむしろ、細胞の外にある病原体に対する応答に最適である。
このアラムのTh2に片寄った特異的な原理は、明らかにされつつある。
実験動物では、アラムはGr-1+白血球の一部を刺激し、大量のIL-4を産生し、アラムと抗原注射後の6時間以内に古典的Th2サイトカイン、Gr-1+好酸球が召集される。
IL-4産生好酸球の招集が、アラムの使用に関するTh2バイアスを説明するかもしれない。
アラム以外のアジュバント設計が必要とされている。
HIV/AIDS、マラリア、結核ワクチンの失敗で、Th1型免疫の必要性が広く認められている。
Th1免疫は、IgG1とIgG3イソタイプを産生することが特徴であり、病原体や病原体感染宿主細胞をオプソニン化あるいは傷害することが可能であり(中和抗体により感染を不能とするのではなく)、同時に、感染宿主細胞を直接殺傷する細胞傷害性CD8+T細胞応答を生じる。
サブユニットワクチンは、Th2応答に片寄ったアラム以外のアジュバントがないことで、その開発が限定されている。
昨今、免疫強化の研究が躍進している。
これらの進歩の一つは、TLR、NLR、CLRなどの受容体、補体などが、広範な種類の微生物成分の自然免疫の認識に関与することが判明した点である。
従って、これらの成分がアジュバントの候補として研究されている。
この様な状況の中で、TLR4を介して獲得免疫を向上させるMPLが比較的安全な成分として注目された。
AS02はMPLとQS21を含む水中油滴型エマルションであり、マラリアワクチンの実地試験で顕著な防御作用を示した。
AS02のCD8+細胞傷害性T細胞の強化は、AS04のそれよりもさらに高く、一方(MPLとQS21のリポソーム型)は、更に強力であるが、副作用のリスクがより高くなる。(つまり、AS01 > AS02 > AS04)
他の多数の研究でMPLの免疫応答について調べられており、そのうちの多くで、Th1応答あるいはTh1とTh2が混合した応答であることがわかっている。
いくつかの研究では、Th1免疫応答が、抗原のタイプや、その投与経路(皮下注射対経鼻対筋肉注射)に依存することが判明し、MPLのTh1応答を促進する能力は、強力であるが圧倒的に強力ではないことを示唆している。』
以上が、論文の中で、Th1免疫応答、CD8+T細胞について述べている部分でした。
この論文が書かれた時期のTh1とTh2の理解ですが、
Th2 IgG4 IgE IL-4 好酸球
Th1 IgG1 IgG3 細胞傷害性CD8+T細胞(CTL) IFNγ
となっています。
ところが、審議会での庵原先生と溝口先生は、
Th1 細胞性免疫作用 (細胞傷害性、CTL)
Th2 液性免疫作用 (抗体)
として述べられていると思われました。
Th1とTh2の免疫応答の分類が、アレルギーの分野と、ワクチンの分野で違っている可能性があります。この点については、後述します。
GSKがMPLの細胞性免疫作用の根拠として引用したこの論文で、MPLがTh1優位だとしていますが、その根拠が、マラリアワクチンの実施で、MPL含有AS01,AS02,AS04が有効であったからで、細胞傷害性T細胞が産生されたことを証明するデータは示されていません。
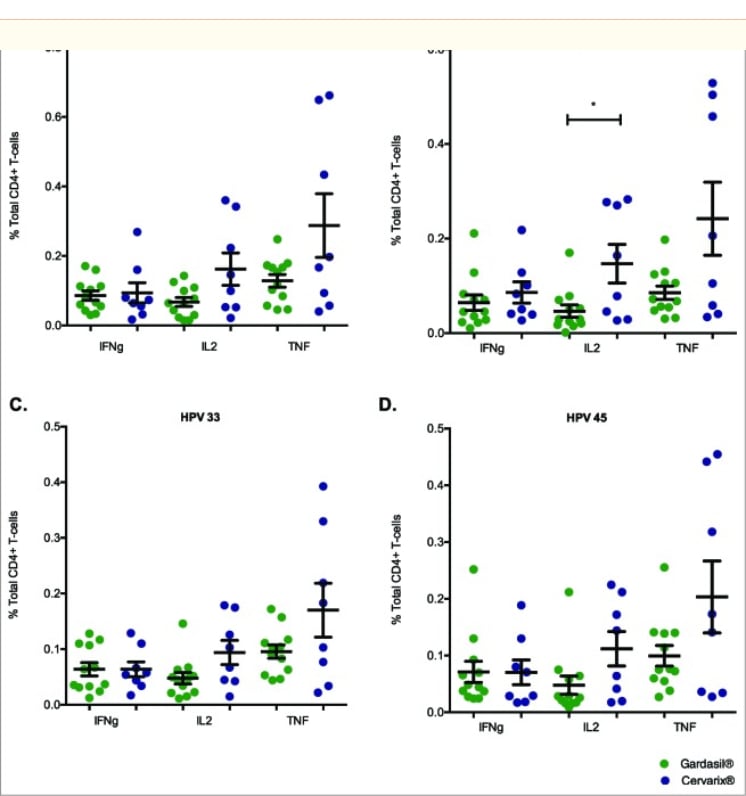
GSKの2015年のB型肝炎ワクチンの論文で細胞傷害性T細胞が検出されなかったことから、IFNγの増加のみで細胞傷害性T細胞が産生されたとする解釈は、間違っている可能性があります。
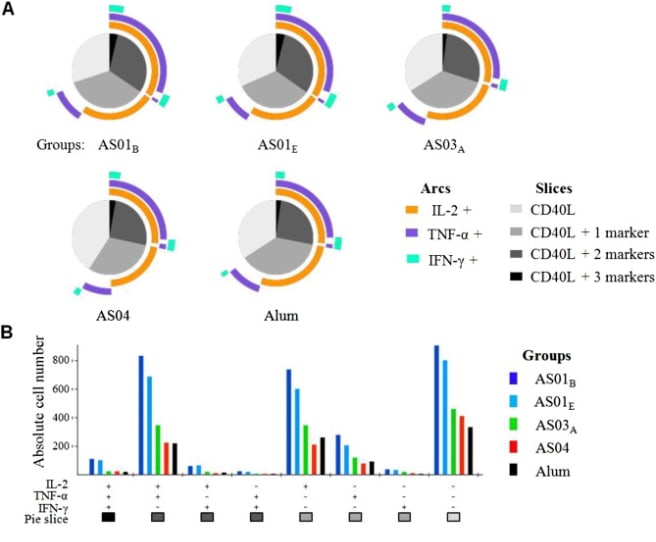
しかも、IFNγの産生は、AS04よりも、サポニンを含むAS01,AS02の方が顕著に高いことも2015年の論文でわかりました。
つまり、GSKがサーバリックスの承認時に提出した資料にある、『MPLが細胞性免疫作用を有するという』記述は、実験で得たデータで科学的に証明されたわけではなく、IFNγが増加したことによる間接的なデータからの類推であり、しかも、IFNγの増加は、AS04よりもサポニンを含むAS01、AS02での方が顕著であり、AS04とアラムでIFNγの産生量に違いがなかったことをもってすれば、MPLがIFNγを増加させるということすら、怪しくなっています。