図:ラットの脳に電極を埋め込んで、ラットが自分でレバーを押すと電気刺激が起こって電極のある部位の脳を刺激する装置を使った実験を脳内自己刺激という。電極が脳内報酬系を刺激する部位に電極があるとラットはレバーを押し続ける。特に、腹側被蓋野と側坐核を結ぶ内側前脳束に電極を埋め込むと、ラットは猛烈な勢いでレバーを押すようになる。
【脳内報酬系を刺激する薬は依存性になりやすい】
この脳内報酬系システムは、正常な快感(食事やセックスなどによる)とともに、麻薬や覚せい剤のような薬物による快感や、そのような薬物への依存の形成にも関わることが知られています。
脳内報酬系においてドーパミン放出を促進し快感を生じると、それが条件付け刺激になって依存症や中毒という状態になります。
コカインのような覚せい剤やモルヒネなどの麻薬のように依存性をもつ物質は、ドーパミン神経系(脳内報酬系)を賦活します。
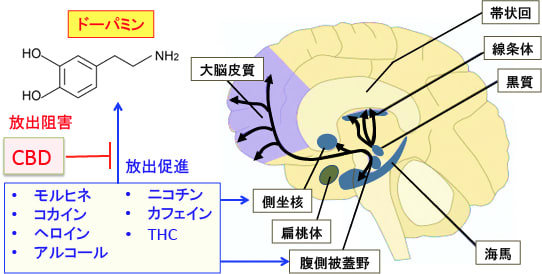
脳内報酬系を活性化するメカニズムは薬によって異なります。
GABA(γアミノ酪酸)作動性ニューロンは脳内報酬系のドーパミンの放出を抑制していますが、モルヒネはGABA作動性ニューロンからのGABAの放出を抑制してドーパミンの産生を増やします。
GABA作動性ニューロンを抑制すると中脳腹側被蓋野から出ているA10神経のドーパミン分泌が促進されて快感が増強することになります。
アルコールもGABA神経を抑制してドーパミンの放出を促進します。
ニコチンは興奮性伝達物質のグルタミン酸の腹側被蓋核への分泌を促進してドーパミンの放出を増やします。
このような依存性のある薬物は連用すると、薬剤耐性によって同じ量を摂取しても快感の度合いが次第に小さくなります。そのため、快感を得るためにさらに摂取量を増やすようになります。
さらに、その薬物が入ってこなくなると、ドーパミン神経系が低下し、不安症状やイライラ感などの不快な気分が生じます。これが禁断症状(離脱症状)です。
繰り返し摂取したい欲求を惹起する作用は強化効果や報酬効果といい、依存性薬物や嗜好性の強い食品にも認められます。
油や砂糖などの甘味はネズミの実験でも強化効果が認められています。つまり、「甘味は中毒(依存性)になる」ということは脳内報酬系の活性化という点から証明されています。ネズミの実験では、甘味の強化効果(報酬効果)はコカインより強いことが報告されています。
そこで、報酬系を抑制する薬は、薬物中毒だけでなく、飽食による肥満や生活習慣病の治療に有効という考えで、報酬系を抑制する薬も開発されています。しかし、このような薬はうつ症状や自殺企図を増やす副作用があって実用化は困難なようです。
報酬効果というのは積極的に行動したくなるモチベーションを与えるので、この報酬効果を阻害すると何もやる気が無くなります。つまり、人間が快感を得る仕組み(脳内報酬系)を抑制することは生きている意味が無いということです。
【カンナビジオールは薬物依存を抑制する】
大麻(マリファナ)が多幸感を引き起こすのは報酬系を活性化するからです。大麻に含まれるΔ9-テトラヒドロカンナビノール(THC)が作用するカンナビノイド受容体のCB1はBAGA作動性ニューロンからのGABA放出を抑制して報酬系のドーパミンの放出を増やします。モルヒネやアルコールと似た作用機序です。
THCが脳内報酬系のドーパミンの放出を増やす作用があるので、大麻は依存性を引き起こす可能性があります。
一方、精神作用のないカンナビジオール(CBD)には依存性薬物の報酬効果を減らす作用が知られています。
例えば、CBDがニコチン依存を抑制する効果が報告されています。次のような報告があります。
Cannabidiol reduces cigarette consumption in tobacco smokers: Preliminary findings. (カンナビジオールはタバコ喫煙者のタバコの消費量を減らす:予備調査の結果)Addictive Behaviors 38:2433–2436, 2013年
【要旨】
近年、ニコチン依存における内因性カンナビノイドシステムの関与が指摘されるようになった。
禁煙の意志のある喫煙者を対象に、禁煙におけるカンナビジオール摂取の効果を検討するために、予備的な無作為化二重盲検プラセボ対照試験を実施した。
24名の喫煙者を無作為に2群に分け、カンナビジオールの吸入群とプラセボ(偽薬)の吸入群に分け、喫煙したくなったら吸入をするようにという指示で1週間の検討を行った。
プラセボ群では喫煙したタバコの量に変化は無かった。一方、CBDを吸入した群では喫煙したタバコの量が40%程度の減少を認めた。このようなCBDによる禁煙効果はCBD吸入終了後のフォローアップ時にも維持された。
これらの小規模な臨床試験による予備的な研究結果は、ニコチン依存の治療にけるCBDの有用性を示唆し、さらに大規模な臨床試験を行う価値があることを示している。
被験者は全て女性で、1日10本以上の喫煙をし、禁煙したいという意志のある人です。
タバコを吸いたいと思った時にエアゾルでCBDを吸入します。プラセボ群ではタバコの数は変わらなかったのに、CBDを吸った群ではタバコの本数が40%減少したという結果でした。
CBDがモルヒネ依存を抑制するという報告もあります。
Cannabidiol inhibits the reward-facilitating effect of morphine: involvement of 5-HT1A receptors in the dorsal raphe nucleus.(カンナビジオールはモルヒネの報酬系亢進作用を阻害する:背側縫線核における5-HT1A受容体の関与)Addict Biol. 18(2): 286-96, 2013 年
【要旨】
カンナビジオールは大麻草に含まれる精神作用を持たない物質で、ネズミの実験では様々な中枢神経系に対する作用を示す。ネズミにおけるヘロイン探索行動の再発をカンナビジオールが抑制することが示されている。
しかしながら、脳刺激報酬および乱用薬物の報酬促進効果に及ぼすカンナビジオールの影響はまだ検討されていない。
そこで、本研究では、脳内自己刺激(ICSS)法を用いて、脳の報酬系機能とモルヒネやコカインによる報酬系促進効果によるカンナビジオールの作用を調べた。
ラットの内側前脳束(MFB)に刺激電極を挿入し、背側縫線核にガイドカニューレ(マイクロインジェクション装置)を挿入し、電気脳刺激に応答するように訓練した。
低用量のカンナビジオールは脳刺激の補強効果に影響を与えなかったが、高用量のカンナビジオールは内側前脳束(MFB)における脳内自己刺激(ICSS)に必要な閾値周波数を顕著に高めた。
コカインとモルヒネは脳内自己刺激の閾値を低下させた。カンナビジオールはモルヒネの報酬系亢進作用を阻害したが、コカインによる報酬系亢進作用は抑制しなかった。
選択的5-HT1A受容体アンタゴニストのWAY-100635を背側縫線核に注入する前処置を行うと、この作用(カンナビジオールによるモルヒネの報酬系亢進作用の阻害作用)は阻止された。
カンナビジオールはどの用量でも脳内自己刺激試験において強化作用を示さないが、モルヒネの報酬系促進作用を抑制する作用があることが本研究で示された。この作用は背側縫線核における5-HT1A受容体の刺激によることが示された。
これらの結果は、脳内報酬系に対するモルヒネの亢進作用をカンナビジオールが阻止する作用を有し、オピオイドの依存を軽減する目的で臨床使用できる可能性を示唆している。
前述のように、脳内自己刺激とは、ラットがレバーを押すと、脳内の特定の領域に電気が流れる実験です。電極が腹側被蓋野と側坐核を結ぶ神経線維である内側前脳束を刺激したとき、
ラットのレバー押し行動が非常に亢進されます。
この論文の実験でも、内側前脳束に電極を挿入して報酬系を自己刺激する実験系でモルヒネやカンナビジオールの効果を検討しています。
モルヒネ自身に報酬系を刺激する作用があるので、モルヒネを投与すると脳内自己刺激の閾値が低下します(ラットは少ないレバー押しで十分に満足する)。このようなモルヒネによる脳内報酬系の亢進作用をカンナビジオールが抑制し、そのメカニズムとして背側縫線核のセレトニン受容体の5-HT1A受容体をカンナビジオールが活性化するためというメカニズムを報告しています。
カンナビジオールには5-HT1Aの作動薬としての作用があり、この作用がモルヒネの報酬系抑制作用に関与しているという報告です。
【大麻は脳内報酬系への作用が弱い】
Δ9-テトラヒドロカンナビノール(THC)の精神作用(陶酔感や多幸感など)はCB1受容体を介する作用です。THC単独の製剤より大麻そのものの方が効果が高く、副作用の出現も少ないことが知られています。
その一つの理由がカンナビジオール(CBD)がCB1とTHCの結合を阻害するアンタゴニスト作用を持つことや、セロトニン受容体の5-HT1Aのアゴニストとして作用する機序などが報告されています。
モルヒネもTHCもGABAを放出している神経からのGABAの放出を抑制してドーパミンの産生を増やします。したがって、大麻もモルヒネも同様な機序で脳内報酬系のドーパミン放出を高めて、快感を得ています。
しかし、モルヒネやコカインに比べて大麻による脳内報酬系の活性化作用は弱いと言われています。その理由はまだ不明ですが、一つのメカニズムとしてカンナビジオール(CBD)がTHCによる報酬系の活性化を抑制している可能性が指摘されています。
CBDがオピオイドやコカインや覚醒剤などの依存の治療に効果があるという報告もあります。
前述のラットの実験では、モルヒネによる脳内報酬系の亢進作用をCBDが抑制し、そのメカニズムとして背側縫線核のセレトニン受容体の5-HT1A受容体をカンナビジオールが活性化するためというメカニズムが報告されています。CBDには5-HT1Aの作動薬としての作用があり、この作用がモルヒネの報酬系抑制作用に関与しているという機序です。
1994年に国立薬物乱用研究所(National Institute of Drug Abuse)のジャック・ヘニングフィールド(Jack Henningfield)博士とカリフォルニア大学のニール・ベノウィッツ(Neal Benowitz)博士がアルコール、ニコチン、コカイン、ヘロイン、カフェインの5つの物質とマリファナを比較した際、離脱症状、耐性、依存性という点においてマリファナは最も低いという結果になりました。
依存性(薬の使用を止められない状態になること)の強さは、強い方からニコチン、ヘロイン、コカイン、アルコール、カフェイン、マリファナの順番です。
離脱症状(連用している薬物を完全に断った時に禁断症状が現れることで、身体依存を意味する)もこれらの中でマリファナが最も弱く、カフェインよりも離脱症状は弱いと薬物乱用の専門家は評価しています。
つまり、大麻は酒やタバコやコーヒーより中毒になりにくいことは医学的に証明されているのです。
大麻はTHCによる脳内報酬系の活性化による多幸感が得られ、CBDなど他の成分によって依存が起こらないようブレーキをかけているような感じです。このような複数の成分による相互作用によって脳内報酬系への活性化作用が適度に制御されていることが大麻に依存性が低いことの理由の一つと言えそうです。