がんの予防や治療における漢方治療の存在意義を考察しています。がん治療に役立つ情報も紹介しています。
「漢方がん治療」を考える
707)至福をもたらすアナンダミド(Anandamide)の増やし方(その1):カンナビジオールとパルミトイルエタノールアミド
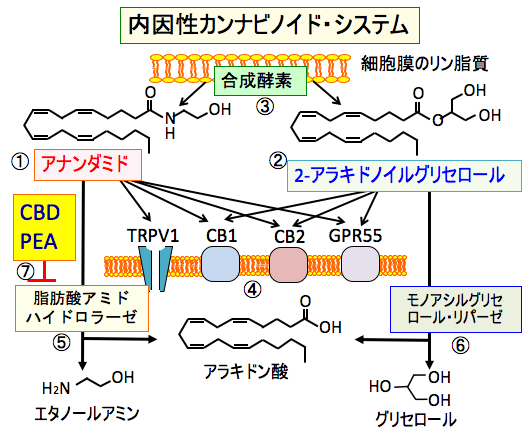
図:内因性カンナビノイドのアナンダミド(①)と2−アラキドノイルグリセロール(②)は細胞膜のリン脂質から合成される(③)。アナンダミドと2−アラキドノイルグリセロールはカンナビノイド受容体のCB1とCB2や、Gタンパク共役型受容体のGPR55やCa透過性の陽イオンチャネルの一種であるTRPV1などに作用して細胞機能を制御している(④)。アナンダミドは脂肪酸アミドハイドロラーゼ(fatty acid amide hydrolase: FAAH)によってアラキドン酸とエタノールアミンに分解され(⑤)、2-アラキドノイルグリセロールはモノアシルグリセロール・リパーゼ(monoacylglycerol lipase; MGL)によってアラキドン酸とグリセロールに分解される(⑥)。 カンナビジオール(CBD)とパルミトイルエタノールアミド(PEA)は脂肪酸アミドハイドロラーゼによるアナンダミドの分解を阻止する作用でアナンダミドを増やす(⑦)。
707)至福をもたらすアナンダミド(Anandamide)の増やし方(その1):カンナビジオールとパルミトイルエタノールアミド
【新型コロナウイルス感染症の流行でコロナ鬱が増えている?】
新型コロナウイルス感染症の流行で、精神科や心療内科は患者が増えたという情報があります。
新型コロナウィルス感染症(COVID-19)の流行によって、自分が感染してしまうのではないかという直接的な不安感や、自粛が続くことによるストレスやフラストレーションから様々な精神症状を呈する人が増え、「コロナストレス」や「コロナ鬱」や「コロナブルー」などと呼ばれる精神症状を呈する患者さんが増えていることが、ニュースなどでも話題になっています。
COVID-19の感染を阻止するために、社会的距離(ソーシャル・ディスタンス)の確保が求められ、さらに自己隔離状態が長く続くと、孤立感や孤独感を助長し、特に高齢者や一人暮らしの人に精神面での深刻な悪影響を与える可能性があります。
孤独感が不安障害やうつ病を悪化させることは容易に理解できます。
高齢者や一人暮らしでなくても、スーパーやデパートなど人が集まる場所でのマスクの着用やアルコールによる手の消毒の要請、社会的距離の確保、外食や娯楽の制限などによって多くの人がストレスを感じています。
COVID-19の流行に対しては、感染や重症化の予防対策だけでなく、精神的ストレスや不安感やうつ症状を軽減する有効な方法が求められています。
私たちは生きていく上でさまざまな欲求を持っていますが、中でも重要だとされているのが一般的に「食欲」「睡眠欲」「性欲」のことを指す「三大欲求」です。この人間の三大欲求の制御に最も関与しているのが、内因性カンナビノイド・システムです。
この内因性カンナビノイド・システムは、幸福感を高め、うつ症状や不安症状を軽減する働きもあります。
内因性カンナビノイド・システムを活性化して幸福感を高めることはコロナ鬱の軽減に有効です。
内因性カンナビノイド・システムについてまず解説します。
【内因性カンナビノイド・システムは細胞間のコミュニケーション・システムの一つ】
私たちの体は、独立した個体です。
外界からの刺激や情報を感知して、その刺激や情報に対して、脳をはじめ、体内の様々な組織や臓器や細胞が反応することによって、行動し生きていくことができます。
このように体を動かし、制御するために、体内には様々なシステムが存在します。
例えば、交感神経系や副交感神経系や内分泌系や免疫系や循環器系や泌尿器系などのシステムが存在し、これらが正常に働くことによって、私たちは健康に生きていけます。
このようなシステムを動かしたり、制御するために、様々な伝達物質が使われています。これらのシステムは多数の細胞から構成されますが、個々の細胞は独立した存在なので、細胞同士が連絡をとるために使われるのが伝達物質です。

図:細胞間のシグナル伝達の方法として、分泌された伝達物質が、分泌した細胞自身に作用するオートクリン(自己分泌)、分泌した細胞の近隣の細胞に作用するパラクリン(傍分泌)、血液によって分泌した細胞から離れた細胞に運ばれ、そこで作用するエンドクリン(内分泌)がある。
伝達物質としては、様々なホルモンであったり、細胞の増殖を制御する成長因子や増殖因子、免疫系を制御するサイトカイン、セロトニンやドーパミンのような神経伝達物質などがあります。
そのような体を制御するシステムの一つに内因性カンナビノイド・システムがあります。
つまり、内因性カンナビノイド・システムというのは細胞間のコミュニケーション・システムの一つなのです。
多くの細胞が、このコミュニケーション・システムを使って、細胞間の連絡を取り合って、組織や臓器の働きを制御しています。
このシステムの主な働きは神経組織における神経伝達の制御です。その他に、免疫細胞や消化管や肝臓や循環器系や呼吸器系などの細胞の伝達にも関与しています。

図:内因性カンナビノイド・システムは、神経伝達(①)や免疫細胞(②)の制御だけでなく、循環器系や呼吸器系や肝臓や消化管など多くの臓器の働きを調節している(③)。
内因性カンナビノイドシステムの基本は内因性カンナビノイドとその受容体から構成されます。
内因性カンナビノイドとカンナビノイド受容体の関係は鍵と鍵穴の関係と似ています。
細胞膜にあるカンナビノイド受容体(鍵穴)に、別の細胞から産生・分泌された内因性カンナビノイド(鍵)がはまり込むことによって、細胞外からのシグナルが細胞内に伝達され、細胞の働きに変化を起こします。

図:シグナル伝達物質(①)は細胞膜の受容体(②)を介して細胞外のシグナルを細胞内に伝える。細胞内では、連鎖的な化学反応(③)が起こって、遺伝子発現や細胞機能の変化が起こる(④)。
内因性カンナビノイドは細胞膜の脂質の成分であるアラキドン酸から合成されるアナンダミドと2-アラキドノイルグリセロールがあります。
これらは、神経伝達物質の分泌を制御することによって疼痛や精神活動や運動機能を制御し、さらに循環系や消化管や肝臓など多くの臓器の働きを制御しています。
カンナビノイド受容体にはCB1とCB2の2種類があります。最近はGPR55が第3のカンナビノイド受容体と考えられています。これらは7回膜貫通型の細胞膜に存在する受容体です。
CB1は脳に多く存在し、特に海馬、基底核、大脳皮質、小脳に多く発現しています。
CB1は脂肪組織、肝臓、肺、平滑筋、消化管、膵臓のβ細胞、血管内皮細胞、生殖器、免疫組織、末梢神経、交感神経などにも発現しています。
一方、CB2は、マクロファージ、好中球、単球、リンパ球(B細胞、T細胞)、ミクログリア細胞など免疫系の細胞に多く発現しています。
さらに皮膚の角化細胞や神経線維、骨芽細胞や骨細胞や破骨細胞などの骨の細胞、肝臓、膵臓のソマトスタチン産生細胞、脳のアストロサイトやミクログリア細胞、脳幹部の神経細胞などにも発現しています。
最近の研究で、神経系のCB2受容体や脳組織のグリア細胞が情動的行動にも関与することが明らかになっており、CB2受容体は不安や抑うつや記憶や知覚などの感情や脳機能にも関与していることが示されています。
したがって、CB2受容体は、免疫反応や炎症反応に対する作用だけでなく、不安やうつや痛みの制御にも関与しています。
図:内因性カンナビノイドのアナンダミドと2-アラキドノイルグリセロールはカンナビノイド受容体のCB1とCB2に作用して様々な作用を発揮する。CB1とCB2は様々な臓器や組織に分布している。
脳で最も多い内因性カンナビノイドは2-アラキドノイルグリセロール(2-AG)で、アナンダミドの200倍くらい存在します。細胞膜のリン脂質からホスホリパーゼCの作用で合成され、モノアシルグリセロール・リパーゼ(monoacylglycerol lipase)で分解されます。
神経細胞から分泌されたアナンダミドは細胞膜を通過して細胞質の脂肪酸結合タンパク質(Fatty Acid Binding Protein)と結合して小胞体に運ばれ、小胞体に存在する脂肪酸アミドハイドロラーゼで分解されます。

図:内因性カンナビノイドのアナンダミド(①)と2−アラキドノイルグリセロール(②)は細胞膜のリン脂質から合成される(③)。アナンダミドと2−アラキドノイルグリセロールはカンナビノイド受容体のCB1とCB2や、Gタンパク共役型受容体のGPR55やCa透過性の陽イオンチャネルの一種であるTRPV1などに作用して細胞機能を制御している(④)。アナンダミドは脂肪酸アミドハイドロラーゼ(fatty acid amide hydrolase: FAAH)によってアラキドン酸とエタノールアミンに分解され(⑤)、2-アラキドノイルグリセロールはモノアシルグリセロール・リパーゼ(monoacylglycerol lipase; MGL)によってアラキドン酸とグリセロールに分解される(⑥)。
アナンダミドと2-AG以外にも内因性カンナビノイドシステムに作用する脂質メディエーターが同定されています。
内因性カンナビノイド・システムは他の神経伝達物質の分泌を抑制することによって神経伝達を制御するというユニークは作用機序を持っています。抑制系の神経伝達物質のGABA(γアミノ酪酸)や興奮系の神経伝達物質のグルタミン酸のシナプス間の放出を抑制するのです。
シナプスというのは2つの神経細胞(ニューロン)の接合部で、神経細胞間のシグナル伝達を行う部分です。
通常の神経伝達物質はシナプス前ニューロンのシナプス小胞に貯蔵されて、刺激が来てシナプス間に放出されます。
神経細胞に刺激が伝わると、シナプス前ニューロンから神経伝達物質が放出され、シナプス後ニューロンにある受容体に作用して神経間のシグナルの伝達が行われます。
内因性カンナビノイドはシナプス後ニューロンから放出されて、シナプス前ニューロンに逆行性に作用して、伝達物質の放出を抑制するのです。これを逆行性シナプス伝達と言います。
内因性カンナビノイドはシナプスの刺激に応じて、シナプス後ニューロンの細胞膜のリン脂質からオンデマンドで合成されて放出されてシナプス前ニューロンに作用するのです。

図:神経を伝って刺激がシナプスに達すると、シナプス小胞が細胞膜に癒合して神経伝達物質がシナプス間隙に放出され(①)、拡散した神経伝達物質がシナプス後細胞に存在する受容体に結合することで刺激が伝達される(②)。刺激を受けたシナプス後細胞では内因性カンナビノイドのアナンダミド(AEA)や2-アラキドノイルグリセロール(2-AG)が合成されて細胞外に放出され(③)、逆行性シナプス伝達(④)としてシナプス前細胞に存在するCB1受容体に結合して(⑤)、神経伝達物質の産生・放出を抑制する(⑥)。
内因性カンナビノイド・システムは運動、学習、記憶、感情、薬物依存、食欲、エネルギー代謝、疼痛などの制御に重要な働きを担っています。さらに、循環器系や免疫系や消化器系の働きの制御も行っています。
栄養素の吸収やエネルギー産生に関わる消化管、肝臓、膵臓、脾臓、骨格筋、脂肪組織にCB1とCB2が分布しており、内因性カンナビノイド・システムが食欲やエネルギー産生のバランスの制御に働いています。
内因性カンナビノイド・システムは生体が生きていくための根幹を制御するシステムと言えます。
【大麻成分は内因性カンナビノイド・システムに作用する】
大麻が病気の治療に役立つ最大の理由は、大麻成分が内因性カンナビノイド・システムに作用するからです。
大麻に含まれるΔ9-テトラヒドロカンナビノールはカンナビノイド受容体の鍵穴に合う偽鍵のようなもので、内因性カンナビノイドと同じようにカンナビノイド受容体のCB1とCB2に結合してシグナルを伝達します。
Δ9-THCがエイズや進行がんの患者の食欲増進や体重増加の作用を発揮するのは、CB1とCB2に作用するからです。
前述のように、カンナビノイド受容体タイプ1(CB1)は中枢神経系において様々な神経伝達調節を行っており、記憶・認知、運動制御、食欲調節、報酬系の制御、鎮痛、脂肪代謝など多岐にわたる生理作用を担っています。
カンナビノイド受容体タイプ2(CB2)は免疫細胞や白血球に多く発現し、免疫機能や炎症の制御に関与しています。
CB1は中枢神経系に多く発現し、CB2は免疫細胞に多く発現していますが、カンナビノイド受容体(CB1とCB2)は多くの組織の細胞に存在し、多彩な生理機能の調節に関与しています。
脳幹部にはCB1はほとんど存在しません。これが大麻に致死的作用が無いことと関連しています。
脳幹部には呼吸中枢があり、モルヒネの受容体のオピオイド受容体は脳幹部の呼吸中枢にも多く存在するので、モルヒネ過剰で呼吸抑制が起こります。大麻には呼吸抑制が起こらないので、致死的な副作用が発生しないのです。
内因性カンナビノイド・システムが関与している疾患として、多発性硬化症、脊髄損傷、神経障害性疼痛、がん、動脈硬化、脳卒中、心筋梗塞、高血圧、緑内障、肥満、メタボリック症候群、骨粗鬆症、うつ病など多数の病気が報告されています。
つまり、これらの疾患の治療に内因性カンナビノイド・システムの制御(活性化や阻害など)が有効である可能性が示唆されているのです。
大麻の主要なカンナビノイドであるΔ9−テトラヒドロカンナビノール(THC)とカンナビジオール(CBD)が奏功する症状が以下のようにまとめられています。

THCは合成THC製剤を使った臨床試験の結果が数多く報告されているので、臨床例での有効性がかなり判っています。神経障害性疼痛や抗がん剤治療による吐き気や嘔吐、食欲低下、筋肉の硬直やけいれんにはかなりの有効性が証明されています。また、がん細胞に対する抗腫瘍効果も一部の腫瘍で示されています。
一方、カンナビジオールは動物実験レベルの研究が多いのですが、てんかんに対する有効性は臨床試験で証明されています。その他、炎症性疾患や不安や抑うつや抗がん作用も示唆されています。大麻が有効な疾患や症状として、カナダ保健省のサイトには以下のような疾患や症状が挙げられています。

【カンビジオールは抗精神病作用を発揮する】
カンナビジオールの抗精神病作用が報告されています。以下のような総説論文があります。
Cannabidiol as a Potential New Type of an Antipsychotic. A Critical Review of the Evidence.(潜在的な新しいタイプの抗精神病薬としてのカンナビジオール:エビデンスの批評的レビュー。)Front Pharmacol. 2016 Nov 8;7:422. eCollection 2016.
【論文の要約】
抗精神病薬の多くは有効性が低く、強い副作用を発現する。
したがって、現在使用されている薬とは異なるメカニズムで作用し、有効性が高く、さらに副作用の少ない抗精神病薬が求められている。
このような目的において、内因性カンナビノイド・システムは新規な抗精神病薬の開発のターゲットとして注目されている。
大麻の長期的な使用が統合失調症の発症リスクを高めるという報告は多い。しかし、統合失調症のリスク要因として大麻の関与に関しては、実際のところコンセンサスは得られていない。
大麻が精神病の発症を促進する成分としてTHCが原因と考えられている。
しかし、THCと同様にCB1に作用する内因性カンナビノイドのアナンダミドが統合失調症の症状を軽減するという報告がある。
一方、カンナビジオールは抗精神病作用が報告されており、その作用機序としてアナンダミドの血中濃度の増加が報告されている。
ネズミやアカゲザルの実験では、CBDには抗精神病作用が認められている。
統合失調症治療薬 アミスルプリド(Amisulpride)と比較した臨床試験が行われている。
ランダム化二重盲検試験で、CBDは既存の統合失調症治療薬 アミスルプリド(Amisulpride)と同程度の有効性を示し、しかも副作用はプラセボ群と同程度に極めて低かった。
CBDの効果はアンンダミドの血中レベルと相関していた。つまり、CBDの抗精神病作用はアナンダミドの血中濃度を増やすことによって発現した。
しかし、その他の作用メカニズムも報告されており、CBDの抗精神病作用のメカニズムに関しては、さらに研究が必要である。
統合失調症の症状には陽性症状と陰性症状と認知障害の3つがあります。
「陽性症状」は「本来、心の中に無いものが存在する」症状で、幻覚・幻聴・妄想・思考の混乱・異常行動などです。
「陰性症状」は「本来、心の中にあるはずのものが存在しない」症状で、感情や意欲の減退・社会的引きこもり・集中力の低下・無関心などです。
「認知障害」は記憶や注意、思考、判断などの脳の高次機能の低下です。
これらの症状に非特異的な不安症状が伴います。
症例報告やいくつかの臨床試験が実施されており、「カンビジオールは統合失調症における症状の改善に有効で、副作用も少ない」という報告があります。
最初の臨床報告はZuardiらの報告(1995年)で、4週間のCBDの投与(〜1500mg/日)で精神病症状の改善が認められました。
Zuardiらはその10年後(2006年)に3例の症例を報告しており、この研究では30日以上にわたって服用量を段階的に増やしています(最大で1280 mg/kg)。
3例中1例において、陽性症状と陰性症状の軽度の改善を認めました。副作用は全く認めませんでした。
最初のランダム化二重盲検試験は2012年に報告されています(Leweke et al.)。
42例の統合失調症患者を対象に4週間の試験で、二重盲検でカンナビジオール (600–800 mg/day) か amisulpride (600–800 mg/day)の投与を受けました。
両方の薬は、統合失調症の陽性症状と陰性症状を顕著に改善し、CBDの効果はamisulprideに匹敵しました。しかし、重要な点は、CBDの副作用はamisulprideと比べて極めて少なかったという点です。
CBDはプロラクチン産生や体重増加や錐体外路症状を引き起こしませんでした。
症状の改善はアナンダミドの血中濃度の上昇と関連しており、CBDは内因性カンナビノイドのアナンダミドの量を増やすことによって抗精神病作用を発揮すると考えられています。
【カンビジオールはアナンダミドの分解を阻害する】
カンナビノイド受容体のCB1を活性化すれば幸福感を得ることができます。大麻の場合はΔ9-テトラヒドロカンナビノール(THC)がCB1のリガンドになりますが、日本ではTHCの入った大麻製剤は大麻取締法によって所持や使用が禁止されています。
THCは大麻からしか見つかっていませんが、現時点では大麻は日本では使用できないのです。
THC以外でCB1に結合して活性化する成分が、ある種のコケで見つかっていますが、入手は困難です。
最近、内因性カンナビノイドのアナンダミドを分解する脂肪酸アミドハイドロラーゼ(fatty acid amide hydrolase: FAAH)の阻害剤が創薬のターゲットとして注目されています。
FAAHを阻害して体内のアナンダミドを増やすことによって大麻のTHCと類似に薬効を発現させようという狙いです。
THCに次いで大麻の重要なカンビノイドのカンナビジオール(CBD)がアナンダミドの分解を阻害する作用があることが報告されています。
CBDはカンナビノイド受容体のCB1とCB2には作用しないためTHCのような精神作用はありません。その他の受容体(セロトニン受容体の5-HT1Aなど)やイオンチャネル(TRPV1やTRPV2など)に作用して多彩な作用を発揮します。CB1やCB2やGPR55に対してはアンタゴニスト(阻害剤)として作用します。
その結果、THCとは全く異なる作用を発揮し、THCの副作用を軽減する作用もあります。(下図)

図:大麻の薬効成分の主体は、Δ9-テトラヒドロカンナビノール(THC)とカンナビジオール(CBD)で、この2つは全く異なる作用機序と薬効を示す。THCは脳内報酬系を活性化して依存性があり、精神作用(気分を高揚する作用)がある。一方、CBDには精神作用はなく、脳内報酬系を抑制して薬物依存を阻止する作用がある。
カンナビジオールの抗精神病作用は血中のアナンダミドの上昇と有意な関連が認められており、カンナビジオールがアナンダミドの分解酵素の脂肪酸アミドハイドロラーゼ(fatty acid amide hydrolase: FAAH)の活性を阻害することによって抗精神病作用を発揮する可能性が報告されています。
FAAHの阻害はアナンダミドだけでなく、他の脂肪酸エタノールアミド(palmitoylethanolamide や oleoylethanolamide)の分解も阻害します。
In vitroの実験では、マウスの神経芽細胞腫細胞(N18TG2)の細胞膜試料、マウスの脳のミクロゾーム、ラットの脳の細胞膜において、カンナビジオールはFAAHを阻害しました。
さらに、カンナビジオールはアナンダミドのトランスポーターを阻害し、好塩基球系の白血病細胞(RBL-2H3)によるアナンダミドの取込みを阻害しました。
FAAH-like anandamide transporter (FLAT)というアナンダミドのトランスポーターが同定されています。
FLATはFaah-1遺伝子のスプライシング変異によるタンパク質であるため、カンナビジオールはFAAHとFLATの両方のタンパク質の同じような部位に結合して、両方のタンパク質を阻害し、アナンダミドの分解と細胞内取り込みを阻害している可能性があります。
しかしながら、最近の研究では、カンナビジオールはヒトのFAAH酵素を阻害しないことが報告されています(ラットやマウスの酵素は阻害するがヒトの酵素は阻害しない)。
しかし、カンナビジオールは、アンナダミドや他のN-アセチルエタノールアミンの細胞内輸送体として作用する脂肪酸結合タンパク質(fatty acid-binding proteins)と結合することが報告されています。
Elmesらは、カンナビジオールは脂肪酸結合タンパク質の結合においてアナンダミドと競合することにおいて、人間においてアナンダミドの分解を減少させると結論づけています。
Fatty Acid-Binding Proteins (FABPs) Are Intracellular Carriers for Δ9-tetrahydrocannabinol (THC) and Cannabidiol (CBD)(脂肪酸結合タンパク質はΔ9-テトラヒドロカンナビノールとカンナビジオールの細胞内キャリアである)J Biol Chem. 2015 Apr 3;290(14):8711-21.
【要旨の抜粋】
Δ9-テトラヒドロカンナビノール(THC)およびカンナビジオール(CBD)は、マリファナ(カンナビス)に存在し、個別にまたは組み合わせて、MarinolやSativexなどの医薬品として使用されている。
これらの疎水性化合物はアルブミンまたはリポタンパク質によって血中に輸送されることが知られているが、細胞内担体は同定されていない。
最近の報告では、CBDとTHCをヒトに投与するとエンドカンナビノイドのアナンダミド(AEA)の濃度が上昇することが報告されており、植物カンナビノイドが内因性カンナビノイドのクリアランスに関与する細胞タンパク質を標的とすることが示唆されている。
脂肪酸結合タンパク質(Fatty acid-binding proteins :FABP)は、アンダミドをその分解酵素の脂肪酸アミドハンドロラーゼ(fatty acid amide hydrolase:FAAH)の局在部位に輸送する細胞内タンパク質である。
コンピュータ分析とリガンド置換アッセイにより、我々は、少なくとも3つのヒトFABP(脂肪酸結合タンパク質)がTHCとCBDに結合することを示し、THCとCBDがFABPをターゲットにすることにより、アナンダミドの細胞内取り込みと分解を阻害することを示した。
さらに、齧歯類のFAAH(脂肪酸アミドハイドロラーゼ)とは対照的に、CBDは人間のFAAHの酵素作用を阻害しないため、FAAHの阻害は、CBD摂取に続く血中アナンダミドの増加を説明できない。
FABP(脂肪酸結合タンパク質)に対するCBDの競合作用は、植物カンナビノイドの摂取後に見られるエンドカンナビノイドの血中レベルの上昇を部分的または完全に説明する可能性がある。
これらのデータは、生体内での内因性カンナビノイドの制御におけるCBDの作用メカニズムを示し、てんかんや他の神経障害に対するそのCBDの有効性とも関連する。
脂肪酸結合タンパク質がカンナビジオールによって占拠されれば、アナンダミドは小胞体に存在するFAAH(脂肪酸アミドハイドロラーゼ)に輸送されないので、分解されずに、血中のアナンダミドの濃度は上昇するというメカニズムです。(下図)

図:神経細胞間で刺激によってアナンダミドが合成され、細胞外に放出されて細胞膜のカンナビノイド受容体に結合して作用を発揮する。一方、細胞内では、アナンダミドは脂肪酸結合タンパク質(fatty acid-binding proteins:FABP)に結合して細胞内を運搬され小胞体の脂肪酸アミドハイドロラーゼ(fatty acid amide hydrolase:FAAH)で分解される。カンナビジオール(CBD)はFABPと結合して、FABPとアナンダミドの結合を阻害する作用がある。その結果、アナンダミドの濃度が高まる。アナンダミドは抗精神病作用を発揮するので、CBDはFABP働きを阻害する機序で抗精神病作用を発揮する。
【パルミトイルエタノールアミドは抗炎症作用と鎮痛作用を発揮する】
大豆レシチンや卵黄や落花生油に抗炎症作用と鎮痛作用を示す成分があることが1950年代から知られていました。その活性成分として発見されたのがパルミトイルエタノールアミド(Palmitoylethanolaide; PEA)です。
PEAは炭素数16の脂肪酸のパルミチン酸にエタノールアミンが結合した構造です。

PEAは体内でも合成され、脳や肝臓や筋肉組織など様々な組織に存在します。
PEAは古くから鎮痛作用や抗炎症作用が知られています。ヨーロッパでは1970年代から鎮痛作用のあるサプリメントとして販売されています。製品名はPeaPureなどです。
チェコスロバキアにおいて1960年代から1970年代にかけてPEAの臨床試験が多く実施され、その抗炎症作用と鎮痛作用が確認されました。
PEAはアスピリンより鎮痛作用が強いことが報告されています。1975年にランセットにPEAの鎮痛作用が報告されています。
初期の研究結果はPEAが感染症に対する抵抗力を高めること、抗炎症作用を示すことを明らかにしています。
例えば、マウスにPEAを経口で投与すると赤痢菌毒素やストレプトリシンO(溶血性連鎖球菌の外毒素)や生きたグループAストレプトコッカスの投与による死亡率を低下しました。
事前にPEAを投与して準備しておくと、外傷性ショックによる死亡を減らすことも報告されています。
PEAが抗がん剤治療の副作用を軽減することや、白血病の動物実験で、抗がん剤治療(シスプラチン、シクロフォスファミド、ビンクリスチン、メソトレキセート)とPEAの併用で生存率が高まることが報告されています。
PEAが神経障害性疼痛や抗がん剤による神経障害を軽減する効果も報告されています。
このような確実な効果が臨床的に確認されていましたが、その作用メカニズムは長く不明でした。PEAの作用メカニズムの研究が進んだのは、1993年にリータ・レーヴィ=モンタルチーニ(Rita Levi-Montalcini)の研究グループが、N-アセチルエタノールアミン型(N- acylethanolamine type)の脂質アミドが肥満細胞の活性を調整する作用があることを偶然に発見したからです。
レーヴィ=モンタルチーニ博士は神経成長因子と上皮成長因子の発見の功績で1986年にノーベル賞(生理学・医学賞)を受賞したイタリアの神経学者です。
肥満細胞に対する神経成長因子の作用がPEAによって影響を受けることを報告しています。これが、PEAの抗炎症作用の最初のメカニズムの報告です。
その後もPEAがPPARα(ペルオキシソーム増殖因子活性化受容体α)のリガンドであることや、内因性カンナビノイドシステムに影響する作用などが報告されています。
1992年から2000年にかけて内因性カンナビノイドのアナンダミドやカンナビノイド受容体CB1とCB2や核内受容体のPPARなどが発見され、それによってPEAがこれらの体内システムに作用することが明らかになってきました。

図:肥満細胞はヒスタミンなどの炎症性メディエーターが詰まった顆粒を持っている(①)。肥満細胞が活性化され、「脱顆粒」によって顆粒内部の炎症性メディエーターが遊離すると(②)、炎症反応やアレルギー反応が引き起こされる(③)。脂肪酸エタノールアミドのパルミトイルエタノールアミドは肥満細胞のPPARα(ペルオキシソーム増殖因子活性化受容体α)に作用して脱顆粒を抑制して、抗炎症作用を示す(④)。さらに、アナンダミドの代謝などにも影響して内因性カンナビノイドシステムの活性を亢進することも報告されている(⑤)。内因性カンナビノイドも肥満細胞のCB2受容体に作用して脱顆粒を抑制することによって脱顆粒を阻害する(⑥)。これらの作用によってパルミトイルエタノールアミドは炎症や疼痛を軽減する効果を発揮する。
【パルミトイルエタノールアミド(PEA)は内因性カンナビノイド】
アナンダミドはアラキドン酸とエタノールアミンが結合した脂肪酸エタノールアミドの一種です。
脂肪酸エタノールアミドは,脂肪酸とエタノールアミンが縮合して生成する化合物で、神経伝達物質として生理学的に重要な機能を有するものがあり、その代表がアラキドン酸にエタノールアミンが結合したアナンダミドと言えます。

図:アナンダミド(アラキドノイル・エタノールアミド)はアラキドン酸とエタノールアミンが結合した化合物
アナンダミドはカンナビノイド受容体CB1とCB2のほかGPR55やTRPV1などにも作用します。
アラキドン酸は4つの2重結合を含む炭素数20の脂肪酸で、ω6系多価不飽和脂肪酸です。細胞膜中のリン脂質として存在し、ホスホリパーゼA2によってリン脂質から遊離し、プロスタグランジンやトロンボキサンやロイコトリエンなどの化学伝達物質が作られます。
アナンダミドも細胞間のシグナル伝達のセカンドメッセンジャーとして、刺激に応じて産生され、内因性カンナビノイドシステムで働いています。
アナンダミドは最初に発見された内因性カンナビノイドで、化学合成したものがCB1とCB2に親和性を示すことで内因性カンアビノイドであることが証明されました。
アナンダミドと同じような脂肪酸エタノールアミドは哺乳動物で多く見つかっています。
前述のパルミトイルエタノールアミドは、炭素数16の脂肪酸のパルミチン酸にエタノールアミンが結合した構造で、古くから鎮痛作用や抗炎症作用が知られています。
パルミトイルエタノールアミドはCB1とCB2には親和性を有しませんが、CPR55に作用することや、アナンダミドの働きに影響することから、内因性カンナビノイドの一種という意見もあります。
PEAの鎮痛効果は、糖尿病性神経障害や抗がん剤による神経障害、手術後疼痛、座骨神経痛、多発性硬化症など様々な原因で起こる神経障害性疼痛の軽減に有効性が臨床試験で確認されています。
他の治療薬で改善しない疼痛に対して効果があることが報告されています。
副作用はほとんど無く、他の鎮痛薬との併用も問題なく、通常の鎮痛薬と併用することによってその鎮痛効果を高めます。他の薬との相互作用も問題ありません。 PPARαと内因性カンナビノイドシステムに作用し、抗炎症作用を有するので、神経難病やがん治療にも役立ちます。
PEAがPPARα(ペルオキシソーム増殖因子活性化受容体α)のリガンドであることや、内因性カンナビノイドシステムに影響する作用などが報告されています。
生体内でPEAが内因性カンナビノイドのアントラージュ効果に関わっていることが報告されています。以下のような報告があります。
The anti-inflammatory mediator palmitoylethanolamide enhances the levels of 2-arachidonoyl-glycerol and potentiates its actions at TRPV1 cation channels.(抗炎症メディエーターであるパルミトイルエタノールアミドは2-アラキドノイルグリセロールのレベルを高め、陽イオンチャネルTRPV1に対する作用を増強する)Br J Pharmacol. 2016 Apr;173(7):1154-62.
【要旨】
研究の背景と目的:パルミトイルエタノールアミド(PEA)はアンンダミドと同類の内因性物質で、カンナビノイド受容体のCB1とCB2や陽イオンチャネルのTRPV1(transient receptor potential vanilloid type-1)に対するアナンダミドの作用を増強する。
もう一つの内因性カンナビノイドである2-アラキドノイルグリセロール(2-AG)が、最近の研究でTRPV1のアゴニストとして作用することが示唆されている。そこで、2-AGの量やTRPV1に対する2-AGの作用に対するPEAの効果を検討した。
実験方法:内因性の脂質の量は液体クロマトグラフ質量分析計(LC-MS)で測定した。測定材料は(i)PEA(10-20 μM, 40 min, 6 and 24 h, 37°C)の存在下で培養したヒトのケラチノサイト(角化細胞)、(ii)豚回虫(Ascaris suu)に過敏性をもつビーグル犬に超ミクロ化PEA(30mg/kg)を1回経口投与した後、1、2、4、8時間経過後の血液サンプル、(iii)健常ボランティアにミクロ化PEA(300mg)を投与後2、4、6時間後の血液サンプル。
TRPV1チャネルに対する2AGの作用は、ヒトTRPV1チャネルを過剰発現させたHEK-239細胞を用いて、細胞内Ca2+濃度を測定することによって行った。
主な結果:ケラチノサイトにおいてPEA処理によって2-AGのレベルは約3倍程度に上昇した。健常人への投与では2-AGの血中濃度は2倍程度、犬の実験系では20倍程度の上昇を認めた。
TRPV1を過剰発現したHEK-239細胞を用いた実験では、2-AGはTRPV1に依存する作用機序で、用量依存的に細胞内Ca2+の濃度を高め、カプサイシンに対する細胞の反応を減弱した。
2-AGによるTRPV1の活性化に対してはPEAはわずかに増強したが、2-AGによるカプサイシンに対するTRPV1脱感作(2-AG-induced TRPV1 desensitization to capsaicin)は顕著に亢進した。(IC50 from 0.75 ± 0.04 to 0.45 ± 0.02 μM, with PEA 2 μM).
結論;これらの結果は、PEAの様々な作用が、カンナビノイド受容体やTRPV1のアンタゴニスト(阻害剤)によってなぜ阻止されるのかという理由を説明できるかもしれない。
TRPV1は唐辛子に含まれるカプサイシンが結合する受容体として最初に発見されたイオンチャネルです。
TRPチャネルは、種々の生理活性物質により活性化され、環境変化を感知する“センサー”タンパク質として働きます。また、セカンドメッセンジャーであるCa2+を流入させ、様々な生化学的反応を細胞中に引き起こし、細胞の適応応答を生じるシグナルトランスデューサーとしても働きます。
このTRPV1には内因性カンナビノイドやPEAなどが作用することが明らかになっています。
PEAはカンナビノイド受容体CB1とCB2に対する結合活性は持っていません。しかし、内因性カンナビノイドのアナンダミドや2-アラキドノイルグリセロールの作用を増強する作用が最近の研究で明らかになっています。
つまり、PEA(パルミトイルエタノールアミド)は、内因性カンナビノイドシステムのアントラージュ効果の重要な体内の脂質メディエーターとして作用していることが最近の研究で明らかになっています。
「アントラージュ(Entourage)」というのは「取り巻き」や「側近」という意味です。
アントラージュ効果という用語は、内因性カンナビノイド・システムの研究において、メコーラム博士の研究グループが1998年に発表した論文で最初に使われています。(Eur J Pharmacol. 353(1):23-31.1998年)
この論文では、内因性カンナビノイドの一種の2-アラキドノイルグリセロール(2-AG)の活性を他の脂肪酸グリセロールエステルが亢進する作用を報告しています。
2-AGはカンナビノイド受容体のCB1とCB2のリガンドとして作用します。2-リノレオイル・グリセロール(2-linoleoyl-glycerol)と2-パルミトイル・グリセロール(2-palmitoyl-glycerol)は、それ自体ではCB1とCB2にはリガンドとしての活性はありませんが、2-AGのCB1とCB2を介する作用(鎮痛作用など)を増強する実験結果を報告しています。
その作用機序として、これらの脂肪酸グリセロールエステルが、内因性カンナビノイドの分解を阻止する作用などを指摘しています。
このように、カンナビノイド受容体(CB1とCB2)に直接作用しない物質が、内因性カンナビノイドの合成や分解や取込みなどに影響して、内因性カンナビノイドシステムの働きに影響する効果を「アントラ−ジュ効果(取り巻き効果)」と呼び、内因性カンナビノイドシステムの制御に重要だと考えられています。
PEA自体は1970年代からヨーロッパで鎮痛剤として使用され、現在ではサプリメントとして販売されています。副作用が極めて少なく、PPARαや内因性カンナビノイドシステムに作用するという点で、利用価値の高いサプリメントと言えます。
THCあるいはTHCの入った大麻製剤は日本では使用できません。しかし、カンナビジオールとパルミトイルエタノールアミドはサプリメントレベルの取り扱いで、CB1を間接的に活性化する目的で利用できると思います。
カンナビジオールとパルミトイルエタノールアミドの併用使用は、内因性カンナビノイド(アナンダミドや2-アラキドノイルエタノールアミド)の血中濃度を高め、抗不安や抗うつ作用や食欲増進などの効果を発揮すると考えられます。
実際、私自身がこの2つを併用してしばらく服用してみましたが、やる気が出てくるような感じはします。
| « 706)カンナビ... | 708)至福をも... » |



