文献レビュー
敗血症の診断と治療 2019
名古屋大学大学院医学系研究科
救急・集中治療医学分野
松田直之
2019年までの敗血症診療の方向性を2017年レベルの文献を中心としてまとめています。ご参照下さい。
医療従事者でない皆さまは,敗血症の基本的知識の拡充のために敗血症YouTubeと合わせて御覧ください。
敗血症の定義と診断に関する進展
敗血症は,感染症による臓器不全の進展である。感染症と区分する目的は,がん,脳卒中,急性心筋梗塞,重症糖尿病,急性肺炎,高齢などのもととなる状態に感染症がやってきたときに,元の病気と生じてくる臓器不全を分けて診療する提案をするためのクリニカルターム(clinical term:診療管理用語)である。
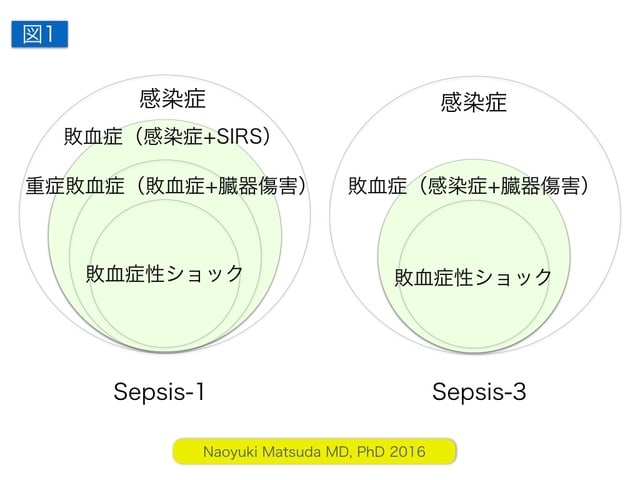
Sepsis-31)の定義が,2016年に世界の敗血症の中心人物たちにより公表され,全身性炎症反応(systemic inflammatory response syndrome:SIRS)2)の基準を敗血症診断に用いない方針となったが,これは正しいとか間違っているを超えた世界的な保健政策である4-8)。全身性炎症という概念と病態は,依然として学術として追求される領域であることは正しい。Sepsis-3では,「敗血症は感染によって引き起こされる生命を脅かす臓器機能不全」と定義されたが,SIRSは敗血症を進行させる病態概念して重要であり,再評価が必要とされている。Fang等8)は,21,491例の感染症患者のデータベースより,Sepsis-1に合致する敗血症でSepsis-3に合致しないものの21日死亡率は約6.96%と報告している。すなわち,Sepsis-3では早期診断よりもむしろ臓器障害としての死亡予測に重点が置かれているため,敗血症の発見が遅れて死亡する可能性が指摘されている。2015年に公表されたANZICSのデータでは集中治療室(intensive care unit,ICU)における臓器不全を伴う敗血症においてSIRS基準を満たさない患者は約1/8,SIRSによる敗血症の診断感度は約88%だったが9),Sepsis-3により臓器不全の進行として敗血症を診断することで,敗血症の早期診断と早期治療を遅らせる可能性がある。このように,SIRSは敗血症の一般的な特徴であり,早期診断のプロセスとしては重要という考えが残存している4-8)。
このように,Sepsis-31)の発表後のSepsis-3に対する問題を提起する論文が,投稿されたのが2017年からである。救急外来における成人の敗血症性ショックとして対応したAustralasian Resuscitation in Sepsis Evaluation (ARISE) trial10)のポストホック解析では,SIRS基準を満たし,血液分布異常性ショックとして乳酸値上昇を認めた1,591例において,qSOFAを満たしたのは1,139例(約71.6%),また,qSOFAおよびSepsis-3の敗血症診断に合致したのは1,010例(約63.4%),さらにSepsis-3の敗血症性ショックの診断に合致したのは203例(約12.8%)という結果である。ここでは,SOFAスコアや乳酸値≧2mmol/Lを用いるSepsis-3では,敗血症性ショックの早期診断を損ねている可能性が指摘された。
また,成人の敗血症を対象とした過去の2つの臨床研究11)の解析としてSepsis-12)による敗血症性ショックの470例が評価され,このうち約57%がSepsis-3の敗血症性ショックの基準を満たしていないと報告された。このデータにおいても,Sepsis-31)の診断基準では臓器不全および死亡率の増加した敗血症性ショックが同定され,Sepsis-3を満たさずにSepsis-1の基準のみを満たした例でも約10%を超える死亡率を認めている。このようなSepsis-3を用いた診断に関する報告が,2020年までに一定数の集積が見込まれ,この解析を本邦でも行う必要がある。
一方,電子記録システム(Millennium:Cerner Corporation,Kansas City,Missouri),クラウドベースの敗血症サーベイランス,CDS(St. John Sepsis Surveillance Agent:Cerner Corporation、Kansas City,Missouri)を用いた8施設の共同解析12)では,Sepsis-3の早期診断に用いqSOFAスコアと,聖ヨハネ敗血症サーベイランスエージェント(SIRSアラート:体温>38.3℃または<36℃,心拍数>90回/分,呼吸数>20回/分,白血球数>12,000/ mm3または<4000/mm3または幼若球>10%,血糖値140~200mg/dLのうち3つ以上を満たす)が比較された。17,044例の入院患者のうち5,992例(35%)が感染疑いとして評価されたが,感染症発症,ICU内死亡,院内死亡のすべての予測において,聖ヨハネ敗血症サーベイランスエージェントがqSOFAに勝る結果だった。感染症の臓器不全への移行における初期評価として,白血球数や血糖値などの血液・生化学検査や心拍数変動などの理学所見は,qSOFA以上に院内における早期診断として有用である可能性が指摘された。qSOFAは,検査ができない状態での敗血症の簡易スクリーニングとしての役割に限定される可能性がある。
さらに,SOFAスコアを用いたSepsis-31)による最終診断が臓器不全の進行する重篤な患者群を検出できることがSepsis-3公表後に検証されたが13-17),臓器障害の臨床情報や予後改善においてはSepsis-218)の24の評価項目の有用性が指摘されてきた19, 20)。これらの評価からは,院外ではなく,院内の敗血症管理においては,SIRSの概念と定義の再構築や新たなバイオマーカーを含めて,敗血症の早期診断と早期治療の達成をターゲットとする課題が提起されている。日本版敗血症診療ガイドライン20163)の4年後の改訂予定では,これらのエビデンスを統合的に評価することとなる。
敗血症および敗血症性ショックにおける疫学と生命予後
敗血症の疫学においては,これまで1991年から2009年までの評価可能な36の臨床研究データとして,28日死亡率の年次推移がStevenson等21)の論文にまとめられている。1991年から1995年における平均死亡率約46.9%から,2006年から2009年の平均死亡率約29%まで,年間約3%ずつの敗血症による死亡率低下として評価されている。これに対して2017年には,韓国からは韓国ショック学会の2015年10月から2016年6月までの19歳以上を対象とした敗血症性ショックのレジストリ22)のAcute Physiology and Chronic Health EvaluationⅡ(APACHEⅡ)スコア平均18.5の468例の結果として,院内死亡率22.9%, 28日死亡率21.8%,90日死亡率27.1%が報告されている。また,台湾からの報告23)では,2002年から2012年までの11年間で診療データベースよりSepsis-3に合致する1,259,578例が抽出され,2002年の638例/10万例より2012年では772例/10万例に敗血症罹患率は年あたり約1.9%に増加しているが,敗血症の院内死亡率は年間あたり0.45%の割合で27.8%から22.8%に減少していることが報告されている。
敗血症の予後に関する報告は,2017年においても多くの論文が検出できる。Leisman等24)の敗血症3,686例を解析した報告では,心不全 (オッズ比1.43; 信頼区間1.20-1.72),低体温(オッズ比1.37; 信頼区間1.10-1.69),低酸素血症(オッズ比1.33; 信頼区間1.12-1.57), 乳酸値≧4.0 mmol/L(オッズ比 1.28; 信頼区間1.08-1.52), 免疫不全(オッズ比1.23; 信頼区間1.03-1.47),および凝固障害(オッズ比1.23; 信頼区間1.03-1.48)が危険因子として挙げられている。 2011年1月から2015年6月までの6施設の後方視的解析25)では,Surviving Sepsis Campaign guideline 201226)における3時間以内の達成を目標とした3時間管理バンドルの4内容が評価され,1)抗菌薬投与前の1時間以内の血液培養検査が50分,2)乳酸値評価が20分,3)広域抗菌薬投与が125分,4)平均血圧低下(≦ 65 mmHg)と乳酸値上昇(≧ 4 mmol/L)に対する30mL/kgの晶質液投与が100分を閾値として,死亡率が上昇するとした。この研究における院内死亡は1,412例(27.8%)であり,3時間より早く対応する必要性が言及されている。この3時間バンドルに含まれる乳酸値については,Oh等27)は18歳以上の1,043例の敗血症患者の解析として,乳酸値が2mmol/L以下の369例(35.4%)に対して,28日死亡率にAPACHEⅡスコア,C反応性蛋白,慢性心不全の既往が関係するとしている。また,Driessen等28)は敗血症性ショックのICU死亡率増加の閾値として血清乳酸値は6mmol/Lを報告しており,一方で日本救急医学会のSepsis Registry Study Group29)は敗血症の院内死亡率増加は血清乳酸値4mmoL/Lを閾値とすると報告している。日本救急医学会のSepsis Registry Study Group30)は,さらに敗血症の生命予後の危険因子として低体温を指摘している。
敗血症のバイオマーカーへの注目
バイオマーカー(Biomarker:生物指標化合物)とは,疾患の存在や進行度を反映する血液中分子である。敗血症の病態生理学的特徴からは,微生物の含有作動分子(リガンド)や,白血球系細胞や上皮系細胞と反応して新たに産生された分子群がバイオマーカーとして期待できる。Sepsis-218)における診断補助として挙げられたもの以外のバイオマーカーとして2017年には,pentraxin-3(PTX3),cytosolic heat-shock protein 90 kDa alpha class B member 1 (HSP90AB1),soluble triggering receptor expressed on myeloid cells-1s(TREM-1),CD64(Fcγ受容体1A), suPAR(可溶性ウロキナーゼ受容体),老化阻止分子α-Klotho,インスリン抵抗性分子Fetuin-Aなどが認められる。
PTX3は,リポ多糖体(リポポリサッカライド:LPS)に反応して特に血管内皮細胞と血管平滑筋細胞から多く産生されるため,interleukin-6(IL-6)などの刺激により肝臓で産生されるCRPと比べれば鋭敏に,敗血症における血管局所の炎症を反映すると考えられる。敗血症におけるアルブミンの有効性を評価したALBIOS研究31)では,958例で切断率の低いlong PTX3を計測しており,PTX3の第1病日値は72(33-186)ng/mLであり,臓器障害の重症度と相関していた。PTX3濃度は,敗血症の第1病日から第7病日で低下したが,敗血症性ショックをでは減少率が有意に低下していた。PTX3を,敗血症罹患のリスク因子としての新たなバイオマーカーとして推奨する論文32, 33)は増加傾向がある。
また,敗血症性ショックにおける小児の血液を用いたprotein-protein interaction network解析34)では,lysine (K)-specific demethylase 6B(KDM6B), histone deacetylase 2(HDAC2), V-Myc avian myelocytomatosis viral oncogene homolog (MYC),HSP90AB1,poly (A)-binding protein cytoplasmic 1 (PABPC1)が,正常小児と強い差を検出できるトップ5として検出されている。これらは,2018年までに炎症病態で上昇することが確認されており,転写因子nuclear factor-κBなどで制御される分子群である。HSP90AB1に関する文献が一定数で存在する。2017年までのデータを振り返る限り,TREM-1については敗血症における感度はCRPやIL-6と同等かもしれない。
敗血症における抗菌薬の有効利用
敗血症は,微生物の持つ炎症性分子とToll-like受容体などの反応による炎症病態を基盤とする。敗血症治療の長期化,免疫膠原病などの慢性炎症病態,がん病態,免疫不全などでは,抗炎症性サイトカインや増殖性サイトカインが複雑に病態を修飾する。病態生理学的には,微生物リガンドを低下させるようにできるだけ早期に抗菌薬を投与することが期待される。また,ドレナージが可能であれば,ドレナージのタイミングを逸しないことが期待される。
敗血症性ショックにおける抗菌薬の投与においては,メチシリン耐性ブドウ球菌における投与としてバンコマイシンを選択する場合には初期投与量を通常より減少させないこと35),Acinetobacter baumanniiやPseudomonas aeruginosaなどを対象としたメロペネムの使用においてもaugmented renal clearanceを考慮して開始初期の投与量を減少させないこと36)が,2017においても薬物動態(pharmacokinetics:PK)と薬力学(pharmacodynamics:PD)の観点より報告されている。Sherwin等37)は,1,552文献の中から14の文献のレビューとして,抗菌薬投与開始までの時間を1時間以内として推奨している。
以上のような抗菌薬の適正管理として,本邦でも薬剤師の関与が期待されている。敗血症76例のコフォート研究38)では,薬剤師の介入により抗菌薬適正使用の割合が約66%から80%に有意に増加した。最初の抗菌剤投与までの中央値が43分であり,適切な抗菌治療までの時間はコホート全体で1時間34分であるとしている。敗血症管理における薬剤師評価は,一般病棟管理における薬剤師レスポンダーとして強く期待される。
敗血症性ショックにおける血圧管理と血管作動薬
敗血症性ショックにおける血圧管理の目標について,これまで2つの大規模臨床研究39, 40)に準じて,平均血圧65mmHgを超える高い血圧を期待する必要はないとする報告が散見される。これらを含めて,2017年11月までの成人敗血症性ショックのデータ解析41)として,MEDLINE,EMBASE,Controlled TrialsのCochrane Central Registerより解析可能な894例が抽出され,高い血圧管理(約75–80 mmHg)は低い血圧管理(約60–65 mmHg)と比較して28日死亡が高まる傾向をが示され(オッズ比1.15,95%信頼区間 0.87-1.52),平均血圧65mmHgレベルを推奨することが確認されている。この解析41)では,昇圧薬を用いて6時間を超えて平均血圧が高い群では有意に死亡リスクが高まるという結果も示されている(オッズ比3.00,95%信頼区間1.33-6.74)。現時点においても,平均血圧65mmHgを目指す血圧管理が推奨され,適時,血管作動薬を適切に減量していくことが必要である。
昇圧に関する2019年までのトピックスとしては,既に1990年代までに循環薬理領域で討議されたアンジオテンシンⅡアナログの再燃である。Angiotensin II for the Treatment of High-Output Shock(ATHOS-3)42)は,ノルアドレナリン0.2μg/kg/分以上や同等に血管作動薬を投与されている血液分布異常性ショックをランダム化し,主要評価項目をアンジオテンシンⅡアナログ投与開始3時間後における10 mmHgの血圧上昇や平均血圧75mmHgの維持とした。本研究は,合成ヒトアンジオテンシンⅡ(LJPC-501)の市販に向けた研究でもある。ATHOS-3の結果は,アンジオテンシンII群161例とプラセボ群158例の解析として,アンジオテンシンII群(163例中114例,69.9%),プラセボ群(158例中37例,23.4%)として,LJPC-501で高い血圧管理ができたという結果だった(オッズ比7.95,95%信頼区間4.76~13.3; p<0.001)。 重度な有害事象は,LJPC-501で60.7%でありプラセボ群の67.1%より低い結果だったが,28日死亡はアンジオテンシンII群で163例中75例(46%),プラセボ群で158例中85例(54%)であり,28日死亡率の低下傾向を認めるものの統計学的有意差を認めなかった(ハザード比0.78; 95%CI 0.57~1.07; P = 0.12 )。
敗血症性ショックにおける平均血圧65mmHgを目指す血圧管理としてのアンジオテンシンIIの臨床研究,すなわち平均血圧65mmHgを目指したノルアドレナリンとアンジオテンシンⅡの比較臨床研究が期待される。敗血症性ショックを対象として2013年2月から2015年5月まで施行されたバゾプレシンとノルエピネフリンの前向き臨床研究VANISH試験43)では,平均血圧65~75mmHgを目標としてバゾプレシンとノルアドレナリンが比較されたが,28日死亡率および急性腎障害の改善に有意差が認められなかった。これに対して,平均血圧60mmHgを超えることを目標としたバソプレシンV1A受容体に選択性の高いセレプレシンの臨床研究が継続されている44)。アンジオテンシンⅡアナログの産業については,アンジオテンシンⅡの学術的背景や病態生理学を重視することが大切であり,日本への導入においては安全性確認として臓器不全を残さないように,また長期予後を慎重に評価していくことが必要な検討内容の一つと評価された。
敗血症性ショックにおける心機能抑制という留意事項
敗血症は,交感神経緊張などのアドレナリン作動性β受容体作用,アシデミア,低体温,サイトカイン受容体シグナルなどにより心筋細胞内で細胞内カルシウム濃度が高まりやすい病態であり,心拡張不全や不整脈の誘引となり,β受容体刺激は原則として禁忌に近い。これらの影響により,敗血症では特に右心系の細胞内カルシウム過負荷が生じやすく,右心不全が生じやすい。
2017年に報告されたメイヨークリニックからの2007年1月から2014年の12月までの388例の敗血症症例の解析45)では,214 例(55.2%)が敗血症に右心不全を合併しており,右心不全と左心不全を合併しているのは100例(25.8%)だった。ドブタミンなどのアドレナリン作動性β受容体刺激は,診療における不整脈発生や免疫抑制等の弊害である一方で,敗血症性ショックの予後を改善するという臨床研究は完全に認められない。
一方,慢性的にβ遮断薬を服用している患者群では敗血症の予後が良好であること46)や,敗血症におけるβ受容体遮断薬が敗血症の予後を改善することは臨床研究や症例報告などで示唆されている。エスモロールの5つの臨床研究のレビュー47)では,エスモロールは生存率を有意に高め,心拍数とトロポニンIを有意に低下させ,血圧,中心静脈圧および中心静脈酸素飽和度を悪化させないことが示めされている。
敗血症において,心筋細胞内カルシウム過負荷は,心房筋,そして心室筋に生じる。緊張の強い状態で救急外来に搬入されるなどの内因性カテコラミンに暴露され,心過収縮をカルシウム代謝の改善まで心刺激を休ませ,体血管抵抗管理と輸液調節で待機するのが最良かもしれない。随伴する敗血症性ショックを対象としたカルシウム感受性増強薬リボシメンダンに関する10の臨床研究について48),588例が解析され,乳酸値を低下させるが,死亡率改善には有意差が認められないという結果だった(リスク比0.96,95%信頼区間0.81-1.12)。このような病態における苦肉の策としては,アドレナリン持続投与あるいは経皮的心肺補助(ECMO)であるが,診療エビデンスは2017年においても不十分である。
敗血症性ショックにおける輸液と輸血について
敗血症性ショックの蘇生におけるearly-goal directed therapy(EGDT)は,日本版敗血症診療ガイドライン3)の通り,その詳細な蘇生プログラムは否定されている。従来,このブログ「救急一直線」でも,EGDTの最も重要な功績は敗血症性ショックの血管拡張性病態における輸液療法の積極性を輸液安全性のモニタリングとともに推奨したことにあると考えている。PRISMグループの解析49)では,2016年までの138施設3,723例の解析として,90日死亡率はEGDTで24.9%,通常治療で25.4%と報告され,あたかもEGDTを否定しているが,EGDTは敗血症性ショックの初期輸液の重要性を2001年に再提起し,2001年以降の通常治療の質を改善させたとものである。
一方,敗血症性ショックの管理の質の高まりにより,初期からノルアドレナリンを併用することにより輸液量を減少させることができることや,結果的に敗血症性ショックにおける輸液量が少ないほうが生命予後が良いことが知られている。Marik等50)は,プレミア病院データベースを用いて,救急外来からICUに入室した連続した敗血症および敗血症ショック症例23,513例の第1病日の体液を1Lの幅に分類し,1-1.99Lから9Lまでとして1L毎に輸液量で患者群を分類した。第1病日の輸液量は人工呼吸を受けていない群で平均4.4Lであり,非ショックで人工呼吸のない郡で3.6Lレベルだった。このMarik等50)の報告は,コホート全体の院内死亡率は25.8%であり,輸液量5Lを超える追加リットルにつき死亡率が2.3%ずつ増加するとし,より少ない輸液管理を推奨する内容である。
また,9施設合同の観察コフォート研究51)として,成人敗血症11,182例を対象として,敗血症の同定から30分以内,31~120分未満,120分以上における輸液開始までの時間の3群が評価され,輸液開始が早いのは低血圧,発熱,尿路感染症,軟部組織感染症,輸液開始が遅いのは心不全と腎不全として確認された。30分以内にクリスタロイドが開始されたのは530例(36%),31-120分が2,388例(21%),120分以上が3,458例(31%)であり,30分以内の輸液開始は120分を超える場合と比較して院内死亡率を有意に改善していた(オッズ比0.76,信頼区間0.64-0.90)。このような輸液開始までのタイミングの研究も散見される。
輸液量を減少させせる工夫として,3%食塩水を用いた研究が報告されているが,REVA research network52)からは,敗血症性ショックにおいて3%食塩水は生命予後を改善しないことが報告されている。この研究は,2012年11月3日から2014年6月13日まで,18歳以上の成人敗血症性ショックを対象としてフランスの22施設で施行された434例の報告であり,酸素化管理をSaO2 88-95%の正常酸素群とFIO21.0の高酸素群,また3%食塩水による蘇生群と,0.9%生理食塩水による蘇生群の4群が評価された。しかし,この研究では,FIO21.0の高酸素群で死亡率が高まる可能性が認められたため,安全性の理由から予定より早めに中止された。敗血症性ショックの管理においても,本研究のように高濃度酸素暴露の危険性が示唆されている。解析された434例における28日死亡は,高酸素で217例中93例(43%),正常酸素群217例中77例(35%),一方,蘇生に用いる食塩水においては高張群で214例中89例(42%),等張群で220例中81例(37%)であり,統計学有意差を認めなかった。敗血症性ショックにおいて,3%食塩水を用いて輸液総量を減少させる成果としては,REVA research network52)を超えた十分なエビデンスが認められない。以上のような,輸液の適正化を探る研究は,2018年移行もTrialなどに報告され,企画されている。
最後に,敗血症性ショックにおける赤血球輸血による酸素運搬の改善として,日本版敗血症診療ガイドライン20163)のCQ.9-1に記載されているようにHb≧7.0 g/dLが推奨され,心血管系イベントのある場合ではHb.10g/dLを考慮する。このデータに補綴する内容としては,UTCOMEREA Study Group53)のデータとして,フランスのマルチセンターデータベースを用いた敗血症6,016例の前向き解析研究がある。本研究53)では,赤血球輸血の有無は死亡率を統計学的には増加させないが(ハザード比1.07,95%信頼区間 0.88-1.30),新たな感染症発症(ハザード比2.77,95%信頼区間2.33-3.28)および低酸素血症の増悪(ハザード比1.29,95%信頼区間1.14-1.47)を認め,ヘマトクリット値26%レベルの管理を適正とし,ハザード比を0.72(95%信頼区間0.55-0.95)に減少できると報告している。
文 献
1. Singer M, Deutschman CS, Seymour CW, et al. The third international consensus definitions for sepsis and septic shock (Sepsis-3). JAMA 2016;315:801-10.
2. American College of Chest Physicians/Society of Critical Care Medicine Consensus Conference: definitions for sepsis and organ failure and guidelines for the use of innovative therapies in sepsis. Crit Care Med 1992;20:864-74.
3. 日本版敗血症診療ガイドライン2016. http://www.jsicm.org/pdf/jjsicm24Suppl2-2.pdf
4. Simpson SQ. SIRS in the Time of Sepsis-3. Chest. 2017 Oct 14
5. Ranzani OT, Torres A. Reply to: Sepsis-3 in community-acquired pneumonia: How reliable is it? Am J Respir Crit Care Med. 2017 Sep 11.
6. Schmoch T, Bernhard M, Uhle F, et al. New Sepsis-3 definition : Do we have to treat sepsis before we can diagnose it from now on? Anaesthesist. 2017;66:614-21.
7. Carneiro AH, Póvoa P, Gomes JA. Dear Sepsis-3, we are sorry to say that we don't like you. Rev Bras Ter Intensiva. 2017;29:4-8.
8. Fang X, Wang Z, Yang J, et al. Clinical evaluation of Sepsis-1 and Sepsis-3 in the ICU. Chest. 2017 Jul 12.
9. Kaukonen KM, Bailey M, Pilcher D, et al. Systemic inflammatory response syndrome criteria in defining severe sepsis. N Engl J Med. 2015;372: 1629-38.
10. Peake SL, Delaney A, Bailey M, et al. ARISE Investigators. Potential impact of the 2016 consensus definitions of sepsis and septic shock on future sepsis research. Ann Emerg Med. 2017;70(4):553-561
11. Sterling SA, Puskarich MA, Glass AF, et al. The impact of the sepsis-3 septic shock definition on previously defined septic shock patients. Crit Care Med. 2017;45:1436-1442.
12. Amland RC, Sutariya BB. Quick Sequential [Sepsis-Related] Organ Failure Assessment (qSOFA) and St. John Sepsis Surveillance Agent to detect patients at risk of sepsis: an observational cohort study. Am J Med Qual. 2017 Feb 1:1062860617692034
13. Donnelly JP, Safford MM, Shapiro NI, et al. Application of the Third International Consensus Definitions for Sepsis (Sepsis-3) Classification: a retrospective population-based cohort study. Lancet Infect Dis. 2017;17:661-70.
14. French Society of Emergency Medicine Collaborators Group. Prognostic accuracy of sepsis-3 criteria for in-hospital mortality among patients with suspected infection presenting to the emergency department. JAMA. 2017;317:301-8.
15. Australian and New Zealand Intensive Care Society (ANZICS) Centre for Outcomes and Resource Evaluation (CORE). Prognostic accuracy of the SOFA score, SIRS criteria, and qSOFA score for in-hospital mortality among adults with suspected infection admitted to the intensive care unit. JAMA. 2017;317:290-300.
16. SepNet Critical Care Trials Group. Incidence of severe sepsis and septic shock in German intensive care units: the prospective, multicentre INSEP study. Intensive Care Med. 2016;42:1980-9.
17. Piano S, Bartoletti M, Tonon M, et al. Assessment of Sepsis-3 criteria and quick SOFA in patients with cirrhosis and bacterial infections. Gut. 2017 Aug 31.
18. Levy MM, Fink MP, Marshall JC, et al. 2001 SCCM/ESICM/ ACCP/ATS/SIS international sepsis definitions conference. Crit Care Med 2003;31:1250-6.
19. Williams JM, Greenslade JH, McKenzie JV, et al. Systemic inflammatory response syndrome, quick sequential organ function assessment, and organ dysfunction: insights from a prospective database of ED patients with infection. Chest. 2017;151:586-96.
20. Shankar-Hari M, Harrison DA, Rubenfeld GD, et al. Epidemiology of sepsis and septic shock in critical care units: comparison between sepsis-2 and sepsis-3 populations using a national critical care database. Br J Anaesth. 2017;119:626-36.
21. Stevenson EK, Rubenstein AR, Radin GT, et al. Two decades of mortality trends among patients with severe sepsis: a comparative meta-analysis. Crit Care Med. 2014;42:625-31.
22. Shin TG, Hwang SY, Kang GH, et al. Korean Shock Society septic shock registry: a preliminary report. Clin Exp Emerg Med. 2017;4:146-53.
23. Lee CC, Yo CH, Lee MG, et al. Adult sepsis-A nationwide study of trends and outcomes in a population of 23 million people. J Infect. 2017;75:409-19.
24. Leisman DE, Doerfler ME, Schneider SM, et al. Predictors, prevalence, and outcomes of early crystalloid responsiveness among initially hypotensive patients with sepsis and septic shock. Crit Care Med. 2017 Nov 3.
25. Pruinelli L, Westra BL, Yadav P, et al. Delay Within the 3-Hour Surviving Sepsis Campaign guideline on mortality for patients with severe sepsis and septic shock. Crit Care Med. 2018 Jan 2.
26. Dellinger RP, Levy MM, Rhodes A, et al. Surviving sepsis campaign: international guidelines for management of severe sepsis and septic shock, 2012. Crit Care Med 2013;41:580-637.
27. Oh DH, Kim MH, Jeong WY, et al. Risk factors for mortality in patients with low lactate level and septic shock. J Microbiol Immunol Infect. 2017 Aug 26.
28. Driessen RGH, van de Poll MCG, Mol MF, et al. The influence of a change in septic shock definitions on intensive care epidemiology and outcome: comparison of sepsis-2 and sepsis-3 definitions. Infect Dis (Lond). 2017: Sep 26:1-7.
29. Tarui T, Yamaguchi Y, Suzuki K, et al. Early evaluation of severity in patients with severe sepsis: a comparison with "septic shock" - subgroup analysis of the Japanese Association for Acute Medicine Sepsis Registry (JAAM-SR). Acute Med Surg. 2017;4:426-431.
30. JAAM Sepsis Registry (JAAMSR) Study Group. Assessment of mortality by qSOFA in patients with sepsis outside ICU: A post hoc subgroup analysis by the Japanese Association for Acute Medicine Sepsis Registry Study Group. J Infect Chemother. 2017;23:757-62.
31. ALBIOS Biomarkers Study Investigators. Pentraxin 3 in patients with severe sepsis or shock: the ALBIOS trial. Eur J Clin Invest. 2017;47:73-83.
32. Hamed S, Behnes M, Pauly D, et al. Diagnostic value of Pentraxin-3 in patients with sepsis and septic shock in accordance with latest sepsis-3 definitions. BMC Infect Dis. 2017 ;17:554.
33. Jie H, Li Y, Pu X, Ye J. Pentraxin 3, a Predicator for 28-Day Mortality in Patients With Septic Shock.
Am J Med Sci. 2017;353:242-46.
34. Liu SY, Zhang L, Zhang Y, et al. Bioinformatic analysis of pivotal genes associated with septic shock. J Biol Regul Homeost Agents. 2017;31:935-41.
35. Katip W, Jaruratanasirikul S, Pattharachayakul S, et al. The pharmacokinetics of vancomycin during the initial loading dose in patients with septic shock. Infect Drug Resist. 2016;9:253-260.
36. Sjövall F, Alobaid AS, Wallis SC, et al. Maximally effective dosing regimens of meropenem in patients with septic shock. J Antimicrob Chemother. 2018;73:191-198.
37. Sherwin R, Winters ME, Vilke GM, et al. Does Early and Appropriate Antibiotic Administration Improve Mortality in Emergency Department Patients with Severe Sepsis or Septic Shock? J Emerg Med. 2017;53:588-595.
38. Laine ME, Flynn JD, Flannery AH. Impact of Pharmacist Intervention on Selection and Timing of Appropriate Antimicrobial Therapy in Septic Shock. J Pharm Pract. 2017:897190017696953.
39. Asfar P, Meziani F, Hamel JF, et al. High versus low blood‐pressure target in patients with septic shock. N Engl J Med 370:1583–93.
40. Lamontagne F, Meade MO, Hebert PC, et al. Higher versus lower blood pressure targets for vasopressor therapy in shock: a multicenter pilot randomized controlled trial. Intensive Care Med 42:542–50.
41. Lamontagne F, Day AG, Meade MO, et al. Pooled analysis of higher versus lower blood pressure targets for vasopressor therapy septic and vasodilatory shock. Intensive Care Med. 2017 Dec 19.
42. Khanna A, English SW, Wang XS, et al. Angiotensin II for the treatment of vasodilatory shock. N Engl J Med. 2017;377:419-30.
43. VANISH Investigators. Effect of early vasopressin vs norepinephrine on kidney failure in patients with septic shock: The VANISH randomized clinical trial. JAMA. 2016;316:509-18.
44. Russell JA, Vincent JL, Kjølbye AL, et al. Selepressin, a novel selective vasopressin V1 aagonist, is an effective substitute for norepinephrine in a phase IIa randomized, placebo-controlled trial in septic shock patients. Crit Care. 2017;21:213.
45. Vallabhajosyula S, Kumar M, Pandompatam G, et al. Prognostic impact of isolated right ventricular dysfunction in sepsis and septic shock: an 8-year historical cohort study. Ann Intensive Care. 2017;7:94.
46. Fuchs C, Wauschkuhn S, Scheer C, et al. Continuing chronic beta-blockade in the acute phase of severe sepsis and septic shock is associated with decreased mortality rates up to 90 days. Br J Anaesth. 2017;119:616-625.
47. Liu P, Wu Q, Tang Y, et al. The influence of esmolol on septic shock and sepsis: A meta-analysis of randomized controlled studies. Am J Emerg Med. 2017 Nov 8.
48. Wang B, Chen R, Guo X, et al. Effects of levosimendan on mortality in patients with septic shock: systematic review with meta-analysis and trial sequential analysis. Oncotarget. 2017;8:100524-32.
49. PRISM Investigators, Rowan KM, Angus DC, et al. Early, Goal-Directed Therapy for Septic Shock - A Patient-Level Meta-Analysis. N Engl J Med. 2017;376:2223-34.
50. Marik PE, Linde-Zwirble WT, Bittner EA, et al. Fluid administration in severe sepsis and septic shock, patterns and outcomes: an analysis of a large national database. Intensive Care Med. 2017;43:625-32.
51. Leisman DE, Goldman C, Doerfler ME, et al. Patterns and outcomes associated with timeliness of initial crystalloid resuscitation in a prospective sepsis and septic shock cohort. Crit Care Med. 2017;45:1596-606.
52. HYPER2S Investigators; REVA research network. Hyperoxia and hypertonic saline in patients with septic shock (HYPERS2S): a two-by-two factorial, multicentre, randomised, clinical trial. Lancet Respir Med. 2017;5:180-90.
53. UTCOMEREA Study Group. Effect of Transfusion on Mortality and Other Adverse Events Among Critically Ill Septic Patients: An Observational Study Using a Marginal Structural Cox Model. Crit Care Med. 2017;45:1972-80.