'13-08-22投稿
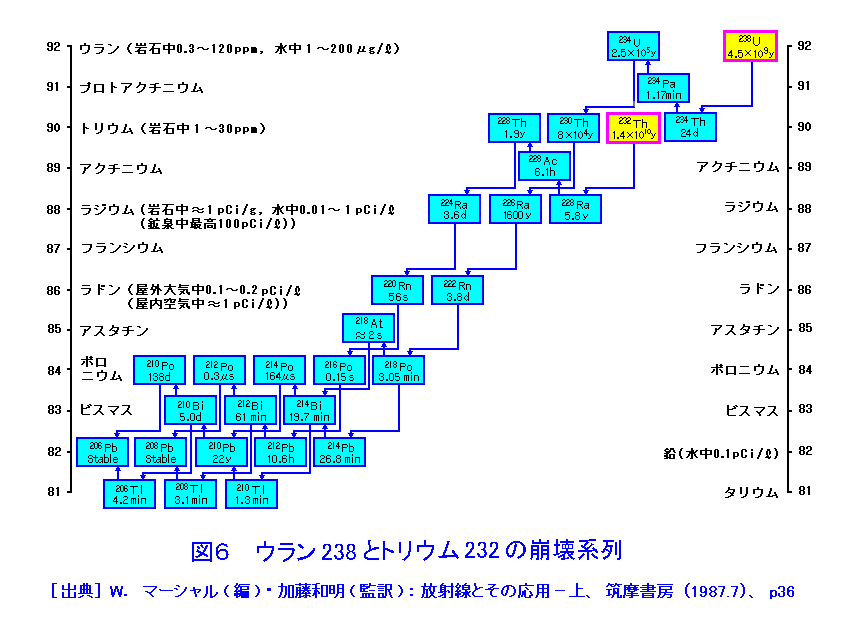
福島原発から海に漏洩しているトリチウム水は既報 トリチウム水の環境への影響に係る記載 2013-03-24の引例
ATOMICA
トリチウムの生物影響 (09-02-02-20)
http://www.rist.or.jp/atomica/data/dat_detail.php?Title_Key=09-02-02-20によれば、
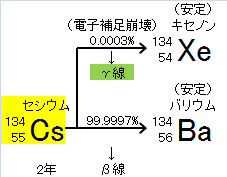
トリチウムはトリチウム水(HTO)の形で環境に放出され人体にはきわめて吸収されやすい。また、有機結合型トリチウム(OBT)はトリチウムとは異なった挙動をとることが知られている。動物実験で造血組織を中心に障害を生ずることが明らかにされ、ヒトが長期間摂取した重大事故も発生している。・・・ トリチウムは水素の同位体で、最大エネルギー18.6keVで平均エネルギー5.7keVという非常に低いエネルギーのβ線を放出し物理的半減期は12年であるという。
ということですが、どの程度有害かどうか?現実的にはわかり難く、またトリチウムはもともと自然界に微量存在していることも事実ですが、長年、気がつかず汚染した飲料水を飲んでいたとしてもその後遺症については定かではないと思っています。
20世紀の夢のエネルギーともてはやされた原発も一度事故が起って環境中に放出されたトリチウムなど、この先何十年とも杞憂と妄想の世界で生活しなければならないのだろうか?とあきらめの境地の方もいると思われます。
一方では環境(水)中の放射性物質の影響と浄化に係る記載(その19:「ホルミシス」と「ペトカウ」効果について)(2012-02-05)で記載しましたように、環境中の放射能、放射線の生体への影響として、
古くから「ホルミシス」効果と「ペトカウ」効果が言われています。
Wikipedia記事検索によれば
ホルミシス効果(hormesis)とは、
「生物に対して通常有害な作用を示すものが、微量かつごく一時的であれば逆に良い作用を示す可能性のある生理的刺激作用のこと。・・・」
のように、個人的には「酒は百薬の長」の類と同様に、その摂取量如何によっては猛毒ともなり命を落とすこともあると思っています。
既報でも記載しましたが、誤解、妄想?杞憂かもしれませんことを
予め断っておきます。
トリチウム汚染水についても通常の水(H2O)と重水素水(HDO)、いわゆる問題となっているトリチウム水(三重水素水 HTO)を高感度に分析して、重量組成比で把握できれば、万一、後遺症が発生した場合の参考になるのでは?と思っています。放射能は測定方法、位置などによって誤差が生じ易いのでは???と、また、一般的には水の中に有害物質が混入している場合、重量換算して組成比で判り易く、表示することが望まれます。
関連投稿:
2013-03-24
要するに通常飲用している水にどのくらい含まれているのか?と思っています。
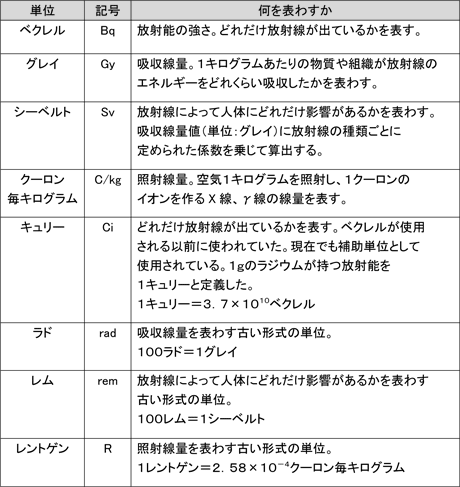
詰まるところは、放射能の単位ベクレル、シーベルトなどは一般人には理解しがたい表現?でその含有量の大小を示しているため?かと個人的には思っています。
クロム、カドミウム汚染のように、化学組成の重量比(・・・、PPM、PPB、PPT、・・・)もしくは重量含有量(・・・mg/L、μg/L、ng/L、pg/L・・・)で表示して報道すれば紛れが少ないのでは?と想われます。
今回は、化学分野で「きれいな水」とはどのようなものか原点に立ち返って、解説されている情報を調べました。
「きれいな水」
引用:http://www.shse.u-hyogo.ac.jp/kumagai/eac/ea/water.html
(一部割愛しました。)
「1.始めに
化学的には当然H2Oを意味しますが狭い意味では液体の水、英語ではWater、気体の水は水蒸気steam(vapor)、固体の水は氷iceと呼ばれ物質の3つの相各々に名前がつけられています。
酸素1原子と水素2原子からなる水分子は水素原子が(+)に酸素原子が(-)に分極するため様々な物質を、特にイオン性物質をよく溶かす性質を持っています。適度なミネラル分を溶かすことで人にとっておいしい水にもなり、有毒な化学物質を溶かすことで生命を脅かす元ともなります。身の回りにに見られる水にはどんなものがとけ込み、またどのような方法できれいな水、化学的に純粋な水が造られて科学技術の進歩に貢献しているかを考えてみます。
古代の元素観と水
万物の根源となるものが水であると最初に言い出したのはギリシャのミレトス野賢人タ-レス(BC640?-546)であると言われている。その後エンペドクレス(BC490-435)やアリストテレス(BC384-322)は空気、水、土、火の4つが物質の基であると考えた。古代インドでは「四大」と称して地(堅)、水(湿)、火(温)、風(動)の4つをそれぞれのもっている性質と対応させて考えていたし、中国では「五行」として木、火、土、金、水のそれぞれを基と考えていた。
水の性質
無色・無味・無臭の液体で融点0℃、沸点100℃(1atm)3.98℃で最大密度0.999973g/cm3をもっています。
H2Oの分子式で表される様に酸素1原子と水素2原子からできています。天然には水素の同位体として1H,2H(D),3H(T)が存在し、酸素の同位体として16O,17O,18Oが存在するため組み合せを考えると実に18種類の水が存在することになります。
水素のうち3H(T,トリチウム)は半減期約12年でβ-崩壊して3Heとなる放射性同位元素ですから9種類は放射性の水です。
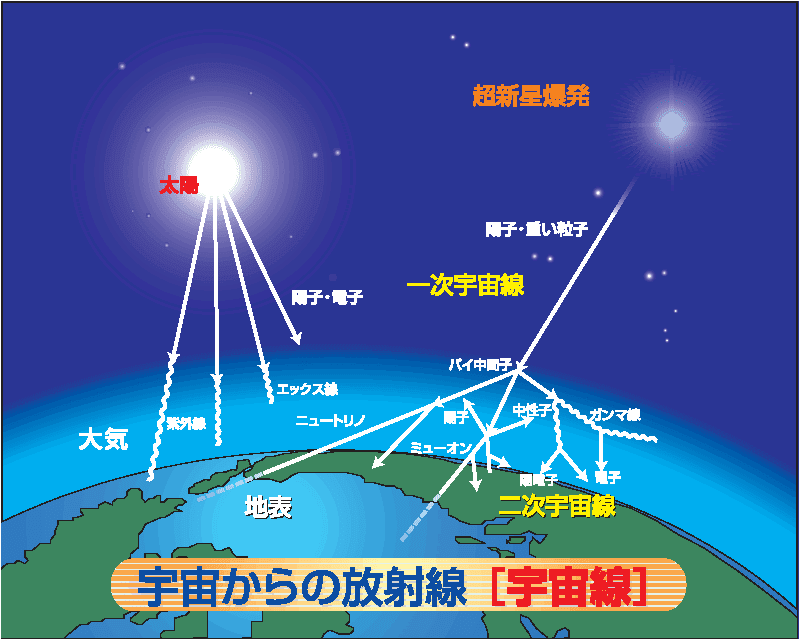
トリチウムは大気上層部で宇宙線により絶えず作られていて例えば 14N(n,3H)12Cなどの反応。地球上で1kg程度しかないので全く気にする必要はありません。D2Oで表される重水は融点3.82℃、沸点101.42℃、密度は25℃で水の1.107倍あり、11.6℃で最大密度を示します。この重水は水の電気分解で残液中に濃縮されることより作られます。
1932年アメリカのユ-リ-により初めて重水の分離が行なわれました。大規模には硫化水素と水との同位体交換反応なども使われます。
HOH(l)+HSD(g)=HOD(l)+HSH(g) K=1.01
重水はウランの核分裂時に発生する速い中性子(秒速2万km/s程度)を熱エネルギ-程度(2.2km/s)の遅い中性子までに減速させる場合に中性子を吸収しやすい軽水よりも都合がいいので原子力産業や、核研究で良く使用されています。
この重水、試薬としても使われていて99.75%の純度で100g2万円程度、100.00%程度の純粋なものでは10g1万数千円と純金と同程度価格で水としては最も高価なものといえます。最近のミネラルウオ-タ-と比較しても5000倍も高価です。
16O:17O:18O=99.757:0.039:0.204
H:D:T=99.984426:0.015574:10-19
自然界ではH216Oが99.76%,H218Oが0.71%,H217Oが0.037%,HD16Oが0.032%含まれています。
HD18Oが6x10-5%,HD17Oが1x10-5%,D216Oが1x10-6%と非常にすくなくなってきます。
単純に水といってもこの様に同位体の混合物で100%H216Oの水は極特殊な研究目的以外使われることはありません。
水は質量の単位の基
フランス革命の制度改革の一環として始まったメ-トル法では質量の基準に水が選ばれました。有名な化学者ラボアジェはこの時に定められた暫定的メ-トルに基づいて、約4℃での10cm立方の蒸留水の質量を精密に測定しました。ラボアジェは王政時代に徴税 請負人をしていた為革命政府に捕らわれ、獄中より実験室に通い、測定終了とともに処刑されたと伝えられています。現在はラボジェや彼に続く研究者の測定を基としてキログラム原器が質量の単位となっています。
水は温度の単位の基
水は温度の基準にも用いられており1気圧下での融点が0℃、沸点が100℃、水の三重点が絶対温度で273.16K(0.01℃)と決められている。
水は熱量の単位の基
熱量の単位も比較的最近まで水1gの温度を14.5℃から15.5℃まで上げるのに要する熱量としてcal(カロリ-)と呼んでいた。現在は仕事の単位であるJ(ジュ-ル)が熱量の単位として用いられ1cal=4.186Jとなっている。
3.自然界での水の存在
水は私たちの生活温度に極めて近い温度(1気圧0℃)で水~氷の変換し、その時大量の熱を吸収又は放出して温度変化に対して緩衝的に働きます。水のほとんど無い砂漠地帯では60~90℃位まで上昇することが知られているし、また南極では-88℃まで気温が 下がったこともあるが南北両極地でも海洋の温度は-2℃位しか下がらないし赤道下の熱帯でも水温は35~36度以上には上がりません。
生物は水環境から生まれてきたこともありその生活は水の特性に大きく助けられています。例えば水は4℃で最大密度を持ち、氷になると9%の密度の減少するため外気温が下がっても底部に4℃に近い水が残り、熱の伝導能力の小さいこともあいまって生物の生存に役だっています。人の体重の約66%は水であり、赤ちゃんの場合は約80%にも達する水は正に生物にとって命の水であると言える。
さて、地球上のほとんどの水は海水として存在しその量は約1.32×1021L、地球上の天然水の97.2%を占めています。その他に陸水(河川,湖沼,地下水)、極地方の氷として、また気圏の水蒸気、雲さらに地下水などとして存在します。・・・
水に溶け込んでいる物質の例
水には様々なものが溶け込みます。水に溶け込んでいるものとしては大きく分けて次の3つがあげられます。
- 固体微粒子(懸濁状シリカ、重金属酸化物)、コロイド状物質(コロイド状シリカ、重金属水酸化物、有機物)、溶存高分子物質、生物(細菌類、藻類)
- 低分子電解質(ナトリウム、カリウム、カルシウム、その他金属陽イオン、塩化物、硫化物、硝酸塩、その他陰イオン)
- 低分子非電解質(溶存酸素、溶存窒素等)
その中でも特に電解質(各種イオン類)を良く溶かします。
陸水中に含まれるイオンの平均的含有量は
Ca2+>Na+>Mg2+,HCO3->Cl->SO42-の順であり、多くは大気中の二酸化炭素の溶解でpH5.5~6.5となっています。
Water's Path(純粋な水への道)
私は化学を専門としているので研究室で日々純粋な水を使用して試薬を調製しています。またハイテク分野では半導体の洗浄に超純水が使用されています。この水がどの様な道筋を経て作られているかを考えてみたいと思います。
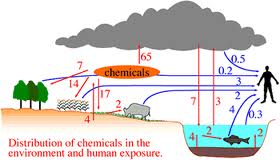
比較的純粋な蒸気となった水が上昇気流にのって雲になり、雨となって降って来る間にレインアウト(雨の核として取り込まれる)やウオッシュアウト(降下する雨滴に取り込まれる)を経て空気中の無機・有機微粒子やCO2ガスを吸収しpH5.6程度の弱酸性となります。大気汚染の基となるNOxやSOx等の酸性ガスが存在するときは更に酸性となることもあります。
この降水の化学的組成の平均値はppm単位で
Na 1.1、K 0.26、Mg 0.36、Ca 0.97
Cl 1.1、F 0.089、S(硫酸+硫黄) 1.5
Si(珪酸+ケイ素)0.839、Fe 0.23 Al 0.11
P(燐酸+リン) 0.014となっている。
日本の年間降水量は平均1750mmでこのうち1/3は蒸発により空に戻り、残り2/3の内約40%は全く利用されずに海に流れ去る。
上水道、農業用、工業用に利用されるのは10%強である。
さてこの雨は川となって流れ、一部の水は地下水となって浄水場に集められます。この過程で各種の無機・有機イオン類や固体微粒子、細菌、藻類が混入してきます。
もし川の水が良質であれば1日4~5m砂の層に通すだけの緩速漉過を行ない塩素殺菌するだけでも十分飲用水として使えますが、残念ながらそのような川は少なく、硫酸アルミニウムなどの凝集剤を加えて鉄やマンガン等の不純物を大型の浮遊物とし、沈降分離する必要があります。その後1日120~150mの急速漉過方式で浄水します。その後病原菌・大腸菌等の消毒のため通常塩素殺菌が行なわれます。この塩素殺菌のため水道水はカルキ臭いといわれ、最近のグルメ指向もあって名水ブ-ムを生む基となっています。 この名水ブ-ムで各地の湧水が注目され美味しいと評判ですが見かけが澄んでいて飲んで美味しく感じられても大腸菌やフッ素、ヒ素その他の有害物質が含まれていることもあり注意が必要です。
井戸水を調査した結果、かなり広範囲にトリクロロエチレン、テトラクロロエチレン、1-1-1-トリクロロエタン等の含塩素有機溶剤が検出され問題になっています。これらの物質は揮発性が大きいので河川では気散により急減しますが、地下に浸透するといつまでも残留する性質があるためです。
ここまでの過程でやっと水道水が得られたわけです。
美味しい水
最近日本の水道水まずくなりましたが海外の水と比べるとまだまだ捨てたものではないようです。
水を美味しくする成分として
- ミネラル これはカルシウム、マグネシウム、ナトリウム、カリウム、鉄、マンガン等で30~200mg/L、特に100mg/l程度がよいといわれています。
- 硬度 これはカルシウム+マグネシウムの量で10~100mg/L、中でも50mg/Lが良い。
日本の水道の硬度は20~80mg/L程度で良好な値です。
- 炭酸ガス 1l中3~30mg
- 溶存酸素 5mg/L以上が望ましい。
- 水温 10℃~15℃
水をまずくする成分
- 過マンガン酸消費量 これはフミン酸などの水中の有機物の量を表し3mg/l以下が望ましい。
- 嫌な匂いをつける物質 フェノ-ル類、シクロヘキシルアミン、ジオスミン、ジメチルイソボルネオ-ル(かび臭い原因)、硫化水素、残留塩素、油
- 嫌な味をつける物質 塩化物イオン、鉄、銅、亜鉛
海水から真水を作る
日本では大体上記の過程で飲めるていどの水が作られていますが、海外では海水から真水が生産されているところがあります。
海水は河川や湖沼の水と異なって約3.5%もの塩類(大部分はNaCl)を含んでいるため脱塩操作が必要になります。
この脱塩には 1.蒸留法 2.逆浸透法 3.電気透析法(イオン交換膜法) 4.イオン交換樹脂塔式法 等があります。
1.蒸留法 実験室で使用する水の場合はこの蒸留法が良く用いられています。大規模プラントでは凝縮熱の回収を行なって熱効率をあげるなどしています。この方法は中東あたりのエネルギ-資源の豊富な所で良く用いられています。
水の蒸発熱は100℃で539calなので20℃の水1gを蒸気にするには619cal(2590J)の熱量が必要で凝縮熱の回収を行なったとしても大量の水を得るには適切ではないので大量に造水するプラントでは多段フラッシュ蒸発法が多く使われています。
これは加熱した海水を圧力を下げた容器の中で多段でフラッシュ蒸発させるもので、蒸気が凝結する際の熱を回収して熱効率を上げています。
2.逆浸透法
イオンは通さないが水は通す膜を半透膜と呼んでいます。この半透膜を介して真水と食塩水をおくと真水が食塩水にしみこみます。逆に、例えば酢酸セルロ-スに処理をおこなった膜などで、塩水に圧力をかけると半透膜を水だけが通過してきて真水が生産できます。
この方法は必要エネルギ-が少なくて済みます。逆浸透モジュ-ルはホロファイバ-(中空糸型)やスパイラル型等を用いています。
3.イオン交換膜を利用した電気透析法
海水中には電気を運ぶイオンが溶け込んでいることを考え、水槽に陽極、陰極の電極をいれ、陽極側に陰イオン交換膜を陰極側に陽イ オン交換膜をおいて水槽を3室に分けて電圧を加えると、海水中のイオンが各々移動し、2つの膜に囲まれた部分に脱塩水が出来ます。
この方法は蒸留法より電気代が少なくて済みます。またこの膜を組み合わせて脱塩すると塩の濃縮もでき、食塩製造もできます。本来 は海水濃縮に適した方法で日本では真水の生産目的より食塩生産の目的でこの電気透析法が用いられています。
4.イオン交換樹脂塔式法
陽イオン交換樹脂と陰イオン交換樹脂とを混合した塔に海水を通じると陰イオンはOH-に交換され陽イオンはH+に交換されて結果
として脱塩水が生成します。3の電気透析法とこのイオン交換樹脂法共非イオン性物質は取り除けません。
NaClとの反応は次の通りです。
陽イオン交換 R-H + Na+ = R-Na + H+
陰イオン交換 R-OH + Cl- = R-Cl + OH-
H+ + OH- = H2O
イオン交換の結果水が生じます。
日本のメ-カ-による脱塩プラント(1984年)では多段フラツシュ法が95.4%、逆浸透法が3.3%、電気透析法が0.45%となっています。イオン交換法は大規模なプラントでは使われていません。
超純水とは
最近はオゾン層破壊の問題もありエアコンや冷蔵庫等の冷媒として、また半導体の表面洗浄剤として使用されてきたフロンガスが使用できなくなり、多量に使っていた半導体分野では代わって超純水が洗浄剤として使われています。しかし水はその特性上各種の物質を溶かしこみ、洗浄の際に0.数μmといわれているメモ-リ-等の基盤上の溝に不純物を残し、製品を駄目にしてしまいます。
1Mビットでは1μmの加工線幅でしたが4Mビットでは0.8μm、16Mビットでは0.5~6μmとなり、除去すべき粒子は線幅の1/10の0.05μmとなってきています。この問題を解決キる一助となる超純水の試験方法が日本工業規格に最近定められました。(JIS K0550~K0556)
超純水の作り方
最初に超純水と呼べるものを精製したのはドイツの物理学者コ-ルラウシェで連続42回真空蒸留を行なって水の電気伝導度を測定したところ3×10-8Ω-1cm-1(18℃)を得たと言われています。現在では理論値の5.45×10-8Ω-1cm-1(25℃)程度の水が得られており、この値は同じ断面積の銅線を地球3500周するだけの抵抗であり、非常に電気を通し難いことが分かります。水が電気を通すのは不純物として溶け込んでいるイオンの為で天然水の中では雨水が最も伝導度が小さく1×10-5Ω-1cm-1(25℃)程度、地下水は5×10-5~3×10-4Ω-1cm-1、河川水の多くは1×10-4~5×10-4Ω-1cm-1程度、海水は3×10-2Ω-1cm-1程度です。原子炉やボイラ-ではかん石が沈着するのを防ぐため1×10-6Ω-1cm-1程度の水が使用されています。しかし伝導度測定だけでは水に溶解している非電解質や水に不溶性の微粒子の存在を知ることができません。
先端技術分野、例えば半導体分野のLSI製造(1Mbit程度)では通常の純水では不十分で1gあたり0.1μm以上の微粒子が数個以下、微生物・細菌は100g当たり数個以下という超純水が必要とされています。これは不純物濃度にすると1ppq以下となり、非常に純度が高いことがわかります。
水を精製する方法は原理的には海水の淡水化の方法が使用できるわけですがそのままでは超純水は製造できません。
蒸留法にしても容器からの汚染を防ぐため石英製の2段蒸留器を使用したり、沸騰の際の飛沫汚染を防ぐため非沸騰式蒸留器を使います。イオン性の物質はイオン交換法で殆ど除去できますがミクロの微粒子については適当なフィルタ-を用いる必要があります。所謂メンブランフィルタ-とかウルトラフィルタ-とか呼ばれているもので一般的な粒子除去用、細菌除去用としてはニトロセルロ-スやセルロ-ス混合エステルを有機溶媒用には再生セルロ-スが用いられている。例えばミリポアフィルタ-では孔径は0.025μm~14μmと除去目的の粒子の直径を選ぶことができます。ウルトラフィルタ-では機械的強度を保つために多孔性フィルム上にコロジオンやニトロセルロ-スの薄膜を積層させて製作し、1~10nmと分子量が百数から数十万の蛋白質等の有機物の分離除去が可能です。最近はさらに高機能性の分離膜が開発され高純度の水が得られるようになってきました。このろ紙は中空糸膜フィルタ-として使用されています。
半導体分野で要求される超純水の水質
| 項目 |
抵抗率(MΩ-cm) |
微粒子(個/ml)>0.1μm |
>0.07μm |
>0.03μm |
生菌(個/l) |
TOC(μC/l) |
シリカ(μg/l) |
Na (μg/l) |
Fe (μg/l) |
Zn (μg/l) |
Cu (μg/l) |
Cl (μg/l) |
溶存酸素(μg/l) |
| 現状 |
>18.0 |
<5 |
- |
- |
<5 |
<10 |
<3 |
<0.1 |
<0.1 |
<0.1 |
<0.1 |
<0.1 |
<30 |
| 16Mビット |
>18.1 |
<10 |
<5 |
<5 |
<1 |
<5 |
<0.5 |
<0.05 |
<0.05 |
<0.05 |
<0.05 |
<0.05 |
<5 |
| 64Mビット |
>18.2 |
- |
- |
<10 |
<1 |
<1 |
<0.1 |
<0.01 |
<0.01 |
<0.01 |
<0.01 |
<0.01 |
<1 |
超純水の保存
私が学生の頃は純水(蒸留水)は銅製の蒸留釜を使った自動蒸留器でしたがその後硝子製蒸留器、イオン交換、逆浸透法及びその組合せに発展し、現在のような超純水製造器が使用されるようになっていますが、純水の純度が上がって来ると保存容器からの汚染が問題になってきます。精製した水は直ちに使うのが原則ですが、2週間保存での汚染デ-タを示します。
水の保存容器による汚染 (ppb)
| 金属 | 容 器 材 料 |
ホウケイ酸ガラス |
ポリエチレン |
| Al |
9.2 |
0.3 |
| Cu |
0.7 |
0.1 |
| Fe |
3.6 |
1.0 |
| Pb |
2.1 |
1.0 |
| Zn |
3.2 |
1.0 |
2回蒸留水を2週間保存
超純水用配管には塩化ビニ-ル(PVC)、ポリプロピレン(PP)、ポリビニリデンフルオライド(PVDF)、パ-フロロアルコキシビニルエ-テル(PFA)、ポリエ-テルエ-テルケトン(PEEK)などが使用されているが、PEEKが良い結果を得ています。半導体工場では超純水を循環させ絶えずピュア-の状態になるようにして使用しています。
分析化学と水
高感度の分析機器の発展で分析感度がppm(100万分の1)からppb(10億分の1)、ppt(1兆分の1)、最近はppq(1000兆分の1)まで登場しています。
ppm:parts per million 10-6
ppb: billion 10-9
ppt: trillion 10-12
ppq: quadrillion 10-15
50mプ-ルの水が約1000トン、つまり109gですからこの中に1gの砂糖を入れると1ppb(10億分の1)となります。
この様に極微量成分の分析を行なうようになってくると試薬やそれを溶解する水の中の不純物の存在も問題になってきます。次に外海洋水の分析値の変遷の一例を示します。
外洋水中の重金属元素濃度(ppb)測定値
| 元素 |
Mn |
Fe |
Co |
Ni |
Cu |
Zn |
Pb |
Cd |
| 1965年 |
2 |
10 |
0.1 |
2 |
3 |
10 |
0.03 |
0.11 |
| 1975年 |
0.2 |
2 |
0.05 |
1.7 |
0.5 |
4.9 |
0.03 |
0.1 |
| ~1980年 |
0.02~0.1 |
0.2~0.5 |
0.005 |
0.2~0.6 |
0.02~0.3 |
0.01~0.6 |
0.02~0.06 |
0.01~0.1 |
測定値は年々小さな値となっています。これは水精製の技術を含めた採水、貯水、分析時のクリ-ン技術の進歩によるもので、実際に海水中の微量金属濃度が低下したためではありません。
次に水の精製法の違いによる不純物の量の一例を示します。
A法: 非沸騰法(NBS)
B法: 水道水を金属製の蒸留器で蒸留
C法: 水道水を活性炭ろ過、イオン交換樹脂処理、
D法: 水道水を活性炭ろ過、イオン交換樹脂、石英2回蒸留、
メンブランフィルタ-処理
蒸留水中の不純物(ppb)
| 元素 |
Mn |
Fe |
Co |
Ni |
Cu |
Zn |
Pb |
Cd |
| A法 |
-- |
0.05 |
-- |
0.02 |
0.01 |
0.04 |
0.008 |
0.005 |
| B法 |
0.1 |
1.0 |
0.3 |
3.0 |
46 |
15.0 |
28 |
2.0 |
| C法 |
0.05 |
0.2 |
-- |
-- |
0.2 |
0.3 |
0.6 |
0.05 |
| D法 |
<0.01 |
0.02 |
0.00 |
<0.01 |
0.03 |
0.01 |
0.00 |
0.001 |
超純水中の不純物の分析法
JIS K0553(1990)には金属元素の試験方法が、またJIS K0556(1990)には陰イオンの試験方法が決められています。
金属元素についてはフレ-ムレス原子吸光法を用います。試料水を50倍に濃縮(蒸発法)したのち分析を行ないます。原子吸光分析法は特定元素の原子線を放出する中空陰極ランプを光源として炭素のチュ-ブ中に導入された超純水試量中の不純物元素を200-300A以上の電流で過熱し原子化した後原子線の吸収量を測るもので、極微量の金属元素の低凌駕できる分析機器です。
陰イオンについてはイオン交換クロマトグラフ法を用います。カラム中に充填された陰イオン交換樹脂中を試料が通過するうちに陰イオン交換樹脂と試料中の不純物の陰イオンとの交換分離によりそれぞれの陰イオンに分離され、電気伝導度の変化を検出する検出器で定量される仕組です。
家庭での浄水器
活性炭の効果:実験室での純水製造においても水の中の有機物の除去には活性炭の使用が効果的です。水道水を作る過程でも特に夏場かびの発性で臭気が強くなることがあります。こんな時にも活性炭は強い味方です。多くの家庭の冷蔵庫にもこの活性炭が食品の脱臭剤として入れられています。活性炭は木炭、ヤシがら、石炭チャ-その他の原料を十分に炭化した後水蒸気による高温処理などを行って作られます。1gあたり800~1200m2程度の面積をもち、多くの有機物をこの広い表面に吸着します。水道水に含まれている塩素成分もこの活性炭表面で反応して除去されます。
最近話題になっている家庭用浄水器には一次フィルタ-に続いてこの活性炭が必ず使われています。ハイテク分野では使用が普通であるメンブランフィルタ-が中空糸膜フィルタ-の形で使用されており高度なろ過もできるようになっています。牛乳よりも高価なミネラルウオ-タ-と称したただの水が飛ぶように売れている時代、水はただ(無料)ではなくなりつつあります。
最後に磨きに磨いた超純水はもはや0℃では凍らず、また100℃でも沸騰しなくなってしまいます。また化学的に純粋な水は決しておいしいものではありません。・・・」という。