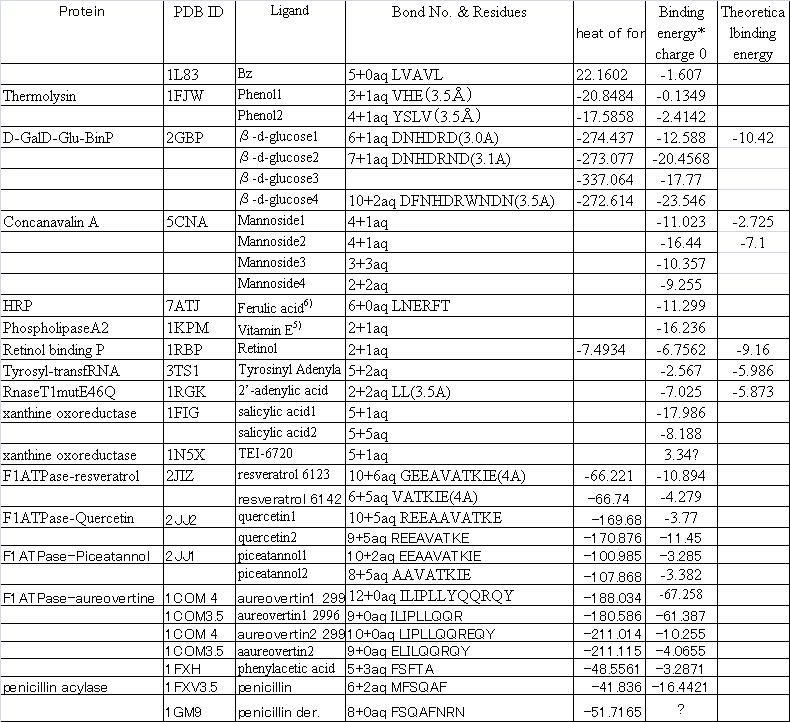
アビジンービオチン複合体以外にも、興味ある複合体が沢山ある。中でも、各種阻害剤はその典型例である。今、流行のレスベラトロールを最後に示している。表2に幾つかの計算結果を示した。どのようにこの結果を読むかは読者にお任せする。
表2 蛋白と基質の結合エネルギー(計算値)
Fig. 2.
The site of binding of resveratrol in bovine F1-ATPase. The α-, β- and γ-subunits are red, yellow, and blue, respectively, and resveratrol is green. (A) Ribbon view of F1-ATPase upwards from the mitochondrial membrane along the central axis of the γ-subunit, showing the inhibitor in solid representation bound between the γ- and βTP-subunits. (B) Side view of a solid representation of resveratrol bound in a pocket in F1-ATPase between the γ- and βTP-subunits. For clarity, the βDP and βE subunits and the three α-subunits have been removed. The pocket is in the “bearing” consisting of the sleeve provided by the N-terminal regions of α- and β-subunits in the “crown” domain of F1-ATPase and the α-helical tip of the C-terminal region of the γ-subunit. (C) Side view in stereo showing interactions of resveratrol with side chains in the binding pocket shown in stick representation with oxygen and nitrogen atoms in binding-site residues in red and dark blue, respectively. The residues shown are either within 4 Å of the inhibitor and form hydrophobic interactions, or they are linked to it via hydrogen bond networks (dotted lines) involving water molecules (light blue spheres), and by a hydrogen bond from the amido group of Val-279 to the π-electrons of the m-dihydroxyphenyl moiety of resveratrol (orange dotted line). (D and E) view of the binding pocket and bound resveratrol (with red oxygen atoms) in solid representation. D is the same view as in C, and in E, bound resveratrol and its binding pocket are viewed along the axis of γ-subunit, upwards from the mitochondrial membrane.
- 当該モデルの結合エネルギーは錯形成の良い指標になる
- 隣接残基の数を増やしても(3.0Å以内→3.5Å以内)安定化エネルギーはあまり変動しない(10%程度)
- A-B錯体は非常に安定(-20kcal/mol)で、pHを下げても(-16.2 kcal/mol)、また、その他のBiotin誘導体でも、Biotin自身よりも小さな値となる
- ヘテロダイマー蛋白ではアロステリック効果が見られ、site2はsite1よりも小さな値となる
- HRP、thermolysinでは結合数が少なく、基質の自由度が大きい
- PhospholipaseA2ではVitamin Eとの結合が比較的強く(特異的インヒビー)Vitamin Eの消炎効果との関係が示唆される
- Thermolysin は芳香環をポケット内に自由に取り込む蛋白として知られているが、フェノールとの複合化のエネルギーは非常に小さく、基質の活性化も小さい。しかし、HOMOの安定化(-0.3 eV)とOH結合の不安定化が起こっている。
- HRP-Ferulic acid複合体では隣接原子の電荷のために HOMOが大きく安定化し、OH結合が非常に弱くなっている。これがHRPの基質活性化(ラジカル化)の主要な機構であろう。
- PhospholipaseA2は2本の同一鎖(chain Aおよびchain B)から成るが、Vitamin Eはこれらに挟まれ、そのOHはchain AのHis48(およびAsp49)と強い水素結合を形成し、錯形成の安定化に寄与する。他方、LEU2、LYS7(chain A)、ASN174、CYS242(chain B)等が疎水チャンネルを形成し、Vitamin Eの側鎖と相互作用する。全体として、当錯体はサンドイッチ構造をとり、挟まれたVitamin Eは200kcal/mol以上の活性化が達成されている。当活性化がVitamin E分子のHOMOの安定化に寄与し、逆に、OH基の不安定化に寄与している
- Phosphoinositide 3-kinaseはシグナル伝達機構に関与するポケットでQuercetin、Myricetin等がその阻害剤として知られている。安定化エネルギーも非常に大きく、これらの阻害効果を端的に物語る。しかし、基質自身のHOMOと結合次数は分子の特性を反映してそれぞれ異なる。現在、ミクロカロリメトリーで実験的に得られた結合エネルギー(300種)と比較して、当法の妥当性を検討している。
<問合せ先>: ◎ラジカルのことならキーコム。出張測定可!
キーコム(株)
〒170-0005 東京都豊島区南大塚3-40-2
KEYCOM Corp. 3-40-2 Minamiotsuka,Toshima-ku Tokyo 170-0005 Japan
TEL:+81-3-5950-3101, FAX:+81-3-5950-3380
Home Page: http//www.keycom.co.jp/
E-mail: info@keycom.co.jp