
緑茶に含まれるカテキンの一種と男性機能不全(ED)治療薬を併用投与することで、正常な細胞を
傷つけずにがん細胞のみを殺し、高い抗がん作用を発揮することを、九州大大学院農学研究院の立
花宏文教授の研究チームが突き止めたニュースをこのブログで掲載したばかりなのに(『抗癌最終
観戦記Ⅰ』)、九大生体防御医学研究所の中山敬一教授らの研究チームは、抗がん剤が効きにくい
がん幹細胞を標的にした治療法を開発、マウスで効果を実証したニュースが届く。それによると、
増殖が速いがん細胞は、常に細胞分裂を行い、抗がん剤や放射線治療はこの分裂中の細胞を標的に
している。一方、がん幹細胞は増殖が遅く、ほとんどが増殖しない「静止期」にとどまり抗がん剤
などは効きにくく、再発のもとになっていたが、細胞を静止期にとどまらせる遺伝子「Fbxw7」に
着目。血液のがんである白血病を発症させたマウスの同遺伝子が働かないように操作したところ、
静止期にとどまるがん幹細胞が急減。このマウスに抗がん剤を投与すると、無治療のマウスや、抗
がん剤のみを投与したマウスに比べ、生存率が大幅に向上。同様の仕組みは、白血病以外のがんで
も予測されているほか、同種の遺伝子はヒトでも確認されているという。中山教授は「増えない細
胞がなぜ静止期にあるかを突き止め、静止期から追い出して、たたくことができた」と話しており、
今後数年をかけて、Fbxw7を一時的に働かなくする薬の実用化のめどを付けるという。

それにしても癌細胞を根絶する抗体医薬品アプローチとはどんなものなのか?ここで再びお復習い
してみた(『進化を続ける抗体医薬』、角田浩行・服部有宏@「バイオサイエンスとインダストリ
ー vol.71 N0,2(2013)」)。ゲノム創薬や、標的分子に特異的に作用する分子標的医薬の創製
(→分子標的治療)が盛んに行われ、分子標的医薬の中で抗体医薬品は、標的分子に対する高い特
異性と少ない副作用という特長から、21世紀に入り最も注目されている医薬品だ。抗体の代表的な
分子であるIgGは、H鎖(VH、CH1CH2、CH3からなる)とL鎖(VL、CLからなる)の2種のポリペプチドが
それぞれ2本ずつ、計4本がジスルフィド結合により結合した糖タンパク質(上図参照)。可変領域
(VHおよびVL)のアミノ酸配列の多様性により多様な標的分子に対して高い特異性と親和性が生み出
され、抗体は元来が生体内分子のため副作用が少なく、高い安全性が期待されているものだ。
また、体内で安定かつ血中半減期が長いために効果が長期間持続する。さらに、抗体は多様な作用
メカニズムの薬効特徴をもち、(1)受容体に結合し生体の反応を遮断する中和作用を有し(2)
標的分子を追尾能力を持つ-専門的に「抗体のFc領域はNK細胞やマクロファージ上のFcレセプタ
ーに結合することにより、これらの細胞を活性化させ、抗体依存性細胞傷害活性(ADCC)を誘導する。
エフェクター細胞ではなく、血液中の補体成分を活性化させ補体依存性細胞傷害活性(CDC)を誘導す
る」ということになる。なので、ここでは出来る限り分かりやすいように?翻意したい。
1975年にKohlerとMilsteinが細胞融合技術を応用したモノクローナル抗体作製法を報告して以来、
モノクローナル抗体は医学・生物学の研究材料、臨床診断薬として貢献をする。1980年代後半には
遺伝子工学的手法を利用して、マウス抗体の可変領域や抗原との結合に直接関わる抗原結合部位
(CDR)を残し、他の部分をヒト抗体に置換したキメラ抗体やヒト化抗体を作製する技術が確立。
1990年代以降には、ファージ提示法を用いたヒト抗体ライブラリー技術、ヒト抗体遺伝子座をマウ
ス染色体に移入したヒト抗体産生トランスジェニックマウスを利用した抗体作製技術が確立され、
免疫原性の問題が回避できるようになり、抗体の医薬品への応用が急速に加速する。
過去10年間で抗体医薬品の承認数は急速に伸び、2012年末までに日欧米で承認された抗体医薬品は、
マウス/ラット抗体5種、キメラ抗体6種類、ヒト化抗体16種類、ヒト抗体9種類を含む合計36品
目に達している。マウス抗体では80%の高頻度で免疫原性が確認されていたが、キメラ抗体では改
善がみられ、ヒト化抗体、ヒト抗体では15%以下まで低減されており両者はほとんど差異のないこ
とが報告されている。
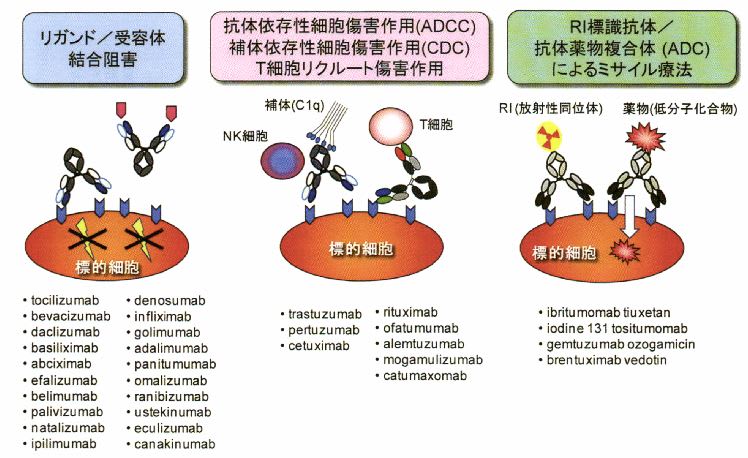
図 抗体医療品の作用メカニズム
抗体医薬品が有する作用機序を上図にまとめると、最も多い作用機序は 上図右のリガンド(=免
疫原性)と受容体の結合や受容体からのシグナル伝達を阻害する作用。がん治療用抗体の中で、こ
の作用機序を有するものがBevacizumab、Cetuximab、Panitumumab、Trastuzumabであり、免疫炎症
領域ではすべての抗体医薬品がこの作用機序で効果を示す。Bevacizumabは、血管新生に関与する
血管内皮細胞増殖因子(VEGF)に結合してその作用を阻害する抗体で、がん組織への血管形成を妨げ
ることにより、栄養供給を断ってがん細胞を傷害する。Bevacizumabは多くの種類のがんに対して
有効であると考えられており、米国では結腸・直腸がんや非小細胞肺がん、HER2陰性の乳がんへの
適応が承認されている。また、現在も多種類のがん種に対して化学療法剤との併用による臨床試験
が行われている。
CetuximabとPanjtumumabは上皮性増殖因子(EGF)の受容体を標的とする抗体であり、EGFによる増殖
シグナルを遮断してがん細胞の増殖を抑制する抗体であり、治癒切除不能な進行・再発の結腸・直
腸がんに対して承認されている。Trastuzumabは標的分子であるEGF受容体ファミリーの1つである
HER2を過剰発現する転移性乳がんの治療薬である。HER2に結合することにより増殖シグナルを遮断
するという作用のほかに、ADCCによりがん細胞を殺傷することが主な作用機序とされている。ADC
CやCDCは、がん治療用抗体に広く利用可能な作用機序である。これらの作用を有する抗体で、2010
年の医薬品売上でも上位に入るのが抗CD20抗体のRituximabである。Rituximab はOKT3に次ぎ1997年
に承認され、非ホジキンリンパ腫に対して著効を示したことから、リンパ腫の治療体系を変えた画
期的な薬剤の1つである。それ以降、CD20を標的とした抗体医薬が各社で開発されている。承認ま
たは臨床開発中の抗CD20抗体は19種類にも及んでいる。
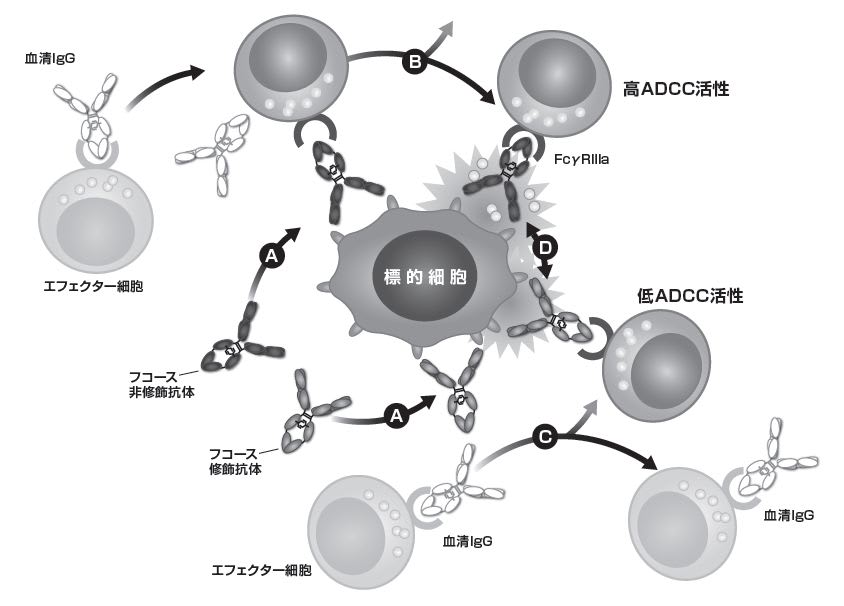

図 フコース非修飾抗体が高ADCC活性を発揮するメカニズム
ADCC を主な作用機序とするRituximabやOfatumumabに加え、放射性同位元素イットリウム90で標識
された抗CD20抗体であるいibritumomabtiuxetanやヨード131で標識された抗CD20抗体であるiodine-
131tositumomabが承認され、いわゆるミサイル療法としての抗体医薬品も実用化されてきた。
ibritumomab tiuxetan はRituximabに抵抗性の症例に対しても有効性が示されている。ミサイル療
法による抗体医薬品に関しては、細胞傷害活性を待つ低分子化合物を抗体に結合させたAntibody
Drug Conjugate (ADC)という分子形の開発が注目を浴びている。最初に承認されたADCは2000年に
上市されたGemutuzumab ozogamicinであり、Calicheamicinを結合した抗CD33抗体である。その後
の10年間は様々なADCが開発されたが、副作用が原因で承認には至っていない。これらADCの研究開
発から明らかになった課題は、標的抗原の発現量やがん細胞特異性および抗体結合後の細胞内移行
性、抗体と化合物を結合させるリンカーの設計で、申請中のTrastuzumab emtansine(T-DM1)は、
Trastuzumabにmaytansinoid cytotoxinを結合しがん細胞内に取り込まれた後にDM1を放出し
がん細胞を傷害するように設計されており、Trastuzumabで効果が弱かった患者群にも効果を示すこ
とが確認されている。また、2011年に承認されたBrentuximab Wdotin は、抗CD30抗体にMonomethy
lauristatin E(MMAE)を結合した新しいタイプのADCであり、この技術を保有するベンチャーのSeattle
Genetics社が関発した初めての抗体医薬品である。2011年にがん治療用抗体の1つが細胞傷害性T
リンパ球抗原(CTLA-4)に対する抗体lpilimumabである。通常、がん治療用抗体の標的と成り得る抗
原は、がん細胞特異的に発現する表面分子やがん細胞の増殖に関与する可溶性分子から選定された。
一方で、lpilimumabは免疫機能を抑制するCTLA-4の機能を阻害し、細胞傷害性T細胞の働きを高め
がん細胞を殺傷する新しいタイプのがん治療用抗体である。進行したメラノーマは治療選択肢が限
られている深刻な疾患であったが、lpilimumabは新しい作用機序により転移性メラノーマ患者の生
存期間の延長を示した最初の医薬品として注目されているという。
その他の疾患領域の抗体医薬品の中で、RSウイルス(呼吸器多核体ウイルス)のFタンパク質に対す
る抗体Palivizumabは比較的古く1998年に承認された医薬品である。RSウイルスは乳幼児に重症の
肺炎気管支炎を起こすウイルスで、通常は感染しても数週間で回復するが、先天的に呼吸器に疾患
を持つ乳幼児が感染すると重症化しやすい。そのため、感染抑制のため予防的に投与される。2012
年に炭疸菌の毒素に対する抗体RaxibacumabがFDAに承認された。バイオテロ対策という特殊な
事情から、臨床試験を実施せずに非臨床試験のみで承認された抗体医薬として話題になった。
現在、臨床試験が実施されている抗体医薬品の数が、2012年末時点で約400種類が報告されている
が、多くの開発品が同一抗原に集中しており、抗原ごとに開発品目を整理すると約150種類の抗体
医薬品は20種類の抗原に集中している。このように熾烈な開発競争が行われている状況下で価値の
高い抗体医薬品を創出して医療の発展に貢献するためには、有用な抗体創製技術を継続的に開発す
る必要があり、抗体の改良技術は可変領域の改良と定常領域の改良に分類することができる。可変
領域は主に抗原に対する結合特性に関与しているが、薬物動態や物理化学的性質にも影響を与える
ことから、可変領域を改変し性質を向上させることができる。定常領域は主にエフェクター機能と
薬物動態に関与し、様々なFc受容体に対する結合特性を制御することで、これらの性質を改良する
ことが可能である。なお、抗体医薬の改良ポイントは、①薬効増強・副作用低減、②利便性の向上、
③コスト低減の3つに大別できる。
さらに、①薬効増強・副作用低減として、(1)抗原体の結合親和性の制御(2)バイスペシフィ
ック抗体(3)エフェクター機能誘導活性の制御などからのアプローチが、また、②利便性の向上
のために、抗体医薬の低用量化や投与頻度の低減は、静脈内投与を皮下投与に切り替えることがで
き、また通院回数を減らすことにつながるため利便性の向上に寄与し、抗体医薬の投与量や投与頻
度は、抗原と抗体の体内動態により決定される。③コスト低減として
コスト低減の観点では、バイオ後続品(バイオシミラーとも呼ばれる)があり、先行バイオ医薬品の
特許が満了し、異なる製造販売業者により開発される同等のバイオ医薬品と定義されるがバイオ後
続品は、低分子医薬品の後発品(ジェネリック医薬品とも呼ばれる)と異なり、科学的に「同一」では
ないことから、異なる開発プロセスや要件が必要とされ、新薬開発と同様のフルパッケージの申請
データにより承認申請を行い、先行バイオ医薬品との比較から得られたデータに基づき、先行バイ
オ医薬品と同等/同質の品質、安全性、有効性を有する医薬品として開発できるが、フルパッケージ
の申請データが必要であることや、製造に関しての投資が高額となり低分子医薬品の場合のように
はに行かない。

この領域における技術革新は日進月歩で、一般的なIgG分子に関する改良技術は成熟しつつある。た
だ、技術がますます成熟し普遍化すると、技術による差別化ができず、近い将来に開発される抗体
医薬品は、フォロワーの余地を残さない完成度の高いものがいきなり市場に投入されると考えられ
るが、完成度の高いもの、抗体分子の特性を熟知し、常に最先端の技術とノウハウを確保し、独自の
技術を磨く必要がある。抗体分子の複雑さや生体機能の複雑さから一朝一タに獲得できるものでは
ない。成功の最大の鍵は、良い標的抗原の選択と、それに対する抗体にどのような機能を付与する
か、それらの組み合わせる独自アイデアが前提になる。標的抗原と病態との関連を深く知る医学・
薬学の、抗体分子の限界と可能性を熟知した抗体創薬の研究者の密接な連携の重要性が指定されて
いる。
慌ただしく、新しい情報に食らいつく習性は個性といえばそうなんだろうが、専門用語が続出する
医療・薬学用語は、経験からすると役立つ確率が低いが、その後役に立ったことがあった(微量成
分自動測定器や廃液の生物処理装置などの開発)。そんなことを考えながら、“進化は自然な生き
る証”なんだと自嘲気味に腑に落すと同時に「オールバイオマスシステム構想」(エネルギー環境)
が浮かんできた。これは早くまとめなくちゃと...。





























※コメント投稿者のブログIDはブログ作成者のみに通知されます