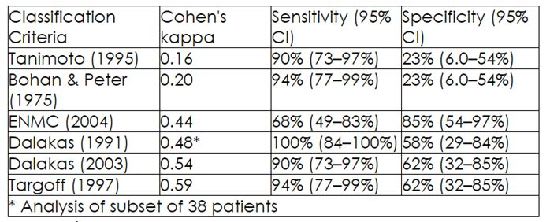
前回の続きで、皮膚筋炎などの特発性炎症性筋疾患の診断についてです。各診断基準の感度特異度比較もなされています。より初期の判定基準、すなわち Bohan Peterや谷本基準(指定難病の基準でもある)は感度はいいものの特異度が相当低く、疾患拾い上げには良くても確定にはならないことがわかる。2004年の欧州神経筋センター(ENMC)基準が、臨床基準、CK上昇、MSAやMRI所見を含む他の検査基準、及びより詳細な筋生検基準に基づいており特異度が増しているが、その分感度が減少した。病理学的PMパターンは特異的と思われるがそれでも模倣疾患があり注意が必要である。この前の日本リウマチ学会のシンポジウムでもIIMの診断について発表されてましたが、いま国際筋炎分類基準プロジェクト(IMCCP)にて診断基準が開発されているとのことです。
7.ENMC
・2004年に国際的な専門家のグループがオランダのNaardenで会合し、臨床研究/試験に使用するため、IBM、PM、DM、非特異性筋炎および免疫介在性壊死性ミオパチーを区別するため筋肉研究会/欧州神経筋センター(MSG/ ENMC)により新しい診断および分類基準が提案された。[Neuromuscul Disord 2004; 14: pp. 337-345]
・(IBMを除く)特発性炎症性筋疾患のための分類基準コンポーネントはAmatoによって提案され、MSG/ENMCワークショップによって承認された。
1.臨床基準
試験対象基準: a)18歳以上(DMおよび非特異的筋炎では幼児期でもよい)、b)亜急性または潜行性発症、c)筋力低下パターン(対称性近位>遠位、頸部屈筋>頸部伸筋)、d)DM典型的発疹(ヘリオトロープ、Gottron丘疹、Gottronサイン、手指や他関節骨隆起部の鱗屑状皮疹、Vサインとショールサイン)
除外基準: a)IBMの臨床的特徴 (see Griggs et al. Ann Neurol 1995;38:705–13)(非対称性筋力低下、三角筋と同様な手/手指屈筋の筋力低下、股関節屈筋と同様な膝伸筋and /or足背屈筋の筋力低下)、b)眼脱力感、孤立性構音障害、頸部伸筋>頸部屈筋の筋力低下、c)中毒性ミオパチー、活動的内分泌性疾患(甲状腺機能亢進または機能低下、副甲状腺機能亢進)、アミロイド症、筋ジストロフィーまたは近位運動神経障害(例えば、SMA)の家族歴
2.血清クレアチンキナーゼ値高値
3.その他の検査基準
a)筋電図: 試験対象基準( i)細動電位の形態にて刺入時と自発活動の増加、陽性の鋭波、または複合的反復的な放電、ii)形態計測分析で、短期間、振幅低下、多相性MUAPsの存在)
除外基準( i)近位筋緊張性ジストロフィーまたは他のchannelopathyを示唆している筋緊張放電、ii)形態計測分析で主に長期間、大振幅のMUAPs、iii)MUAPsの補充パターンの減少、
b)MRI: 拡散やSTIR画像で筋組織内の斑状の増強信号(浮腫)
c)血清筋炎特異的抗体(MSA)の検出
4.筋生検および除外基準
a)筋内膜炎症性細胞浸潤(T細胞)は非壊死筋線維周囲へそして侵入する
b)筋内膜CD8 + T細胞は非壊死性筋線維の周囲へ移行するが侵入しない、または遍在性MHC-1発現
c)筋束周辺萎縮
d)小血管における膜侵襲複合体(MAC)沈着、または毛細血管密度減少、または、電子顕微鏡での内皮細胞における管状細網封入体、または筋周囲束状繊維上のMHC-1発現
e)血管周囲、筋周囲の炎症細胞浸潤
f)散在性筋内膜CD8+ T細胞浸潤、 明らかに筋線維周囲や侵入はない
g)優勢な異常な組織学的特徴として多くの壊死性筋線維。炎症細胞は血管周囲にないかわずか。筋周囲浸潤は明らかでない。電子顕微鏡での小血管又はpipestem毛細管のMAC沈着がみられるかもしれない、しかし内皮細胞における管状細網封入体は珍しいか明らかではない。
h)縁取り空胞rimmed vacuoles、赤色ぼろ線維ragged red fibres、シトクロムオキシダーゼ陰性繊維はIBMを疑わせる
i)非壊死線維の筋細胞膜上のMAC沈着。 免疫病理を伴う筋ジストロフィーの他の適応症
分類基準
・Definite PM : 1.発疹を除くすべての臨床基準、2.血清CK上昇、3.筋生検基準としてbを含み、そして、c,d,h,iを除外
・Probable PM : 1.発疹を除くすべての臨床基準、2.血清CK上昇、3.その他の検査条件(3の1)、4.筋生検基準はbを含み、かつ c,d,g,h,iを除外
・Definite DM : 1.すべての臨床基準、2. cを含む筋生検基準
・Probable DM : 1.すべての臨床基準、2.筋生検基準はdまたはe含む、または血清CK上昇、 またはその他の検査条件 (3の1)
・非特異的筋炎 : 1.発疹を除くすべての臨床基準、2.血清CK上昇、3.その他の検査条件(3の1)、4.筋生検基準はeまたはfを含み、他のすべてを除外
免疫介在性壊死性ミオパチー : 1.発疹を除くすべての臨床基準、2.血清CK上昇、3.その他の検査条件(3の1)、4.筋生検基準はgを含み、他のすべてを除外
・上記に詳述したようにこのシステムは、臨床基準、CK上昇、MSAやMRI所見を含む他の検査基準、及びより詳細な筋生検基準に基づいている。
・基準及び除外基準から構成され、その両方がIIM罹患に患者を分類するために満足されなければならない。
・これらの基準は、次のカテゴリを区別する: 1)封入体筋炎; 2)多発性筋炎; 3)皮膚筋炎; 4)非特異的筋炎( 非特異的筋周囲/血管周囲性浸潤を伴う、しかしPMやDMの診断所見のない患者)、5)免疫媒介性壊死性ミオパチー(非炎症性浸潤が存在しない場合)。
・この分類基準は、病因に基づいた診断を可能にし、従って、全ての場合において、組織病理学的調査を必要とすることを意図している。
・また、DMは4つのグループに細分される: 1) definite DM; 2) probable DM; 3) amyopathic DM ;4) possible DM sine dermatitis
・amyopathicの場合を除き、筋生検はDMの診断のために重要である。DMにおいてみられる組織学的異常の小血管周囲のC5b-9または補体のMAC沈着は、このhumorally媒介性微小血管障害が特に筋束外周にての毛細血管密度の減少につながる。これは、DMにかなり特徴であり、JDMにおいてときおりみられる筋線維の梗塞を説明することができる。MAC沈着は他のIIMからDMを区別するのに非常に高感度で特異的である。
・Bohan とPeter分類の出版以来、PMは発疹がなくまた他の筋神経疾患を持たない患者における排他的な診断として定義されてきた。 PMの存在が問題視されたこともあったが、その後の研究で患者の大部分(63%)でPMの組織学的に明白な知見を伴う明確な臨床実体としてそれが確認されている。ENMCの改訂分類基準は、最近のPM免疫病原性の理解の進歩を考慮にして進められた。
・筋生検は、PMの確認のためにだけでなく、IBM やさらに筋ジストロフィー、酸性マルターゼ欠損症、およびNMなどの模倣性疾患の除外のためにも重要である。
・PMが筋線維に向けたHLA拘束性細胞媒介細胞傷害性免疫応答の結果であるため、PMの組織学的特徴はDMで見られるものとは異なる。
・いわゆる 筋炎特異的自己抗体(MSA)に関しては、それはその存在が事実上IBMと筋ジストロフィーを除外することが強調されたが、その感度は20-25%のみである[Curr Opin Rheumatol. 2001; 13: 476–482]。 またそれらは炎症性筋疾患のない患者でも見られるように、これらの抗体は筋炎に“特異的ではない”。それらはまだ、より最新の免疫病理によって定義される炎症性筋疾患のサブタイプ(例えば、DM、PM、非特異性筋炎、または壊死性筋炎)に関して特異的であることが実証されていない。
・オーバーラップと腫瘍随伴DMは考慮されていない。
・臨床現場で使用するには複雑。
8.それぞれの分類基準の比較
・Linklaterらは特発性炎症性筋疾患(IIM)のための6つの既存の分類基準の性能を比較した。すなわち、Bohan Peter分類(1975)、Dalakas分類(1991)、谷本分類(1995)とTargoff分類(1997)、Dalakas分類(2003)、欧州神経筋センター基準(ENMC)分類(2004)。 [Clin Exp Rheumatol 2013; 31: pp. 767-769]
・PM、 DM、封入体筋炎(IBM)又は非炎症性ミオパシーの専門家の診断を受けた52人の患者が含まれた。
・陽性の診断として、'definite', 'probable' or 'mild/ early' ラベルを使用した。一方で陰性診断として' possible 'を使用した。
・専門医の診断との実質的な合意は、Dalakas(2003)で、 κ=0.69、感度77%、特異度99%で、 ENMCで κ=0.49、感度71%、特異度82%、で一致を示した。
・より初期の4つの判定基準、すなわち Bohan Peter、谷本、TargoffとDalakas(1991) はすべて高感度(>86%)持っていたが低特異度(
・このIIMのためのBohan Peterの非常に低い特異度は、93%の特異度を記録したオリジナルの論文[Arthritis Rheum 1980; 23; 581-90.]とは非常に対照的である。 この不一致の理由は、おそらくコントロールの選択においてにあり、オリジナルの研究では、対照として他のCTD、主に全身性硬化症および全身性エリテマトーデスの患者を使用していた。
・2009 ACR/ARHP Annual Scientific Meetingにて、特発性炎症性筋疾患の分類基準:承認基準の性能比較が行われた。
・ENMC分類が開発され、それ以前に公開された基準に比較してその性能を評価することを目的とした。ゴールドスタンダードとして専門コンサルタント診断を使用。
・専門コンサルタントの診断と分類の基準との間の合意は、Cohenのカッパ統計量を用いて測定した。 Cohenのカッパ値 0.41- 0.60 は 適度な合意を示す。
・Targoff基準は、専門家の診断と適度な合意があったが(Cohen's kappa 0.59)、他の基準はあまりなかった。
・Targoff基準の強みの1つは、診断を行うために疾患特異的所見(筋生検の陽性所見、DM皮膚所見、筋炎特異的抗体のいずれか)存在することを必要とすること。
Arthritis & Rheumatism, Volume 60, October 2009 Abstract Supplement
The 2009 ACR/ARHP Annual Scientific Meeting. Philadelphia October 16-21, 2009.
Classification Criteria For Idiopathic Inflammatory Myopathy: Comparison Of The Performance Of Accepted Criteria
9.とくに多発性筋炎の診断は慎重に
・ IBM除く特発性炎症性筋疾患の患者を診断するための臨床、検査室の適用性へのレトロスペクティブフォローアップ調査がなされた。 [Neurology.2003; 61: 316–321] 1977-1998年の間に筋炎の診断(亜急性の近位筋筋力低下、他の神経筋疾患の除外)の165人の患者にて、臨床検査、および組織病理学的基準に基づく初期診断は、PMは9例(5%)、DMは59例(36%; 54名は孤立性発症、3名は結合組織疾患[CTD] 関連、2名は悪性腫瘍関連)、不特定筋炎(筋周囲/血管周囲浸潤あり、PMまたはDMなし)は65例(39%; 38名は孤立性発症、26名はCTD関連、1名は悪性腫瘍関連)
・この研究における患者の大多数はBohan Peter基準に従ってPMと診断されていた(皮膚の特徴の欠如のため)。
・フォローアップ評価では、PMとされた9名のうち5名はS-IBMの所見を開発した。
・筋周囲/血管周囲浸潤所見があるがしかし PMの診断を許可されたであろう筋線維を囲む筋内膜浸潤炎症細胞がなく、DMの診断を許可されたであろう皮膚の変化またはperifascicular筋線維萎縮はなかったPMでもDMでもない例が97例あり(不特定筋炎とpossible筋炎)、これらの患者の四分の一は後に結合組織病(CTD)と診断された。19%はプレドニゾン応答性壊死性筋疾患を持っていた。
・このグループ内の組織病理学の違いを考慮して、このグループは、異なる免疫病原性の患者を含むと考えられた [Neurology.2003; 61: 288–290]。
・長期的研究によって提供された証拠は、 慎重な査定と長期的なフォローアップが行われた場合、純粋なPMの診断はほとんど確認されていないことを明らかにした。
・まだ公開されていないがMilisendaらのレトロスペクティブ研究で15年間の診断的PMパターンを持つすべての筋生検例を再評価した。 合計1290生検のうち46でPMパターンを見いだした。筋生検の時点で、36人の患者で他の疾患に関連したPM、残り10人の患者ではPM単独として分類されていた。しかし再評価後とフォローアップでは1人の患者のみでこの診断が残った。主な最終的な診断は、結合組織病(CTD)(36%)とSIBM(28%)だった。[J Autoimmun. 2014 Feb-Mar;48-49:118-21.]
・組織病理学はPMを決定するための最も効果的な検査法と考えられているが、それは機会的であり決定的ではない。PMとs-IBMの診断において筋生検は患者の85%近くで信頼性の高い測定法であるが、残り15%における診断のエラーは 臨床と病理所見の総合評価によって回避又は低減できる。これは医師により患者全体像を作ることが重要である。
表・臨床的および病理学的PMパターンを模倣することができる状態または疾患
筋毒性薬剤、特にペニシラミン、ジドブジンおよびスタチンへの曝露
内分泌疾患(甲状腺機能亢進症、機能低下症、副甲状腺機能亢進症、機能低下症)
神経性疾患(神経学的検査と筋電図によって除外)
筋ジストロフィーと代謝性ミオパチー(病歴と筋生検により除外)
封入体筋炎(臨床試験と筋生検により除外)
免疫介在性壊死性ミオパチー(筋生検により除外)
感染症:ウイルス(HIV、HTLV-1、HCV)、寄生虫(旋毛虫、サルコシスチス)
10.新たな方向性 IMCCP
・特発性炎症性筋疾患(IIM)のための分類基準が、成人および小児のリウマチ専門医、皮膚科、神経科医、疫学および生物統計学者を備え、国際·学際的共同研究、 国際筋炎分類基準プロジェクト(IMCCP)にて開発された。
・開発された分類基準(web計算を参照)は筋生検データの有無にかかわらず使用され、IIMを有する確率を提供する。
・確率モデル : 各項目および得点
最初の症状の発症の18≤年齢
最初の症状≥40の発症年齢 2.3
臨床筋項目
客観的な対称性筋力低下、近位上肢、通常進行性 0.7
客観的な対称性筋力低下、近位下肢、通常進行性 0.6
頸部屈筋が頸部伸筋に比べ相対的筋力低下 1.6
下肢近位筋が遠位筋よりも相対的筋力低下 1.5
皮膚項目
ヘリオトロープ疹 3.3
Gottron丘疹 2.3
Gottronサイン 3.4
その他の臨床的項目
嚥下障害または食道運動障害 0.7
検査項目
血清クレアチンキナーゼ活性(CK) 1.2
血清乳酸脱水素酵素(LDH)活性または血清アスパラギン酸アミノトランスフェラーゼ(ASAT / AST / SGOT)活性または血清アラニンアミノトランスフェラーゼ(ALAT / ALT / SGPT)活性
抗Jo-1(抗His)抗体陽性 4.2
上記の項目からスコアを合計 0.9
(筋生検が利用可能な場合、他のすべての変数のスコア合計を 0.9によって乗算し、その後陽性の生検のスコアを加える)
筋生検項目
単核細胞の筋内膜浸潤所見、筋線維を取り囲むが、侵入しない 1.4
単核細胞の筋周囲および/または血管周囲浸潤所見 1.2
筋束傍萎縮所見 1.6
縁取り空砲所見 2.2
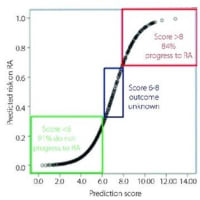
・IIMの分類は、事前に決定確率のカットオフに基づいており、それは≥50%にする必要がある。 また筋炎における臨床試験における選択基準については、このカットオフは≥90%する必要がある。 得られた各確率は、独自の感度と特異度に対応している。
・患者はIIMを有すると分類された後に、IIMのサブ分類を行う。これは、ヘリオトロープ、ゴットロン丘疹またはゴットロンサインの皮膚所見、筋力低下パターン、筋生検所見の有無による 分類ツリーに基づいてる
:多発性筋炎、免疫介在性壊死性ミオパチー、封入体筋炎、amyopathic DM、皮膚筋炎、若年性皮膚筋炎。
参考文献
J Autoimmun. 2014 Feb-Mar;48-49:118-21.
J Autoimmun. 2014 Feb-Mar;48-49:122-7.
Clin Exp Rheumatol. 2013 Sep-Oct;31(5):767-9.
Neuromuscul Disord. 2004 May;14(5):337-45.


















わかりやすくて とてもありがたいです。