
![]()
彦根藩二代当主である井伊直孝公をお寺の門前で手招き雷雨から救ったと伝
えられる"招き猫"と、井伊軍団のシンボルとも言える赤備え。(戦国時代の
軍団編成の一種で、あらゆる武具を朱塗りにした部隊編のこと)の兜(かぶ
と)を合体させて生まれたキャラクタ
【再エネ革命渦論 186 アフターコロナ時代 185】
● 技術的特異点でエンドレス・サーフィング
特異点真っ直中 ㊿+⑰

図1. NTTグループ温室効果ガス排出量の削減イメージ(国内+海外)
● 人工光合成時代に突入?!
10月27日、日本電信電話(NTT)は,太陽光エネルギーを利用する半導体光
触媒と二酸化炭素(CO2)を還元する金属触媒を電極として組み合わせた人
工光合成デバイスを作製し,世界最長の350時間連続炭素固定を実現。人工
光合成はこれまでに世界中で様々な研究が進められており,特に高いCO2変
換効率を実現できる触媒に関する検討が盛んに行なわれている。
一方で,連続したCO2変換の試験時間は数時間から数十時間レベルに留まっ
ており,長時間化に向けた劣化抑制の技術確立が課題となっていた。 同社
では,長時間連続して気相中のCO2をより効率的に変換可能な人工光合成の
実現をめざし,光をエネルギーとして利用するための長寿命な半導体光触媒
電極と,気相のCO2を高効率に変換するために電解質膜と一体化した繊維状
の金属触媒電極により構成した人工光合成デバイスを設計した。半導体光触
媒として用いている窒化ガリウム(GaN)系電極は,GaN表面と水溶液の界面
で生じる劣化反応の抑制が課題だった。そこで,GaN表面の凹凸をより滑ら
かにし,光を十分に透過する厚さ2nmの}均一な酸化ニッケル(NiO)薄膜を
保護層として形成することでGaNと水溶液の接触を防ぎ,電極の劣化を大幅
に抑制することに成功。 また,従来の水溶液中に溶存しているCO2を変換す
る金属電極は板状の構造が主流だが,今回,気相のCO2を変換するために,C
O2拡散性の高い繊維状金属とCO2変換反応に必要なプロトン(H+)を反応場に
供給する役割を持つ電解質膜を一体化した電極構造を考案。 これにより水
溶液中に電極を浸漬させることなくCO2変換反応に必要なプロトン(H+)を反
応場に供給できるようになり,気相のCO2を直接変換することを可能にした。
これらの電極構造の工夫により,従来に比べ10倍以上のCO2変換効率を実現
した。 この人工光合成デバイスに疑似太陽光を照射し,気相のCO2変換試験
行なった結果,350時間連続してCO2がCOやHCOOHに変換されたことを確認し
た。生成したCOやHCOOHから算出した単位面積当たりの累積炭素固定量は420
g/m2に達し,半導体光触媒を用いた人工光合成において世界最長の350時間
連続動作を実現した。この検証による炭素固定量は,樹木(スギ)の木1本
が1m2当たり約1年間で固定するCO2を上回る量に相当するという。
【要点】
1.半導体光触媒電極の劣化反応抑制技術:半導体光触媒として用いている
窒化ガリウム(GaN)系電極は、GaN表面と水溶液の界面で生じる劣化反応
の抑制が課題でした。そこで、GaN表面の凹凸をより滑らかにし、光を十分
に透過する厚さ2nmの均一な酸化ニッケル(NiO)薄膜を保護層として形成
することでGaNと水溶液の接触を防ぎ(図2a)、電極の劣化を大幅に抑制
することに成功。
2.従来の水溶液中に溶存しているCO2を変換する金属: 電極は板状の構造
が主流ですが、今回、気相のCO2を変換するために、CO2拡散性の高い繊維
状金属とCO2変換反応に必要なプロトン(H+)を反応場に供給する役割を持
つ電解質膜(※14)を一体化した電極構造を考案しました(図2b、左) 。
これにより水溶液中に電極を浸漬させることなくCO2変換反応に必要なプロト
ン(H+)を反応場に供給できるようになり、気相のCO2を直接変換することを
可能にしました。これらの電極構造の工夫により、従来に比べ10倍以上のCO2
変換効率を実現した。 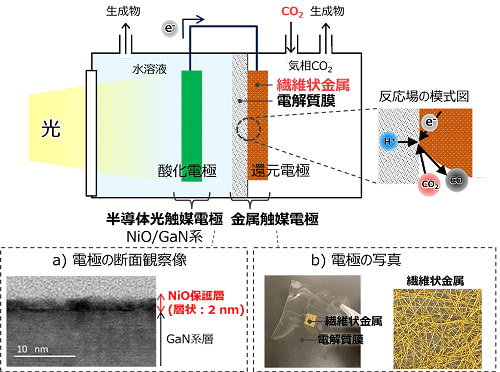

図2.人工光合成デバイスの概略図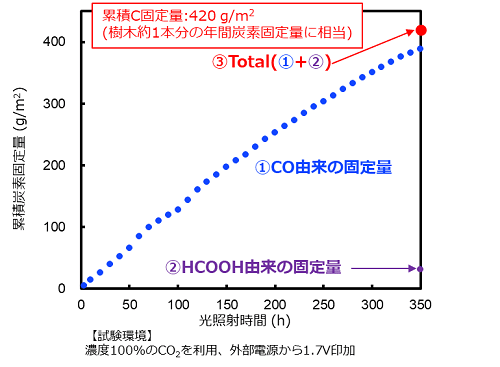
図3. 光照射時間に対する炭素固定量の変化【概要】
【展望】
<研究グループは,今後,より高性能な人工光合成反応を実現するために,
電極での反応の更なる高効率化,電極の長寿命化およびこれらの両立をめざ
す。
[関連特許]
特許7356067 二酸化炭素の気相還元装置、および、二酸化炭素の気相還元方法
[概要】
光触媒からなる酸化電極への光照射により、水の酸化反応と二酸化炭素の還
元反応を進行させる技術を人工光合成という。また、金属からなる酸化電極
と還元電極の間への電圧印加により、水の酸化反応と二酸化炭素の還元反応
を進行させる技術を二酸化炭素の電解還元という。太陽光を利用した人工光
合成技術や、再生可能エネルギー由来の電力を利用した電解還元技術は、二
酸化炭素を一酸化炭素、ギ酸、エチレン等の炭化水素やメタノール、エタノ
ール等のアルコールに再資源化することが可能な技術として注目され、近年
盛んに研究されている。従来、非特許文献1、2にあるように、人工光合成
技術や二酸化炭素の電解還元技術では、還元電極(Cu)を水溶液中に浸漬
させ、その水溶液中に溶解させた二酸化炭素(CO2)を当該還元電極に供
給し、還元する反応系が用いられてきた(非特許文献1の図2参照)。しかし、
この二酸化炭素の還元方法では、水溶液への二酸化炭素の溶解濃度や水溶液
中での二酸化炭素の拡散係数に限界があるため、還元電極への二酸化炭素の
供給量が制限されるという問題がある。
この問題に対し、還元電極への二酸化炭素の供給量を増加させるため、還元
電極に対して気相の二酸化炭素を供給する研究が進められている。非特許文
献3の図1に示された二酸化炭素の気相還元装置では、還元電極に対して気
相の二酸化炭素を供給できる構造を有する反応装置を用いることで、還元電
極への二酸化炭素の供給量が増大し、二酸化炭素の還元反応が促進する。
【非特許文献】
1.Satoshi Yotsuhashi、外6名、“CO2Conversion with Light and Water by GaN Pho-
toelectrode”、Japanese Journal of Applied Physics、51、2012年、p.02BP07-1-p.02B-
P07-3
2.Yoshio Hori、外2名、“Formation of Hydrocarbons in the Electrochemical Reduction
of Carbone Dioxide at a Copper Electrode in Aqueous Solution”、Journal of the Chemical
Society、85(8)、1989年、p.2309-p.2326
3.Ichitaro Waki、外2名、”Direct Gas-phase CO2 Reduction for Solar Methane Gener-
ation Using a Gas Diffusion Electrode with a BiVO4:Mo and a Cu-In-Se Photoanode”、
Chemistry Letter、47、2018年1月13日、p.436-p.439
(【特許請求の範囲】
【請求項1】 酸化電極を含む酸化槽と、 二酸化炭素が供給される還元槽と、
イオン交換膜と還元電極とを積層したガス還元シートであり、前記イオン交
換膜を前記酸化槽に向け、前記還元電極を前記還元槽に向けて、前記酸化槽
と前記還元槽との間に配置されたガス還元シートと、 前記酸化電極と前記
還元電極とを接続する導線と、 前記還元槽を囲む熱源と、を備え、 前記酸
化電極に光を照射する光源、又は、前記酸化電極と前記還元電極との間に電
圧を印加する電源を備える二酸化炭素の気相還元装置。
【請求項2】 前記酸化電極は、 n型半導体である請求項1に記載の二酸化
炭素の気相還元装置。
【請求項3】 前記還元槽を囲む熱伝導性板及び断熱材を更に備える請求項1
又は2に記載の二酸化炭素の気相還元装置。
【請求項4】 二酸化炭素の気相還元装置で行う二酸化炭素の気相還元方法に
おいて、 前記二酸化炭素の気相還元装置は、 酸化電極を含む酸化槽と、 二
酸化炭素が供給される還元槽と、 イオン交換膜と還元電極とを積層したガス
還元シートであり、前記イオン交換膜を前記酸化槽に向け、前記還元電極を
前記還元槽に向けて、前記酸化槽と前記還元槽との間に配置されたガス還元
シートと、 前記酸化電極と前記還元電極とを接続する導線と、 前記還元槽
を囲む熱源と、を備え、 前記酸化槽に電解液を注水する第1の工程と、 前
記還元槽に熱を加える第2の工程と、 前記還元槽に前記二酸化炭素を流入す
る第3の工程と、 前記酸化電極に光を照射し、又は、前記酸化電極と前記還
元電極との間に電圧を印加する第4の工程と、 を行う二酸化炭素の気相還元
方法。
【請求項5】 前記第2の工程では、 前記還元電極の表面で起きた前記二酸
化炭素の還元反応により前記還元電極の表面に生成される液体の沸点よりも
高い温度の熱を加える請求項4に記載の二酸化炭素の気相還元方法。
【発明の概要】
しかしながら、非特許文献3に開示された二酸化炭素の気相還元装置では、
以下の式(1)-(4)に示すような二酸化炭素の還元反応が進行すると、
還元電極では水(H2O)、ギ酸(HCOOH)、メタノール(CH3OH)、
エタノール(C2H5OH)等の液体生成物が生成され、その液体生成物が
還元電極の表面に付着してしまう。そのため、還元電極の表面に対して気相
の二酸化炭素を直接供給できなくなり、二酸化炭素の供給量が減少すること
で二酸化炭素の還元反応の寿命が低下してしまう。
CO2+2H++2e-→CO+H2O ・・・(1)
CO2+2H++2e-→HCOOH ・・・(2)
CO2+6H++6e-→CH3OH+H2O ・・・(3)
2CO2+12H++12e-→C2H5OH+3H2O ・・・(4)
従って、二酸化炭素の還元反応により還元電極の表面に生成する液体生成物
を除去して還元電極に対して常に気相の二酸化炭素を直接供給することで、二
酸化炭素の供給量を維持し、二酸化炭素還元反応の寿命を向上させることが
課題である。
また、液体生成物が還元電極に付着していると、液体生成物を回収するため
に一度還元槽を開放する必要があり、その作業を行う間装置の運転が停止さ
れる。したがって、装置を停止させることなく、液体生成物を簡便に回収す
ることが課題である。
本発明は、上記事情に鑑みてなされたものであり、本発明の目的は、二酸化炭
素の気相還元装置において、二酸化炭素の還元反応の寿命を改善し、還元電
極に付着した液体生成物を簡便に回収可能な技術を提供することである。
【課題を解決するための手段】
本発明の一態様の二酸化炭素の気相還元装置は、酸化電極を含む酸化槽と、
二酸化炭素が供給される還元槽と、イオン交換膜と還元電極とを積層したガ
ス還元シートであり、前記イオン交換膜を前記酸化槽に向け、前記還元電極
を前記還元槽に向けて、前記酸化槽と前記還元槽との間に配置されたガス還
元シートと、前記酸化電極と前記還元電極とを接続する導線と、前記還元槽
を囲む熱源と、を備え、前記酸化電極に光を照射する光源、又は、前記酸化
電極と前記還元電極との間に電圧を印加する電源を備える。 本発明の一態様
の二酸化炭素の気相還元方法は、二酸化炭素の気相還元装置で行う二酸化炭
素の気相還元方法において、前記二酸化炭素の気相還元装置は、酸化電極を
含む酸化槽と、二酸化炭素が供給される還元槽と、イオン交換膜と還元電極
とを積層したガス還元シートであり、前記イオン交換膜を前記酸化槽に向け、
前記還元電極を前記還元槽に向けて、前記酸化槽と前記還元槽との間に配置
されたガス還元シートと、前記酸化電極と前記還元電極とを接続する導線と、
前記還元槽を囲む熱源と、を備え、前記酸化槽に電解液を注水する第1の工
程と、前記還元槽に熱を加える第2の工程と、前記還元槽に前記二酸化炭素
を流入する第3の工程と、前記酸化電極に光を照射し、又は、前記酸化電極
と前記還元電極との間に電圧を印加する第4の工程と、を行う。 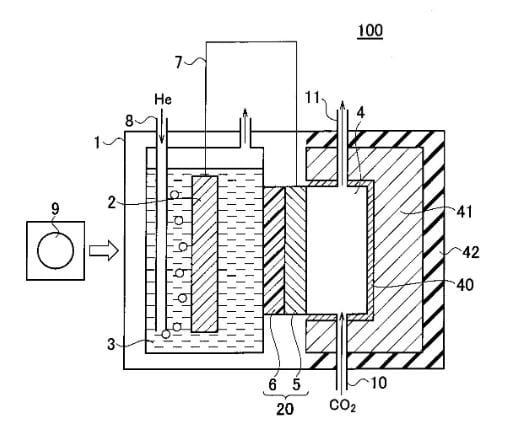
図1.実施例1~4に係る二酸化炭素の気相還元装置の構成を示す構成図
【符号の説明】 1:酸化槽 2:酸化電極 3:水溶液 4:還元槽 5:還元
電極 6:イオン交換膜 7:導線 8:チューブ 9:光源 10:気体入力口
11:気体出力口 12:電源 20:ガス還元シート 40:熱伝導性板 41
:熱源 42:断熱材 51:槽 52:槽 71:めっき液 72:還元剤
100:二酸化炭素の気相還元装置
【発明の効果】
本発明によれば、二酸化炭素の気相還元装置において、二酸化炭素の還元反
応の寿命を向上し、還元電極に付着した液体生成物を簡便に回収可能な技術
を提供できる。
【図面の簡単な説明】
【図1】実施例1~4に係る二酸化炭素の気相還元装置の構成を示す構成図
【図2】無電解めっき法を用いたガス還元シートの作製方法を示す図
【図3】実施例5~8に係る二酸化炭素の気相還元装置の構成を示す構成図
【図4】従来の二酸化炭素の気相還元装置の構成を示す構成図
【図5】従来の二酸化炭素の気相還元装置の構成を示す構成図
【発明を実施するための形態】
以下、図面を参照して発明の実施形態を説明する。図面の記載において同一
部分には同一の符号を付し説明を省略する。本発明は、下記実施例に限定さ
れるものではなく、その要旨の範囲内で数々の変形が可能である。
[発明の概要]
本発明は、光照射による二酸化炭素の還元反応を引き起こし、又は、二酸化
炭素の電解還元反応を引き起こし、当該還元反応の効率を向上させる二酸化
炭素の気相還元装置に関する発明であり、燃料生成技術や太陽エネルギー変
換技術の技術分野に属する。
本発明は、イオン交換膜上に還元電極を形成して得られるガス還元シートを
用いて、還元電極の表面に気相の二酸化炭素を直接供給して還元する。この
とき、二酸化炭素の還元反応により還元電極の表面に液体生成物が生成する
が、本発明では、還元槽の周りに熱源を配置し、その熱源によって還元電極
の温度を液体生成物の沸点以上又は沸点よりも高い温度に維持することで、
液体生成物を気化させて除去する。
これにより、還元電極の表面に生成される液体生成物を除去可能となり、常
に気相の二酸化炭素を還元電極に直接供給可能となることから、二酸化炭素
の還元反応の寿命を向上させることができる。また、液体生成物を気化させ
るので、液体生成物の回収が簡便になる。
[実施例1]
[二酸化炭素の気相還元装置の構成]
図1は、実施例1に係る二酸化炭素の気相還元装置の構成を示す構成図であ
る。二酸化炭素の気相還元装置100は、酸化電極2を含む酸化槽1と、二
酸化炭素が供給される還元槽4と、イオン交換膜6と還元電極5とを積層し
たガス還元シート20であり、イオン交換膜6を酸化槽1に向け、還元電極
5を還元槽4に向けて、酸化槽1と還元槽4との間に配置されたガス還元シ
ート20と、酸化電極2と還元電極5とを接続する導線7と、還元槽4を囲
む熱伝導性板40、熱源41、断熱材42と、酸化電極2に光を照射する光
源9と、を備える。 酸化槽1には、電解液である水溶液3が注水される。酸
化槽1内の酸化電極2は、酸化槽1内に注入された水溶液3に浸漬される。
実施例1の酸化電極2は、半導体又は金属錯体からなる電極であり、例えば、
窒化物半導体である。実施例1の酸化電極2は、異なる種類の窒化物半導体
を積層した積層構造でもよく、インジウムやアルミニウムを含むような異な
る組成で構成してもよい。実施例1の酸化電極2は、窒化物半導体の代わり
に、酸化チタン、アモルファスシリコンのような光活性を示す化合物を用い
てもよい。 水溶液3は、酸化槽1に注水される電解液である。
水溶液3は、例えば、水酸化カリウム水溶液である。水溶液3は、水酸化カ
リウム水溶液の代わりに、例えば、水酸化ナトリウム水溶液、塩化カリウム
水溶液、塩化ナトリウム水溶液等を用いてもよい。
ガス還元シート20は、イオン交換膜6と還元電極5とを積層した構造を備
える。イオン交換膜6は、例えば、炭素-フッ素からなる骨格を持つ電解質
膜であるナフィオン(商標登録)、フォアブルーSシリーズ、アクイヴィオ
ン等である。還元電極5は、例えば、銅である。還元電極5は、銅の代わり
に、金、白金、銀、パラジウム、ガリウム、インジウム、ニッケル、スズ、
カドニウム、それらの合金でもよく、それらの金属及び金属酸化物とカーボ
ンとの混合物質でもよい。還元電極5は、導線7で酸化電極2に接続される。
このガス還元シート20は、酸化槽1と還元槽4との間に配置され、イオン
交換膜6は酸化槽1に向けて配置され、還元電極5は還元槽4に向けて配置
される。
光源9は、二酸化炭素の気相還元装置100を運転するための光源であり、
酸化電極2に対して対向配置される。光源9は、例えば、キセノンランプ、
擬似太陽光源、ハロゲンランプ、水銀ランプ、太陽光、これらの組み合わせ
等である。
[ガス還元シートの作製方法] 図2は、ガス還元シート20を作製する方
法として用いた無電解めっき法の反応系を示す図である。イオン交換膜6に
はナフィオンを用い、還元電極5には銅を用いた。イオン交換膜6の片面を
研磨し、イオン交換膜6を沸騰硝酸と沸騰純水とにそれぞれ漬け込む。左右
2つの槽51,52に、表1に示すめっき液71と還元剤72とをそれぞれ
満たす。 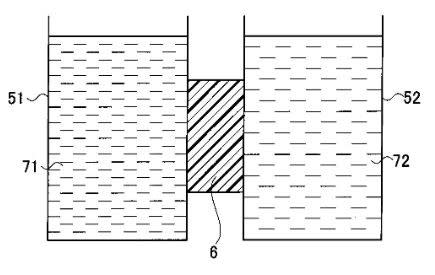 図2.
図2.
槽51と槽52とは、イオン交換膜6によって隔てられている。イオン交換
膜6は、研磨面をめっき液71側にして配置する。めっき液71とイオン交
換膜6の研磨面との界面において、下記の酸化還元反応が起きて銅(Cu)
が析出することで、イオン交換膜6上に還元電極5が形成されたガス還元シ
ート20が得られる。
BH4-+4OH-BO2-+2H2O+2H2+4e-
Cu2+2e-→Cu
尚、ガス還元シート20の作製方法は、無電解めっき法以外に、例えば、電
気めっき法、物理蒸着法、化学蒸着法等でもよい。
[二酸化炭素の気相還元方法] 次に、二酸化炭素の気相還元装置100で
行う二酸化炭素の気相還元方法について説明する。電気化学測定結果、ガス・
液体生成量測定結果も併せて説明する。
第1の工程; まず、酸化槽1に電解液である水溶液3を注水し、その水溶
液3に酸化電極2を浸水させる。酸化電極2には、サファイア基板上にn型
半導体であるn型窒化ガリウム(n-GaN)の薄膜と窒化アルミニウムガ
リウム(AlGaN)とをその順にエピタキシャル成長させ、その上にニッ
ケル(Ni)を真空蒸着して熱処理を行うことで酸化ニッケル(NiO)の
助触媒薄膜を形成した基板を用いた。水溶液3は、1mol/Lの水酸化カ
リウム(KOH)水溶液とした。酸化電極2の光照射面積(受光面積)は
2. 5cm2とした。
第2の工程; 次に、半導体光電極として機能する酸化電極2の酸化助触媒
形成面が照射面となるように光源9を固定する。光源9には、300Wの高
圧キセノンランプ(波長450nm以上をカット、照度6.6mW/cm2
)を用いた。
第3の工程; 次に、還元槽4の周囲を熱伝導性板40で囲い、その熱伝導
性板40の周囲に熱源41を配置し、更に熱源41の周囲を断熱材42で囲
う。熱効率を高めるため、それぞれは密着させることが好ましい。熱伝導性
板40には、銅板を用いた。熱源41には、ラバーヒーターを用いた。断熱
材42には、硬質ウレタンフォームを用いた。そして、還元電極5の表面近
傍温度が60℃となるように熱源41で還元槽4を加熱する。尚、還元電極
5の表面近傍温度は、例えば熱電対を用いて測定可能である。
第4の工程; 次に、酸化槽1に対してはチューブ8からヘリウム(He)
を、還元槽4に対しては気体入力口10から二酸化炭素(CO2)を、それ
ぞれ流量5ml/minかつ圧力0.18MPaで流入する。酸化槽1に
流入する気体は、アルゴン、窒素、二酸化炭素等の不活性ガスでもよい。
第5の工程; 次に、酸化槽1と還元槽4とをヘリウムと二酸化炭素とでそ
れぞれ十分に置換した後、光源9を用いて酸化電極2に均一に光を照射する。こ
の光照射により、酸化電極2と還元電極5との間に電気が流れる。酸化電極
2の表面では水の酸化反応が起こり、ガス還元シート20内の[イオン交換
膜6-還元電極5(銅)-気相の二酸化炭素]からなる三相界面では、二酸
化炭素の還元反応が進行する。このとき、還元電極5の表面には、水(H2
O)、ギ酸(HCOOH)、メタノール(CH3OH)、エタノール(C2
H5OH)等の液体生成物が付着するが、熱源41で還元槽4を加熱している
ため、付着した液体生成物は気化して還元電極5の表面から除去され、気相
の二酸化炭素と気化した液体生成物との混合気体が気体出力口11から流出
する。
第6の工程; 最後に、光照射中の任意の時刻に酸化槽1及び還元槽4の各
気体を採取し、ガスクロマトグラフ及びガスクロマトグラフ質量分析計にて
反応生成物を分析する。その反応生成物を分析した結果、酸化槽1内では、
水の酸化反応による酸素が生成され、還元槽4内では、プロトンの還元反応
による水素、及び、二酸化炭素の還元反応による一酸化炭素、ギ酸、メタン、
メタノール、エタノール、エチレンが生成していることを確認した。また、
光照射時の酸化電極2と還元電極5との間の電流値を、電気化学測定装置(
Solartron社製、1287型ポテンショガルバノスタット)を用いて測定した。
[実施例2]
実施例2では、還元電極5の表面近傍温度を100℃とした。これ以外の方
法及び二酸化炭素の気相還元装置100の構成は、実施例1と同様である。
[実施例3]
実施例3では、還元電極5の表面近傍温度を110℃とした。これ以外の方
法及び二酸化炭素の気相還元装置100の構成は、実施例1と同様である。
[実施例4] 実施例4では、還元電極5の表面近傍温度を130℃とした。
これ以外の方法及び二酸化炭素の気相還元装置100の構成は、実施例1と
同様である。 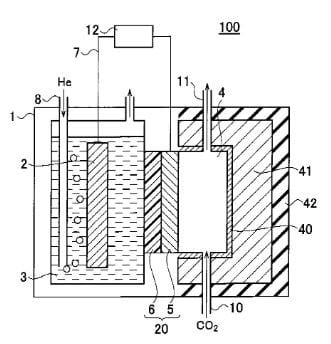 図3.
図3.
[実施例5]
[二酸化炭素の気相還元装置の構成]
図3は、実施例5に係る二酸化炭素の気相還元装置の構成を示す構成図であ
る。実施例5では、光源9の代わりに、電源12を用いる。電源12は、導
線7の経路上に挿入される。実施例5では酸化電極2で光を受光する必要が
ないので、実施例5の酸化電極2は、白金(ニラコ製)を用いて構成した。
実施例5の酸化電極2は、白金の代わりに、例えば、金、銀、銅、インジウ
ム、ニッケル等の金属でもよい。実施例5の酸化電極2の表面積は、約0.
55cm2とした。その他の構成は、実施例1と同様である。
[ガス還元シートの作製方法]
ガス還元シートの作製方法は、実施例1と同様である。
[二酸化炭素の気相還元方法]
第1の工程; まず、酸化槽1に電解液である水溶液3を注水し、その水溶
液3に酸化電極2(白金)を浸水させる。
第2の工程; 次に、還元槽4の周囲を熱伝導性板40で囲い、その熱伝導性
板40の周囲に熱源41を配置し、更に熱源41の周囲を断熱材42で囲う。
そして、還元電極5の表面近傍温度が60℃となるように熱源41で還元槽
4を加熱する。
第3の工程; 次に、酸化槽1に対してはチューブ8からヘリウム(He)を
還元槽4に対しては気体入力口10から二酸化炭素(CO2)を、それぞれ
流量5ml/minかつ圧力0.18MPaで流入する。
第4の工程; 次に、酸化槽1と還元槽4とをヘリウムと二酸化炭素とでそ
れぞれ十分に置換した後、酸化電極2と還元電極5との間に電源12を導線
7でつなぎ、電圧1.5Vを印加する。
第5の工程; 最後に、光照射中の任意の時刻に酸化槽1及び還元槽4の各気
体を採取し、ガスクロマトグラフ及びガスクロマトグラフ質量分析計にて反
応生成物を分析する。
[実施例6]
実施例6では、還元電極5の表面近傍温度を100℃とした。これ以外の方
法及び二酸化炭素の気相還元装置100の構成は、実施例5と同様である。
[実施例7]
実施例7では、還元電極5の表面近傍温度を110℃とした。これ以外の方
法及び二酸化炭素の気相還元装置100の構成は、実施例5と同様である。
[実施例8]
実施例8では、還元電極5の表面近傍温度を130℃とした。これ以外の方
法及び二酸化炭素の気相還元装置100の構成は、実施例5と同様である。
[実施例1-8の効果]
次に、実施例1-8の効果を説明する。ここでは、従来構成の効果と比較す
る。図4は、実施例1-4(図1)に対応する従来構成であり、比較対象例
1という。図5は、実施例5-8(図3)に対応する従来構成であり、比較
対象例2という。比較対象例1、2は、いずれも、還元槽4の周囲に、熱伝
導性板40、熱源41、断熱材42が配置されていない。 表2は、実施例
1-10及び比較対象例1、2に関して、光照射時又は電圧印加時から10
分後の二酸化炭素還元反応のファラデー効率を示す表である。 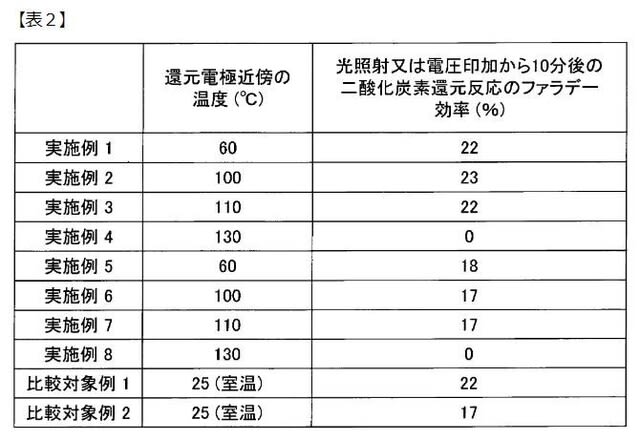
ファラデー効率とは、式(5)に示すように、光照射時又は電圧印加時に電
極間に流れた電流値に対して、各還元反応に使われた電流値の割合を示すも
のである。
各還元反応のファラデー効率=(各還元反応の電流値)/(酸化電極-
還元電極間の電流値) ・・・(5)
式(1)の「各還元反応の電流値」は、各還元生成物の生成量の測定値を、そ
の生成反応に必要な電子数に換算することで算出可能である。例えば、還元
反応生成物の濃度をA[ppm]、キャリアガスの流量をB[L/sec]
、還元反応に必要な電子数をZ[mol]、ファラデー定数をF[C/mo
l]、気体のモル体をVm[L/mol]としたとき、式(6)を用いて算
出可能である。
各還元反応の電流値[A]=(A×B×Z×F×10-6)/Vm ・(6)
表2より、実施例1-3と比較対象例1とのファラデー効率は同程度の値で
あり、実施例5-7と比較対象例2とのファラデー効率も同程度の値である。
これは、光照射時又は電圧印加時から10分後では還元電極5の表面に付着
する液体生成物が極微量であり、反応面が失われていないためと考えられる。
一方で、実施例4及び実施例8では、ファラデー効率が0%であった。これ
は、還元電極5の表面近傍温度が130℃と高いため、イオン交換膜を形成
するスルホン酸基が分解され、イオン交換膜がイオン交換機能を失ったこと
が原因と考えられる。
以上より、還元電極5の表面近傍温度は130℃未満であることが好ましい
と考えられる。
尚、イオン交換膜6の例として挙げたナフィオンやフォアブルーSシリーズ
の使用可能温度は110℃、アクイヴィオンの使用可能温度は140℃であ
り、この温度以下で使用する必要がある。
表3は、実施例1—3、5-7及び比較対象例1、2に関して、光照射時又は
電圧印加時から20時間後の二酸化炭素還元反応のファラデー効率の維持率
を示す表である。 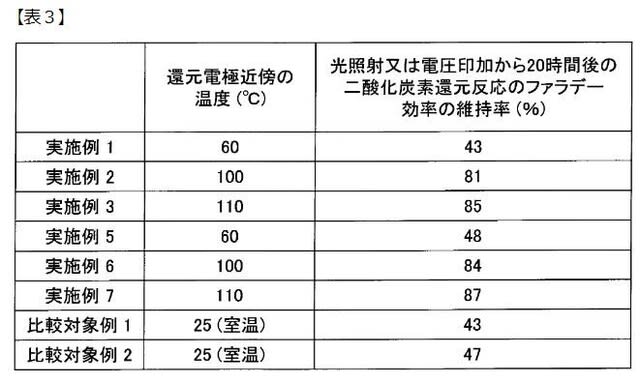
二酸化炭素還元反応のファラデー効率の維持率とは、式(7)に示すように、
10分後の二酸化炭素還元反応のファラデー効率に対する20時間後の二酸
化炭素還元反応のファラデー効率と定義した。
二酸化炭素還元反応のファラデー効率の維持率=(20時間後の二酸化炭素
還元反応のファラデー効率)/(10分後の二酸化炭素還元反応のファラデ
ー効率) ・・・(7)
上表3より、比較対象例1及び比較対象例2に対して、実施例2、3及び実
施例6、7は、それぞれ、二酸化炭素還元反応のファラデー効率の維持率が
向上しており、二酸化炭素還元反応の寿命が向上したことがわかる。これは、
実施例3及び実施例7において、還元電極5の表面近傍温度を110℃にす
ることで、還元電極5に付着した液体生成物である水(沸点100℃)、ギ
酸(沸点100.8℃)、メタノール(沸点64.7℃)、エタノール(沸
点78.37)がすべて気化し、実施例2及び実施例6において、還元電極5
の表面近傍の温度を100℃にすることで水、メタノール、エタノールが気
化し、還元電極5の表面から除去されたことにより、還元電極5の表面に気
相の二酸化炭素を常に供給できるようになったことが要因と想定される。実
施例2及び実施例6よりも実施例3及び実施例7の方が、二酸化炭素還元反
応のファラデー効率の維持率が高いのは、ギ酸が気化したことによると考え
られる。
更に、実施例1及び実施例5の二酸化炭素還元反応のファラデー効率の維持
率は、比較対象例1及び比較対象例2と同様の値で、実施例2、3及び実施
例6、7よりも小さい値である。これは、還元電極5の表面近傍温度が水、
ギ酸、メタノール、エタノールの沸点より低く、還元電極5に付着した液体
生成物が除去できなかったことにより、還元電極5の表面の反応場が失われ
てしまったためと考えられる。したがって、還元電極5の表面近傍温度は、
全ての液体生成物の沸点よりも大きい値であることが好ましい。すなわち、
熱源41の加熱温度は、還元電極5の表面で起きた二酸化炭素の還元反応に
より還元電極5の表面に生成される全ての液体生成物の沸点よりも高い温度
であることが好ましい。
[本発明の効果]
本発明によれば、二酸化炭素の気相還元装置100は、還元槽4を囲むよう
に配置された熱源41を用いて、二酸化炭素の還元反応により還元電極5の
表面に生成する液体生成物を加熱するので、その液体生成物を気化させ、還
元電極5の表面から除去できる。これにより、還元電極5に対して常に気相
の二酸化炭素を直接供給可能となり、二酸化炭素の供給量を維持可能となる
ので、二酸化炭素還元反応の寿命を向上させることができる。更に、その液
体生成物を気化させるので、すべての還元生成物を気体としてまとめて回収
可能となり、還元電極5の表面に生じた液体生成物の回収が簡便になる。
---------------------------------------------------------------------
[脚注]
ナフィオン:ナフィオンはスルホ化されたテトラフルオロエチレンを基にし
たフッ素樹脂の共重合体で、1960年代にデュポン社のWalther Grotによって
発見された[1]。最初のイオン伝導性を持つポリマーである。ナフィオンの類
稀なイオン伝導性はスルホ基で修飾されたテトラフルオロエチレン(テフロ
ン)にペルフルオロビニルを組み込むによるものである[2][3]。ナフィオン
は優れた熱、機械的安定性により固体高分子形燃料電池のプロトン伝導体と
してかなり注目されている。ナフィオンの優れた導電特性の化学的特長に研
究の焦点があてられた。SO3H(スルホ酸)グループ上のプロトンは持ち上げ
られる。陰イオンや電子は膜内を移動せず陽イオンだけ移動する。
via Wikipedia
出所:燃料電池の要!高分子電解質「ナフィオン」とは | M-hub(エムハブ)
--------------------------------------------------------------------
自在行動概論 ⑤
パレスチナ問題とその歴史
「環境リスク本位制時代」を公言している私(たち)には、「パレスチナ問
題」は、「人類消滅」を加速させる「世界大戦」の説明要因の1つであるこ
とを踏まえ、その歴史をお温習いしておこう。
via jp.Wikipedia
2008 - 2009:ガザ紛争
イスラエル国防軍の作戦名は「キャストレッド作戦( מבצע עופרת יצוקה、英語: Operation
Cast Lead)」。「鋳造された鉛」の意味で、ユダヤ教の祭日であるハヌカーの際、子
供達に与えられるドレイドルという独楽を指している。 イスラエルに批判的なアラブ
諸国などでは「ガザの虐殺(مجزرة غزة 、英語:Gaza Massacre)」と呼ばれている]。
この時点では、第四次中東戦争(1973年10月)以来最大の死傷者を出した紛争とな
った[15][16]。パレスチナ側では民間人を含む1,300人以上が死亡したが、犠牲者の
大多数は一般市民であり、特に死傷者の1/3は子供で、未成年の被害者が特段に
多い紛争となった。 これまでに、市民への無差別攻撃、怪我人搬送のために走行
していた国際赤十字の救急車両への攻撃、国際連合が運営し、避難所としてイス
ラエルへも通告していた女学校への無差別空爆、幼児への無差別銃撃など、数多
くの戦争犯罪が判明している 。
経過
イスラエル軍による空爆
2008年12月27日(現地時間午前11:30、UTC午前9:30)、イスラエル空軍がガザ地
区全土に大規模な空爆を開始した。2009年1月3日の地上侵攻までの死者は430人
にのぼった。
1月3日、イスラエル軍はガザ地区への大規模な砲撃の後、歩兵、戦車、砲撃隊な
どの隊列が侵攻を開始し、事態は市街戦に発展した。ハマースとの激烈な戦闘が
行われている。ガザ地区では、空爆や砲撃によって自宅を失った一般市民4,000人
が更に避難民と化した。
1月6日、イスラエル軍が国際連合パレスチナ難民救済事業機関 (UNRWA) の運営
する避難所となっている学校を砲撃、少なくとも40人が死亡した。これに対し、スラ
エル軍は同施設の付近からハマース側の攻撃があったために加えた反撃であると
主張しているが、UNRWAや地元住民は「現場に戦闘員はいなかった」と否定して
いる。 1月7日、イスラエル軍は国際機関らによる援助物資の搬入のため、27日の
攻撃開始以来初めて、3時間程度戦闘を停止した。
停戦への動き 戦闘開始が年末で、多くの諸外国がクリスマス及び年末年始の休暇
の時期に入っていたことから停戦調停が遅れ、戦闘が長引く要因になった。 ハマー
スの代表団は1月9日夜、カイロ入りし、仲裁国のエジプトと停戦交渉に入った。エジ
プトによる停戦案にイスラエル側は原則同意の方針を示したが、ハマースの在外指
導部はこれを拒否した。その他にも国際連合やフランスなどから停戦案が提示
されたが、どれも合意には至らなかった。 戦闘開始から3週間たった
1月17日、イスラエルは一方的な「停戦宣言」を出し部隊の引き上げを始めた。ただ
し、この停戦は上記のエジプト仲介による停戦プロセスとは関係がない。直後、ハマ
ースも抗戦を停止した。その後イスラエル軍は、アメリカのバラク・オバマ新大統領
が就任した20日にガザの市街地からの撤退を完了した。
戦闘後
戦闘停止後、各国・団体によるガザへの復興支援が始まったが、イスラエルとエジ
プトが国境封鎖と検問を継続しており生活用品の運搬にも支障が出ている。
1月27日、エジプト政府が停戦協定を2月5日前後に発効させる方向で調整をしてい
ると報じられた。 同27日、境界付近で爆発が起こり、パトロール中のイスラエル兵
1人が死亡。イスラエルは直ちにガザ方面へ反撃し、農民1人が殺害された。イスラ
エルは人道物資支援の検問所をすべて閉鎖した。 現在も散発的にガザから迫撃
砲が撃ちこまれ、それに対してイスラエル軍が反撃するなど小規模な戦闘は今も
続いている。このため、ガザの境界近くに住むイスラエル人住民の間からは、問題
の根本的解決のためにガザ再攻撃を望む声が強まっている。
1月18日にハマース側が1週間の停戦を表明したことで、一応の終結を見た。
1月21日にイスラエル国防軍は、ガザ地区から撤退した。これは、1月20日のバラク
・オバマの米国大統領就任に配慮したものといわれている。オバマは「イスラエルの
自衛権」に理解を示す声明を出し、引き続き米国はイスラエル支持を鮮明にした。
一方、ジョージ・ミッチェル元上院議員を中東問題特使に任命したが、米国最大の
ユダヤ人団体名誉毀損防止同盟のエイブラハム・フォックスマン委員長は、「ミッチ
ェル氏は中立だ」「だから心配だ」と不満を口にした。 イスラエル南部でロケット弾攻
撃のビデオ, 2009年3月 イスラエルはガザ地区の封鎖を継続しており、ハマースは
もとより、他の住民も密輸トンネルの再建で対抗しようとしている。これは民生品が
長期の包囲で不足しているためである。ハマースは1年の、イスラエルは1年半の停
戦案を提示したが、進展は見られない。 双方による報道管制も行われている。特に、
イスラエルは報道関係者のガザ地区への立ち入りを一切禁じ、アルジャジーラなど
従来よりガザ地区に記者が駐在しているマスコミ以外は、直接取材は不可能に近い
状況になっている。1月3日の地上侵攻作戦では、規制解除前に報じたイランの記者
を逮捕した。1月9日には米3大ネットワーク(ABC、CBS、NBC)やCNN、欧州の主
要メディアなどが連名で、現地取材を認めるよう声明を出した。イスラエル最高裁
は、外国メディアの現地取材を認める判決を出したが、イスラエル国防軍側はまだ
認めていない。
3月31日、イスラエルのベンヤミン・ネタニヤフ・リクード(団結)代表が、1999年以来
10年ぶりに首相に就任。
2010 - 2017:パレスチナ側の手詰まりと米トランプ政権発足
2010年4月13日、イスラエル国防軍の命令1649[66] およびイスラエル国防軍命令1
650(英語版)が発効した。1969年の命令329で布告した規制を拡大するもので、「不
法入国者」の定義を単に滞在・在住許可証を携帯していない者から、「ユダヤ・サマ
リア[注 9]」でイスラエル国防軍の在住・在留許可を受けていない者に拡大した。 こ
れにより、ガザ地区出身者の、ヨルダン川西岸への立ち入りが実質的に許可制とな
り、パレスチナ人住民のガザ地区への追放も法制化された。 アメリカ合衆国仲介の
和平交渉が暗礁に乗り上げ、12月には南アメリカ諸国においてパレスチナの国家
承認の動きが起こった[68]。 2011年5月15日、ヨルダン川西岸、ガザ地区、レバノン
のイスラエル国境付近、シリアのゴラン高原などで、イスラエルの占領に抗議する
集会・デモが行われ、国境を越えた参加者をイスラエル軍が砲撃・発砲し、合計で
12人が死亡した。
この項つづく
------------------------------------------------------------------------------------------------------ 風蕭々と碧い時
風蕭々と碧い時
John Lennon Imagine
Deck The Halls

『アダムス ファミリー: サウンドトラック』はハミー・マンとマーク・シャイマンがプロデュ
ース]。 ハミー・マンが編曲し、デューク・エリントン、アーヴィング・ミルズ、マーク・シ
ャイマン、サクシー・ダウェルが作曲。 1991年12月3日にキャピトル・レコードからリリ
ース。 MCハマーの「Addams Groove」は映画のテーマソングであり、映画の上映
前にミュージックビデオが流された。
『アダムス・ファミリー』は、漫画家チャールズ・アダムスが作成した漫画と、デヴィッド
・レヴィが制作した1964年のテレビシリーズの登場人物のアメリカの超自然的ブラッ
クコメディ映画(1991年)。 元撮影監督バリー・ソネンフェルドがスクリーン監督デビ
ュー作の本作は、モーティシア・アダムス役でゴールデン・グローブ賞にノミネートさ
れたアンジェリカ・ヒューストン、ゴメス・アダムス役でラウル・ジュリア、フェスタ・アダ
ムス役でクリストファー・ロイドが出演。 この映画は、長く離れ離れになっていた親戚、
ゴメスの弟フェスター・アダムスと思われる人物と再会する、奇妙で不気味な貴族一
家に焦点を当る。
● 今夜の寸評:































※コメント投稿者のブログIDはブログ作成者のみに通知されます