子宮頸がんは女性の悪性腫瘍のうち世界で2番目に頻度が高く、2002年にはほぼ50万人が新たに診断を受け約27万人が死亡しているが、その約80%が開発途上国の女性。
日本では1年間での新たな罹患者が約7000人、死亡者は約2000人
米国では1年間での新たな罹患者が推定12000人、死亡者は4000人以上
HPVの感染は通常は基底膜を超えてウイルスが体内に侵入しないため、自然感染で抗体価の上昇は限定的
HPV-16/18は世界中で70%の子宮頚癌及び50%の前癌病変(CIN2/3以上)の原因となる。
HPV-6/11は世界中で90%の尖圭コンジロームの原因となる。
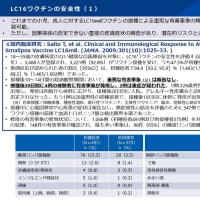
HPV-16/18 AS04アジュバントワクチンは、接種後6.4年が経過しても極めて良好な長期的有効性を示すとともに高い免疫原性が持続し、良好な安全性が確認された。
(Lancet; No 9706)
4価のワクチンは尖圭コンジローム予防のため男性にも適応(海外)
子宮頚癌におけるHPV16/18関連の占める割合 60-80%
日本では約60%
*4価ワクチン:ガーダシル(Gardasil™)
・FDAに2006年に認可された。
・国内で2011年7月1日に製造販売承認
・国内で2011年8月26日に発売
・HPV感染のない女性における接種において、ワクチンに含まれるタイプのHPVによる子宮頚癌前癌病変(2度以上の異形成)及び子宮頚癌を97-100%予防する。
[N Engl J Med. 2007 May 10;356(19):1915-27]
・既に性交渉歴のある女性が大部分を占めた研究においては、ワクチン接種で子宮頚癌前癌病変(2度以上の異形成)及び子宮頚癌の予防率は低下して44%。
・HPV感染のない女性における接種において、HPV-16/18に関連した他のタイプのHPVに対しても子宮頚癌前癌病変(2度以上の異形成)及び子宮頚癌の予防効果が約20%あり。
[J Infect Dis. 2009 Apr 1;199(7):926-35.]
2006 FDAにより認可された。
接種方法:9歳から26歳に対して0.5mlを0, (1-)2, 6ヶ月で3回、同じワクチンを接種。
ベトナムの少女を対象とする研究で、標準的な0-2-6法と比較した0-3-9法と0-6-12法の非劣性が示されている[JAMA 2011;305(14):1424-1431]
日本におけるサーバリックスとの違い
・太腿に筋肉注射が可能
・尖形コンジローマに適応あり
(日本における年間推定患者数は男性18,382人、女性20,281人 日本臨牀. 2009:67;153-6. )
・注射針が付属していない
・牛乳由来成分がウイルス培養時に使用されている
・接種間隔が0, 2, 6ヶ月(CDCは最低4週間あければ接種可としている)
・接種適応が9歳から
・アジュバントがヘプタバックスと同じ水酸化Al・K
・18価の抗体低下が早いが副作用は少ない
・導入年(2011年)の公費負担について自治体の対応が不透明
日本における海外のガーダシルとの違い
・男性に接種適応がない
*2価ワクチン:サーバリックス(Cervarix™)
・FDAに2009年に認可された。
・国内で2009 年10 月16 日に製造販売承認
・国内で2009 年12 月22 日に発売
・HPV感染のない女性における接種において、ワクチンに含まれるタイプのHPVによる子宮頚癌前癌病変(2度以上の異形成)及び子宮頚癌を93%予防する。
・無作為化した女性において、全てのタイプのHPVによる子宮頚癌前癌病変(2度以上の異形成)及び子宮頚癌の発生が30%減少する。
・HPV感染のない女性における接種において、HPV-16/18に関連した他のタイプのHPV(子宮頚癌の原因の約20%)に対しても子宮頚癌前癌病変(2度以上の異形成)及び子宮頚癌を約50%予防。
[Lancet. 2009 Jul 25;374(9686):301-14. Epub 2009 Jul 6.]
・予防接種前に感染した病変に対しての治療効果はなし。
2009年にFDAに認可、100カ国以上で認可されている。
・ワクチンの効果は理論上20年近く抗体価が保たれるとされるが、最長6.4年まではワクチンの効果(HPV 16/18感染(初発)に対して95.3%、12ヵ月持続感染に対して100%)は証明されている[Lancet. 2009 Dec 12;374(9706):1975-85.]
用法及び容量:10歳以上の女性に、通常、1回0.5mLを0、1、6ヵ月後に3回、上腕の三角筋部に筋肉内接種する。
日本で使用しているのはベルギー産
シリンジのキャップ及びプランジャーには天然ゴム(ラテックス)が含まれているため、ラテックス過敏症のある被接種者においては、アレルギー反応に十分注意する
副反応
疼痛99%
発赤88.2%
腫脹78.8%
痛みのためか若い女性でワクチン後のfaint報告数が増加
妊娠中は妊娠終了まで延期
授乳期の接種は推奨されないが否定するデータもなし
全体としてはワクチン接種(2価)による流産の有意な増加は認められないが、妊娠前3ヵ月以内のワクチン接種のリスク増大の可能性について完全に払拭することができない[Wacholder S, 2010 BMJ]
子宮件癌検診について
米国産科婦人科学会(ACOG)子宮頸癌検診の新規ガイドライン2009
- 子宮頸癌検診は21歳で開始すべき
- 30歳未満のほとんどの女性は、2年に1回検診を受けるべき
- 連続して3回受けたパップテストの結果が正常であった30歳以上の女性は、3年に1回の検診でよい
- 特定のリスク因子を持つ女性はより頻回に検診を受ける必要があるかもしれない. そのリスク因子とは, HIV陽性, 免疫抑制, 子宮内でのDES暴露あるいは子宮頸部上皮内腫瘍(CIN)2、CIN3、子宮頸癌の治療歴など
[Obstetrics and Gynecology 2009-12]
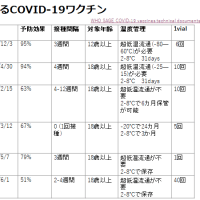
2回接種の推奨について:
2016年10月7日米国でHPV2回接種のFDA承認
2016年10月19日ACIPが2回接種を推奨(15歳未満で接種を開始した場合に限り、6-12月の接種間隔で)
2016年12月16日米国でHPV2回接種のプログラムを開始
2017年5月12日WHO Position Paperを更新 9-14歳をターゲットに2回接種を推奨
2014年12月に米国でFDAが製造販売を承認
2015年2月に米国でACIPが推奨接種ワクチンに認定(2016年末には米国で流通するワクチンは9価のHPVワクチンのみとなる)
2016年10月に米国でACIPが推奨、接種を15歳未満で開始した場合に限り、接種回数を2回接種に変更(上記参照)
HPVの2価、4価、9価ワクチンには共通して遺伝子型 16及び18が含まれ、この遺伝子型のHPVは子宮頸がんの原因の66%、その他のHPV関連悪性腫瘍の原因の大部分を占める
HPV4価と9価に共通して含まれる遺伝子型6及び11は、主に尖圭コンジローマの原因となる
HPV9価にのみ含まれる遺伝子型 31, 33, 45, 52及び58は子宮頸がんの約15%の原因とされる
2008-2012年の米国での評価で、HPV16及び18によるHPV関連癌が推計24,600例に対して、追加5価によるHPV関連癌は推計3,800例であり、その多く(3,100例)が女性での癌であった
ACIPは2価または4価で接種を開始した場合、9価ワクチンを用いて接種を完了させることを推奨しているが、2価または4価で接種を完了している場合には9価での追加接種は推奨していない
HPV接種に加えて、21歳から65歳にかけて、子宮頸がんのスクリーニング検査を受けることが推奨されている