ポリオワクチン [Polio Vaccine]
2011/4/30更新(一部古い情報を含む可能性があります)
1953年、米国でIPVの開発(Salk)
1955年、IPVの使用承認、有効性についての証明
1959年、国立予防衛生研究所にてワクチンを試験製造(Salk)、国内メーカーでワクチン(Salk)の国内量産に着手し一部に接種
1960年、米国でOPVの開発(Sabin)
1960年、北海道から流行が始まり日本で患者数ピーク(5606人:日本ポリオ研究所、6500人:東京都感染症情報センター)、生ポリオワクチンの試験的集団接種(長岡)
1960年~1964年、日本で不活化ワクチンの推奨接種
1961年、日本で流行性生ワクチン緊急接種(全ての3ヶ月~5歳までの小児、流行地では9歳までの小児全員1300万人が対象) (モダンメディア, 2010)
1962年、生ポリオワクチン製造所設立、更に生ワクチン1700万人分を輸入し13歳未満の小児に接種
1963年、米国でOPV接種が承認(1961年カナダで承認)
1964年~国産第一ロットが国家検定に合格。現在、生ワクチンの法律による接種(国産OPVを2回接種)(1976年~定期)
1968年、財団法人日本生ポリオワクチン研究所設立
1980年、ドロッパー法へ変更
1980年に日本国内最後の野生株ポリオ感染報告
1988年時点では125カ国以上で35万症例以上
1990年代には政策や資金の投入によってポリオ罹患者の数が急速に減少
1991年に南北アメリカ地域ペルーで最後の野生株の症例が報告
1994年に南北アメリカ地域で排除宣言
1997年に西太平洋地域カンボジアで最後の野生株の症例が報告
1998年にヨーロッパ地域トルコで最後の野生株の症例が報告
1999年には野生株ポリオ2型により麻痺を生じた最後の症例が報告
2000年に西太平洋地域で排除宣言
2002年に欧州地域で排除宣言
2003年時点では6カ国で784症例の報告
2005年までには残りの1型・3型による症例も1988年から99%減少した
2010年時点での野生株ポリオ発症報告の75%はインドとナイジェリア
その他、流行国はパキスタン、アフガニスタンを含む4か国
輸入症例を認めているのはその他8か国
そのうちアンゴラ、チャド、コンゴ民主共和国では再流行を認め、別の地域へ流行を広げる可能性あり。
2010年8月時点では、輸入例に端を発して、ポリオ撲滅達成国、タジキスタンでの流行あり(1例の野生株を除いて、ワクチン関連株vaccine-associated paralytic poliomyelitis (VAPP)の流行 458例中27例の死亡症例)
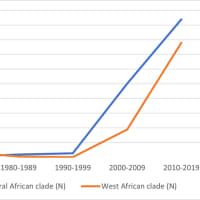
アフリカの野生株ポリオウイルスによる感染報告は流行国のナイジェリア21例から62例に増加(WPV1 + WPV3)も、全体では2010年に657例/12カ国から2011年に350例/12カ国まで改善を認める。
再興感染は2011年にアンゴラ5例(WPV1)、チャド132例(WPV1 + WPV3)、コンゴ民主共和国93例(WPV1)でみられる。
outbreakによる輸入感染は2011年にコートジボワール、ギニア、マリ、ニジェール、ケニア、中央アフリカ共和国、コンゴ共和国、ガボンでみられる。
MMWR March 23 2012, 61(11);190-194
2011年には野生株ポリオウイルス(WPV)の感染は16か国で650例あり、アフガニスタン、インド、ナイジェリア、パキスタンで常時流行が起こり、アンゴラ、チャド、コンゴ民主共和国では再流行を認めた。また中央アフリカ共和国、中国、コートジボワール、ガボン、ギニア、ケニア、マリ、ニジェール、コンゴ共和国の9カ国で輸入感染の発生を認めた。またワクチン由来株ポリオウイルス(cVDPV)による感染症例が、アフガニスタン、コンゴ共和国、モザンビーク、ニジェール、ナイジェリア、ソマリア、イエメンの7カ国で67例報告された。
2012年には野生株ポリオウイルスの感染は5カ国で223例あり、アフガニスタン、チャド、ニジェール、ナイジェリア、パキスタンでのみが起こった。インドは2011年1月を最後に野生株ポリオウイルスの報告がないため、2012年2月にWHOによって流行国のリストから外された。アフリカ地域では2つの遺伝子型のWPV1と1つのWPV3が見つかっている。またワクチン由来株ポリオウイルス(cVDPV)による感染症例が、アフガニスタン、チャド、コンゴ民主共和国、ケニア、ニジェール、パキスタン、ソマリア、イエメンの8カ国で67例報告された。ほとんどのcVDPVの流行はモザンビーク(type1)、イエメン(type3)を除いて、type2のcVDPVによるものだった。
WER 12 April 2013, vol. 88, 15 (pp. 153–160)
2012年4月27日に単独IPV(Salk) イモバックスポリオが薬事承認を得て、8月31日より国内で販売を開始、9月より定期接種化された
2012年7月27日、DPT-IPV(Sabin) テトラビック、クアトロバックが製造販売承認
2012年10月31日 、DPT-IPV(Sabin) テトラビック、クアトロバックが国内で発売、同年11月より定期接種
2012年11月10日、ナイジェリアで野生株ポリオ3型により麻痺を生じた最後の症例が報告
2014年3月27日、WHO南アジア事務局(SEARO)でポリオ排除の認定(Polio-free certification: WHO South-East Asia)
2014年5月5日、野生株ウイルスの国際的拡大についてIHRのEmergency CommitteeからPublic Health Emergency of International Concernの声明(WHO statement on the meeting of the International Health Regulations Emergency Committee concerning the international spread of wild poliovirus)
(2015年追記)
2014年7月4日、4種混合ワクチンDPT-IPV(Salk)「スクエアキッズⓇ皮下注シリンジ」の製造販売承認
2014年7月24日以降に野生株ポリオウイルスの新規確定症例報告がないことから、ポリオの流行国のリストから外れた。残る流行国はアフガニスタン、パキスタンの2か国のみ。
(WHO Removes Nigeria from Polio-Endemic List)
2015年12月9日、4種混合ワクチンDPT-IPV(Salk)「スクエアキッズⓇ皮下注シリンジ」の発売開始
今後2015年3月に決議されたWHA68.3に基づく世界ポリオ根絶計画に沿った対応(EB138/25, Dec 2015)
①2015年末までの野生株2型ポリオウイルスの廃棄
②2016年7月までのワクチンセービン株2型ポリオウイルスの廃棄
③不活化ポリオワクチンの定期接種への導入
④ウイルス封じ込めのための適切な設備基準に準拠した国が指定した拠点施設においての2型ポリオウイルスの取り扱い。
⑤根絶計画の遅れに伴い不足する資金19億9600万米ドルの捻出。
(2019年追記)
10月24日の世界ポリオデーに合わせて、WHOが3つあるポリオウイルス血清型のうち、2015年の2型野生株根絶宣言に続いて、3型野生株も世界で根絶状態にあることを宣言した(Two out of three wild poliovirus strains eradicated)
国内のポリオ報告数推移(感染症情報センター 予防接種の話)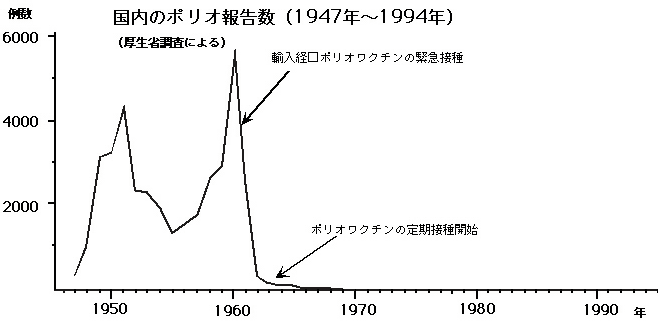
Polio
感染性が高く、主に経口で感染し、小腸で増殖する
脊髄前角細胞を侵し、麻痺を発生させる
潜伏期間は曝露から前駆症状の発症まで9-12日(5-35日)、発症から麻痺症状が生じるまで11-17日(8-36日)<Mandell, Douglas, and Bennett's Principles and Practice of Infectious Diseases , Seventh Edition>
初期症状は発熱、疲労、頭痛、嘔吐、頚部硬直、四肢の痛み
感染者のうち約1/200人の割合で、非可逆性の麻痺(通常下肢)をきたす(5歳以下に多いとされる)
このうち5-10%が呼吸筋麻痺により死亡する
発症数十年を経て、30-60%にポストポリオ症候群(筋力の低下・萎縮・手足の痺れ、筋肉痛等)を生じる
生ワクチンの経口(OPV), 不活化ワクチンの注射(IPV)の2種類
Vaccine associated paralytic poliomyeltis (VAPP):ワクチン関連麻痺性急性灰白髄炎
生ワクチンに関しては復帰変異によるワクチン関連麻痺性急性灰白髄炎(非対称性の麻痺)のリスクあり
日本では1970年から2000年の間に36例[ポリオワクチンを巡る最近の状況と我が国の将来(平成12年8月31日)公衆衛生審議会感染症部会ポリオ予防接種検討小委員会](ワクチン接種者に20例、非接種者に16例、約1/200-440万人の確率、約1/200-486万人、接触者約1/789万人。2006年にワクチン株由来あるいは VDPV 株由来の弛緩性麻痺についても、届出対象となった。[ポリオワクチンに関するファクトシート, 2010])
海外での報告では50万~350万人に1人の割合
0.04-0.13/100,000[Guimard T, et al. Am J Trop Med Hyg 81:1141, 2009]
子供よりも成人で頻度が高い
一方で途上国では、安価な値段、接種のしやすさ、ワクチンを受けていない人への移行等の利点があり、WHOでの推奨ワクチンである。
製薬会社によると3型の成分が主に関連し、過去に接種歴のない成人の初回接種時に起こりやすいとされる(1/78万人)
1999年以降米国ではIPVを使用するようになり、訴訟の問題から多くの国でも導入が進んでいる
OPVに伴う3つのリスク(1>2>3)
1. ワクチン関連麻痺(VAPP)
2. ワクチン由来ポリオウイルス(VDPVs)の流行
3. 液性免疫不全者によるVDPVsの慢性的排泄
OPVはVDPVを排除するため単価に切り替えられるところに来ている
[N Engl J Med 2011; 364:2273-2275]
日本では1961年6月カナダ・旧ソ連から経口生ワクチンを緊急輸入して国内の罹患率を低下させた歴史あり。
日本の定期接種はOPV2回であるが、野生株の感染報告の大部分を占める1型・3型の抗体保有率が低い(特に高齢者では60~80%程度の抗体保有率)ことが知られている
2型は全年齢を通じて100%近い高率を示す
特に1975年から1977年生まれの人の1型の保有率は低くなっており、これらの人達は、自分の子供がポリオウイルスワクチンを服用する時、あるいはポリオウイルスの流行地へ渡航する時に感染の危険性があるため、厚生省からは平成8年、これらの人達がポリオウイルスワクチンを服用できる機会を確保するように、通知あり(下記参照)
当面のポリオ予防対策について(平成8年11月28日 健医感発第147号 各都道府県・指定都市衛生主管部(局)長あて厚生省保健医療局エイズ結核感染症課長通知)
標記については、平成8年10月16日公衆衛生審議会伝染病予防部会より別添のとおり意見が出されたので、これに基づきポリオの抗体保有率が低い年齢層(現在19歳から21歳(昭和50年から52年生まれ)の者)に対し、下記の点に留意の上、各都道府県及び市町村において情報提供及び予防接種の接種機会の確保等にあたられるよう指導方お願いする。
昭和50年から52年生まれの方については、I型の抗体保有率が低い(昭和50年生:56.8%、昭和51年生:37.0%、昭和52年生:63.8%)ことがわかっています。しかし、この年齢層でもII型に対する免疫は十分についていますので、I型やIII型に対してもある程度の感染予防の効果はあるといわれていますが、ポリオの流行地に行く際やお子さんがポリオの予防接種を受ける際には、子どもの頃にポリオの予防接種を受けた方でも予防接種を受けることをお勧めします。
米国CDCの推奨では、IPVとOPVを混ぜて接種する場合は小児では4回の接種を基本としているが、18歳以上でのIPVの使用は推奨されていない。
また、IPVのみで接種する場合も4回目の接種は4歳以上では推奨されていない(FIGURE 2. Catch-up immunization schedule for persons aged 4 months through 18 years who start late or who are more than 1 month behind)。
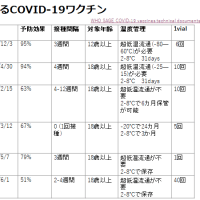
経口ポリオワクチンは2回服用し,免疫獲得率は1.2型が95%以上で3型が80%以上とされている(1999年厚生労働省調査で1回内服では1, 2型が90%以上、3型は41.5%)
ポリオウイルスの抗体検査には、中和反応(NT法)と補体結合反応(CF法)がある
NT法はウイルス液と抗体(被検血清)を反応させ、反応後のウイルスの感染性を感受性細胞を用いて測定する方法で、感染防御のための抗体を直接測定でき、感度・型特異性が高い測定方法
CF法はウイルス抗原と抗体(被検血清)を反応させた後、一定の補体を添加し抗原-抗体-補体を結合させ残存補体を定量する方法で、群特異性が高く比較的早期に抗体が消失するため、感染のスクリーニングに適する測定方法
乳児期にワクチン接種済である成人の抗体有無を調べるためには、NT法が有用(4倍以上で陽性)
OPV ( ⇔ IPV) 利点と欠点
安価(⇔ 高価)
簡便(⇔針と注射器を必要とするため医療行為・医療廃棄物の問題)
高く長い効果(⇔接種回数が多く、追加接種が必要)
局所分泌型抗体(IgA)も産生(⇔中和抗体のみで腸管等の局所には免疫獲得なし、定着には効果が低い)
周囲でも免疫獲得(⇔接種者のみが免疫獲得)
免疫不全者・妊婦で使用できない(⇔使用可能)
時に本来の病原性が出現(⇔病原性なし)
[2009年時点]*多くの国がIPVを導入している。
OPV単独接種を施行する国 – 日本、英国、中国、インド、インドネシア、ブラジル等
IPV単独接種を施行する国 – アイスランド、米国、オランダ、カナダ、スウェーデン、ドイツ、ノルウェー、フィンランド等
IPV, OPV併用接種を施行する国 – フランス、オーストリア、イスラエル、イタリア、デンマーク、ハンガリー、リトアニア等
米国では1990年代にIPV (OPV併用)に移行、1999年から全てIPV単独へ
OPV
1954年、Dr. A.B. Sabinによる臨床実験
用法及び用量
6週間以上の間隔をおいて2回経口接種し、接種量は毎回0.05mLとする(約2滴)
定期接種の接種対象年齢は生後3月から90月に至るまでの間であるが、生後3月から18月までの間に2回の接種を完了することが望ましい
IgM, IgGはOPV接種後2-3日で上昇を認め、IgMは2-3ヶ月で消失する。ウイルス血症は接種後2-5日で起きる。
生後6か月までの乳児でType1-3をそれぞれ、72%, 88%, 75%が便中に排出を認める。
徐々に排出する割合は低下するが、50%前後になるのに4W程度はかかる。[Am J Epidemiol 86:112-136, 1967]
IPV
1955年、Dr. J Salkによる不活化ワクチン開発、米国で実用化
• IPOL®: Contains IPV only
• Pediarix®: Contains IPV, DTaP, and HepB vaccine; approved for use as a three dose primary series in infants born of hepatitis B surface antigen-negative women, beginning as early as 6 weeks of age
• Pentacel®: Contains IPV, DTaP and Hib; approved for use in infants and children at 2, 4, 6, and 15 through 18 months of age
• Kinrix®: Contains IPV and DTaP; approved for the fifth dose of DTaP and the fourth dose of IPV at 4 to 6 years in children whose previous DTaP doses were with Infanrix® or Pediarix®
効果:
2回接種後、3価のポリオウイルスで93%以上が中和抗体上昇、3回接種後は100%。
ワクチン間隔が短い場合、またはポリオの抗体価が高い母親から生まれた幼児ではワクチン接種後の効果は減弱。
キューバでのRCTでは生後6, 10, 14週でIPVもしくはプラセボを接種して、セロコンバージョン率はポリオの1, 2, 3型それぞれに対して、94, 83, 100%であり、3回の接種で母親の抗体との干渉の可能性は軽減されるかもしれない。
感染防御レベルまで上昇した抗体は少なくとも理論的には5年は続く[N Engl J Med. 2007 Apr 12;356(15):1536-44.]。
途上国でのIPVの効果についての情報は少ない。
セネガルでのIPVでの感染防御率は1, 2回接種により、それぞれ36, 89%だった[Lancet 1988 Apr 23;1(8591):897-9.]。
ポリオウイルスに対する血清中の抗体は上昇するものの腸管内での分泌型IgA 抗体は上昇しないため、経口感染して腸管で増殖するポリオに対しての局所での免疫は不十分となりやすい。
副反応:
ベロ細胞由来のIPVによる局所反応発生率はプラセボと同等であり、ワクチン関連の麻痺性灰白髄炎を含めて重篤な反応と関連するとのエビデンスはない
IPOL®
接種方法:筋肉または皮下注射
成人:
ワクチン未接種であれば0.5mlを1-2月間隔で2回接種して、6-12ヶ月後に3回目を接種する。
ワクチン接種の既往(3回未満のIPVの接種、少なくとも1回のOPV)があれば、少なくとも1回のIPVを追加して、時間が許せばワクチン接種を終了させるために2回目のIPVを接種する。最後までワクチン接種が終了しているが、暴露のリスクが高い人に対しては、1回のOPVを追加する。
小児:
初回接種として、0.5mlを生後2, 4, 6-18ヵ月で3回接種する。少なくとも4週間は接種間隔をあける必要があり、8週間以上間隔をあけることが望ましい。
ブースター接種として、0.5mlを4-6歳で接種する。初回接種からブースターまでは少なくとも6ヵ月以上の間隔をあける。最終のブースター接種は、それまでに何度IPVを接種されていても4歳以上である必要がある。4-6歳で最終の接種がされていなければ、できるだけ速やかに実施する必要がある。
できるだけ早期、かつ短期の間隔での予防接種はセロコンバージョンを減弱するため、差し迫った状況にある場合おいてのみ行われるべき。
IPOL®内容: Type 1 poliovirus 40 D-antigen units, type 2 poliovirus 8 D-antigen units, and type 3 poliovirus 32 D-antigen units per 0.5 mL (0.5 mL, 5 mL)
日本におけるIPVの状況
1990年 Sabin IPV臨床治験(ポリオ研)
2001年 製造承認申請
2005年 製造承認申請取り下げ
DPT+IPV 臨床治験実施中(1期3回接種終了、追加接種データ待ち)
野生株ポリオ撲滅後のポリオウイルス病原体管理の厳格化が必要であることから、弱毒化ポリオウイルスに由来するSabin-IPV製造技術の確立が期待されている
2011年12月27日に阪大微研よりDPT(ジフテリア、百日咳、破傷風)との混合ワクチンが承認申請され、さらに2012年2月23日にSanofi Pasteur社より単独IPVの承認申請がされた
OPVによる認定麻痺事例
予防接種法に基づく認定人数
2000年 1人
2001年 2人
2002年 1人
2003年 2人
2004年 1人
2005年 0人
2006年 0人
2007年 2人
2008年 4人
2009年 1人
2010年 2人
2次感染対策事業に基づく認定数
2004年 2人
2005年 3人
2006年 0人
2007年 0人
2008年 0人
2009年 0人
2010年 1人 (VAPP発生年と認定年にはズレがある)
Ref 第16回厚生科学審議会感染症分科会予防接種部会
Reference:
http://www.srl.info/srlinfo/90_virus/
NT法: 各約4000円 (80点)
CF法: 各約1000円 (80点)
中和抗体4倍以上がカットオフ値
一般にプラーク数を60%以上減少させる血清の最大希釈倍数の逆数で表示する
Polio End Game Plan (SAGE 2014)
2018年までに世界からポリオを根絶するために、2016年4月から3価の経口生ポリオワクチン(tOPV)の使用を中止し、1型と3型を含む2価の経口生ポリオワクチン(bOPV)と1回以上の不活化ポリオワクチン(IPV)で予防接種を行う方針となっている。