FDA News Release
FDA approves Gardasil 9 for prevention of certain cancers caused by five additional types of HPV
米国FDAがMerk社による9価のHPVワクチン(Gardasil 9)を承認した。
FDAによると、子宮頸がん、外陰部、膣、肛門がんの9割を予防できる可能性がある。
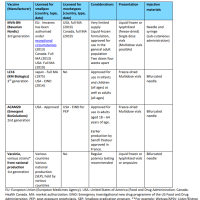
承認された接種年齢は女性で9-26歳、男性で9-15歳。
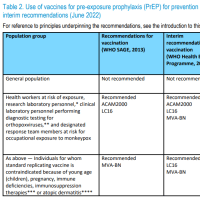
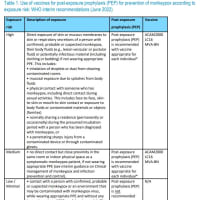
4つのがんの予防を目的としたHPV 16, 18、尖圭コンジローマの予防を目的としたHPV 6, 11に加えて、4つのがんの予防を目的としたHPV 31, 33, 45, 52, 58の5つの遺伝子型が含まれる。5つの遺伝子型は、HPV 16, 18でカバーされない子宮頸がんの20%がカバーされる。
16-26歳の14,000人を対象に実施した無作為化比較試験において、これまでの4つの遺伝子型に同等の効果がみられたことに加え、製剤に追加された5つの遺伝子型による4つのがんの97%に効果がみられた。
追加された5つの遺伝子型による肛門がんの頻度は低いため、効果は78%の効果がみられる4価製剤が基本となる。
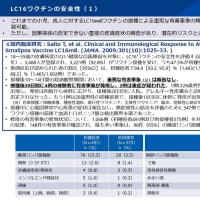
安全性については、男女13,000人に評価が行われ、最も頻度が高いのは接種部位の疼痛、主張、発赤、頭痛となっている。
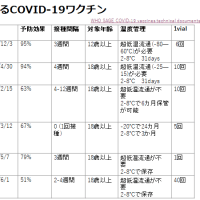
接種回数はこれまで同様に3回で、初回からそれぞれ2, 6月の間隔を置いて接種を行う。