1.補体システムとは
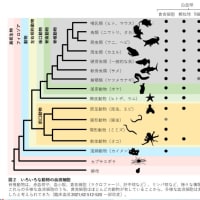
補体システムとは、獲得免疫より古くからある自然免疫であり、最近の研究ではサンゴやカブトガニからも補体が見つかっているとのことです。
補体系は20種類以上のタンパク質やタンパク質断片から成り、それらのタンパク質が組み合わされ連携することで、様々な防御活動を行っています。例えば、補体系のあるタンパク質が他のタンパク質を活性化し、そのタンパク質がまた他のタンパク質を活性化するという連鎖的な反応を行い、最終的には「細胞膜傷害性複合体」という複合体を構成して、細菌や細胞に穴を開けて破壊してしまいます。
補体系の活性化には(発見された順に)、「古典経路」(抗体複合体から反応する)、「副経路」(抗体を介さないで反応する)、「マンノース結合レクチン経路」(病原体の糖タンパク質を認識して反応する)の3つプロセスがあります。
「蛋白分画とは
血液から細胞成分(赤血球,白血球,血小板)を取り除いたものを血漿とよび,血漿から主にフィブリノゲン(血液を固める働きをもつ蛋白質)を取り除いたものを血清と言います。血清の中の蛋白をおおまかに分類する方法に電気泳動法があり,蛋白質を5つのグループに分けます(アルブミンと,α1,α2,β,γ の4つのグロブリン分画)。
各分画の基準値(%)と各分画に含まれる主要蛋白は次のようになります(聞き慣れない名前ばかりと思いますが,主なものを列挙しておきます)。
アルブミン分画(62~71%):トランスサイレチン(甲状腺ホルモンを輸送)
アルブミン(浸透圧維持・物質の輸送)
グロブリン分画
α1(2~4%):α1アンチトリプシン(炎症で増加する急性期蛋白)
α1酸性糖蛋白(炎症で増加する急性期蛋白)
α2(5~10%):α2マクログロブリン(プラスミンなどの活性抑制)
セルロプラスミン(銅の輸送に関与。炎症でも上昇)
ハプトグロビン(ヘモグロビンと結合)
β(7~11%):β リポ蛋白(脂質輸送)
トランスフェリン(鉄の輸送)
C3(補体第3成分,生体防御に関与)
γ(10~20%) 免疫グロブリン(IgG・IgA・IgM)
アルブミンとグロブリン分画のγ(γグロブリン)で80%近く占めますので,総蛋白濃度に影響を及ぼすのはアルブミンとγグロブリンの変動です。 」
血液から細胞成分(赤血球,白血球,血小板)を取り除いたものを血漿とよび,血漿から主にフィブリノゲン(血液を固める働きをもつ蛋白質)を取り除いたものを血清と言います。血清の中の蛋白をおおまかに分類する方法に電気泳動法があり,蛋白質を5つのグループに分けます(アルブミンと,α1,α2,β,γ の4つのグロブリン分画)。
各分画の基準値(%)と各分画に含まれる主要蛋白は次のようになります(聞き慣れない名前ばかりと思いますが,主なものを列挙しておきます)。
アルブミン分画(62~71%):トランスサイレチン(甲状腺ホルモンを輸送)
アルブミン(浸透圧維持・物質の輸送)
グロブリン分画
α1(2~4%):α1アンチトリプシン(炎症で増加する急性期蛋白)
α1酸性糖蛋白(炎症で増加する急性期蛋白)
α2(5~10%):α2マクログロブリン(プラスミンなどの活性抑制)
セルロプラスミン(銅の輸送に関与。炎症でも上昇)
ハプトグロビン(ヘモグロビンと結合)
β(7~11%):β リポ蛋白(脂質輸送)
トランスフェリン(鉄の輸送)
C3(補体第3成分,生体防御に関与)
γ(10~20%) 免疫グロブリン(IgG・IgA・IgM)
アルブミンとグロブリン分画のγ(γグロブリン)で80%近く占めますので,総蛋白濃度に影響を及ぼすのはアルブミンとγグロブリンの変動です。 」
「…体表面を突破した病原体に対しては、さまざまな防御ペプチドや防御細胞が関与するより複雑な非特異的防御システムが発動する。
補体
脊椎動物の血液には30種類程度の抗微生物タンパク質から構成される補体システムが存在する。これらのタンパク質はさまざまな組み合わせで、3種類の防御活動を行う。それぞれの防御活動で、補体系タンパク質は、あるタンパク質が別のタンパク質を活性化し、そのタンパク質がさらに活性化を行うという一連の連続反応、すなわちカスケードを生じさせる。
■最初に補体は病原体に結合して、貪食細胞に的であることを認識させて攻撃しやすくする。
■その後、炎症応答を活性化し、感染部位に貪食細胞を集結させる。
■最終的には、細菌のような侵入してきた細胞を溶解(破裂)させる。
インターフェロン類
貪食細胞
ナチュラルキラー細胞
(引用終わり)」
「Bordet (1895年)は、溶菌現象には抗体以外の易熱性の因子が必要と報告した。Ehrlichはこの因子を補体(complement)と命名した。補体は、血液中に存在する約20種の易熱性のタンパク質からなる複雑な反応系で、溶菌作用、オプソニン作用、貪食細胞の感染部位への集合を促進するなどの機能をもつ。補体系のタンパク質は非動化の条件(56℃,15分)で完全に失活する。


(引用終わり)」
「…補体蛋白の中で最も重要な働きをするC3は,最近サンゴやカブトガニなどの種々の無脊椎動物で発見されており,補体の起源は,当初考えられていたよりかなり古いことが推定される。原索動物のマボヤにおいてはレクチンを認識分子として機能するレクチン経路の原型の存在が確認されている。この原型をもとに,遺伝子重複とエクソンシャフリングなどを重ね,哺乳類に存在するレクチン経路や古典的経路に進化したものと思われる。補体系の活性化に働くマンノース結合レクチン(mannose-binding lectin;MBL)とフィコリンは,自然免疫において生体に侵入した病原体を非自己と認識するパターン認識分子である。そして,MBLとフィコリンはコラーゲン構造をもち,獲得免疫で働く補体古典的経路のC1q分子とは類縁関係にあると考えられている。」
「①古典経路は体内に侵入してきた細菌や細胞の膜抗原に抗体(IgGやIgM)が結合して免疫複合体を形成すると、補体第1成分(C1)がこの抗体と結合して、C1が活性化されます。活性化したC1は補体C4を活性化し、その後、補体(C2~C8)を次々に活性化します。その結果、最終的に膜上に補体第9成分(C9)の複合体を細胞壁(膜)に埋め込み、細菌や細胞に穴をあけます。
②別経路は古典経路とは異なり、免疫複合体を必要とせず、補体第3成分(C3)が少しずつ加水分解を受け(C3H2O)、血液中のB因子と結合します。B因子と結合したC3H2Oは大量のC3を活性化(C3b)します。このC3bが病原体の細胞壁に結合すると順次補体の活性化が進み、古典経路と同じように最終的にC9の複合体を形成して、細胞壁に穴をあけます。
③レクチン経路は3種の補体活性化経路のうち、最も新しく発見された経路です。高校生には耳慣れないレクチンという言葉ですが、レクチンとは糖鎖に結合活性を示すタンパク質の総称です。したがって、レクチン経路は病原体の細胞壁の特徴的な糖鎖構造を認識することに始まる補体活性化経路です。すなわち、病原体の細胞壁のマンノースを血液中に存在するマンノース結合レクチン(MBL)という物質が認識して結合すると、MBLと結合したMBL結合セリンプロテアーゼ(MASP)という酵素が活性化されます。この活性化したMASPが補体第4因子(C4)を活性化し、順次補体を活性化して、最終的に、他の補体活性化経路と同様にC9の複合体で細胞壁に穴をあけます。」
2.補体系の役割
補体系の役割としては、大まかに以下のような三つの働きがあります。
(1)抗原のオプソニン化
「オプソニン化」とは、微生物などの抗原に「抗体」や「補体」が結合して、抗原が食細胞に取り込まれやすくすることをいいます。食細胞に結合して食作用をしやすくする血清因子のことを「オプソニン」といい、補体のC3bや抗体のIgG(免疫グロブリンG)などがそれに該当します。一次感染では「補体」がオプソニン化の中心になり、抗体ができている二次感染ではIgGがオプソニン化の中心になります。
(2)膜侵襲複合体による細菌の破壊
補体系のタンパク質は、通常は血液中を不活性な酵素前駆体の形で循環しています。異物(細菌など)の侵入により刺激を受けると、補体系のタンパク質は活性化して、サイトカイン(低分子タンパク質で情報伝達物質で警戒情報)を放出したり、さらに他のタンパク質と連携して連鎖反応を押し進めるようになります。この連鎖が進むと、最終的には補体複合体「膜侵襲複合体(細胞膜傷害性複合体」ができて、それが細菌や細胞に穴を開け破壊します。
(3)マクロファージ等への走化性刺激
補体系からの警戒情報(サイトカインの放出)により、マクロファージなどの食細胞が呼び寄せられます。マクロファージなどは警戒情報を得ると、仮足というタンパク質の繊維状のもので、その発出場所に移動するようです(アメーバ運動)。
「補体(ほたい、英: complement)とは、生体が病原体を排除する際に抗体および貪食細胞を補助するという意味で命名された免疫系(補体系)を構成するタンパク質であり、補体系の役割は大きく言って下記の3つから構成されるものである。
- 抗原のオプソニン化
- 膜侵襲複合体による細菌の破壊
- マクロファージ等への走化性刺激
の3つである。
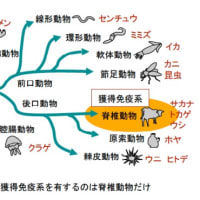
「補体」という名だが、進化の歴史においては、獲得免疫よりも補体の確立のほうが古い。
補体系は自然免疫に属しており、獲得免疫系のように変化することはない。
補体系は血液中の多数の小タンパク質からなり、それらは通常不活性な酵素前駆体の形で循環している。いくつかのトリガーの1つによって刺激を受けると系のタンパク質分解酵素が特定のタンパク質の分解反応を行い、サイトカインの放出を誘導し、さらに分解反応が進むようにカスケードの増幅を始める。この活性カスケードの最終結果は反応の大規模な増幅であり、細胞殺傷性の膜侵襲複合体(細胞膜傷害性複合体、MAC, membrane attack complex)の活性化である。補体系は20以上のタンパク質とタンパク質断片からなる。その中には、血清タンパク質、漿膜タンパク質、細胞膜レセプターを含む。これらのタンパク質は主に肝臓で合成され、血清のグロブリン分画の約5%を占める。
補体系の活性化には3つの生化学的プロセスがある:古典経路、副経路、マンノース結合レクチン経路である。
…補体(ほたい)とは免疫反応を媒介する血中タンパク質の一群で、動物血液中に含まれる。抗体が体内に侵入してきた細菌などの微生物に結合すると、補体は抗体により活性化され、そして細菌の細胞膜を壊すなどして生体防御に働く。補体は易熱性であり、56℃、30分の処理で失活する(非働化)。
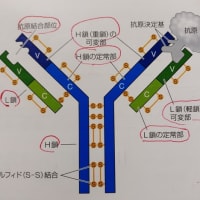
補体と呼ばれるタンパク群には複数のタンパクがあり、英語で補体を表す "complement" の頭文字をとってC1からC9で表される。C1にはさらにC1q、C1r、C1sという3種の分子の複合体であり、その他はC5a、C5bといったような複数の分子に分解される。これらのタンパク質群が連鎖的に活性化して免疫反応の一翼を担う。
さらに、C1からC9の補体タンパク質以外にB因子、D因子などを含めた16種類のタンパク質、液性(血液中にある)の5つの調節因子(I因子、H因子、C4Bp、C1抑制因子、properdin)、細胞膜上の4種類の調節因子(CR1、CR2、membrane cofactor protein、decay accelerating factor)などのタンパク質も補体の機能の発現・調節に関与しており、これらを総称して補体系と呼ぶ。
古典的経路
古典(的)経路とは、C1の活性化に始まる経路のことである。体液性免疫の抗体抗原複合体に補体C1が結合することでC1が活性化する。以降も基本的に数字順に活性化するが、C4は例外的に2番目に来る。『C1→C4→C2→C3b→C5b』まで活性化され、あとはC5bにC6以降が次々と結合、最終的にC5b6789にまでなる。
C5b6789は『細胞膜傷害性複合体』あるいは膜侵襲複合体(英: membrane-attack complex、MAC)といわれ、細菌の表面に取り付き細胞膜を破壊する。この働きを免疫溶菌反応、または免疫溶菌現象という。細菌の感染に対して好中球の貪食と並び重要な機構である。
副経路
C3は一部の細菌に対しては抗体を介さず直接その表面に結合し、いきなりC3a、C3b活性化(→以下は古典経路と同じ)の経路をとる。この経路を副経路あるいは第2経路という。
…補体系は宿主細胞にきわめて強力な傷害作用を与える可能性がある。このことは活性化が強力に制御されていることを意味する。補体系は補体制御因子(補体制御タンパク質)によって制御されている。これらは血液の血漿に補体タンパク質以上に高濃度で含まれており、補体制御因子の中には、細胞が補体のターゲットとならないよう、細胞の膜表面に存在するものもある。CD59はMAC形成時にC9の重合を阻害する。CD46(MCP)はC3bとC4bを分解する。DAFはC3の活性化を阻止する。補体制御因子は、異種移植において注目されている。ブタにヒトの補体制御因子を組み込むことで、ブタからヒトへの臓器移植時の拒絶反応が軽減される。
…補体系は他の免疫性要素とともに多くの病気の原因となっていると考えられている。例を挙げるとBarraquer-Simons症候群、喘息、紅斑性狼瘡、糸球体腎炎、様々な関節炎、自己免疫性心臓病、多発性硬化症、炎症性大腸炎、虚血再灌流障害等である。アルツハイマー病やその他の神経変性病態を示す中枢神経系の病気にも、補体系が関与しているのではないかという疑いは次第に高まっている。
経路の最終段階のところの欠損によって自己免疫病と感染症の両方に罹りやすくなる場合もある(特にナイセリア髄膜炎ではC56789複合体がグラム陰性菌を攻撃する際の役割に原因があって)。
補体制御因子のH因子と補体調節蛋白の突然変異は非典型的溶血性尿毒症症候群に関係がある。さらにH因子によく見られる単一ヌクレオチド多型(Y402H)は眼の習慣病の年齢に関連した黄斑変性症と相関がある。両病気とも、最近の知見では宿主の表面での補体の異常活性に原因がある。
感染症による変調
最近の研究によってHIV/AIDSにおいて、補体系が操作され患者の身体にいっそうの傷害を与えていることが示唆されている。」
「オプソニン化(オプソニンか、opsonization)とは微生物などの抗原に抗体や補体が結合することにより抗原が食細胞に取り込まれやすくなる現象。オプソニン作用とも呼ばれる。食細胞に結合して食作用を受けやすくする血清因子をオプソニンと呼ぶ。オプソニンとして働く主な分子として、補体のC3bと抗体のIgG(免疫グロブリンG)があるが、一次感染では補体がオプソニン化の中心となり、すでに抗体ができあがっている二次感染ではIgGがオプソニン化の中心となる。 」
「膜侵襲複合体(まくしんしゅうふくごうたい、英:Membrane-Attack Complex :MAC)または終末補体複合体(しゅうまつほたいふくごうたい)、細胞膜傷害性複合体(さいぼうまくしょうがいせいふくごうたい)は、蛋白質から成る複合体。ふつう宿主の補体系の活性化により病原体の細胞膜表面、特にC3活性化部位の付近に形成され、標的細胞の細胞膜に膜貫通孔を導くことで脂質二重膜を破壊し、それらを溶菌や細胞死に至らせる免疫系の作用因子(エフェクター)として働く。」
「走化性(そうかせい、英:chemotaxis)とは、生物体(単一の細胞や多細胞の生物体を問わず、細胞や細菌など)の周囲に存在する特定の化学物質の濃度勾配に対して方向性を持った行動を起こす現象のことであり、化学走性(かがくそうせい)ともいう 」
…真核生物の化学走性機構は細菌のそれとはまったく異なっているが、化学物質の濃度勾配を感知することが決定的に重要である点は同様である。
…受容体や細胞内シグナル伝達経路、効果器メカニズムの進化の違いが、すべて多様な真核生物の化学走性機構にかかわっている。真核単細胞生物ではアメーバ運動と繊毛(あるいは真核生物鞭毛)が主な効果器である(たとえばアメーバやテトラヒメナ)。より進化した脊椎動物由来の真核細胞の中にも、免疫細胞のように必要とされる場所へ移動するものがある。免疫担当細胞(顆粒球、単球、リンパ球)以外にも、従来は組織中に固定されていると考えられていた多くの細胞が特定の生理的(正常な)条件下(肥満細胞、線維芽細胞、血管内皮細胞)や病理学的(病的な)条件下(転移など)で移動することがわかっている。
…細菌の走化性とは対照的に、真核細胞が移動するメカニズムは解明が不十分である。外部からの走化性濃度勾配を感知する機構が存在するらしく、それが細胞内のホスファチジルイノシトール三リン酸(PIP3)という物質の濃度勾配となり、シグナル伝達によって最終的にアクチンフィラメントの重合が起きる。アクチンフィラメントの+端(成長する側、アクチンの項を参照)は様々なペプチドを通じて細胞膜の内側と連結し、仮足を形成する。PIP3の産生がDOCK2と呼ばれるタンパク質の細胞膜への集積を起こし、さらにホスファチジン酸というリン脂質が産生されDOCK2と結合することで仮足形成が効率的に進むことが明らかになっている。 真核細胞の繊毛も化学走性を起こす。この場合は主にCa2+(カルシウムイオン)依存性に、基底小体と9+2構造の微小管からなるシステムが繊毛運動を誘導される。数百に及ぶ繊毛が、基底小体相互間に作られた細胞膜下のシステムによって協調運動を行うが、シグナル伝達経路の全容は未解明である。」
「仮足は、鞭毛や繊毛と並ぶ、原生生物の3つの移動様式の1つを担う。このような仮足による運動をアメーバ運動と呼ぶ。このとき細胞の運動方向を決定するものを主仮足、それ以外のものを副仮足(亜仮足)と呼び、副仮足はさらに長さに制限がない非限定仮足(indeterminate pseudopod)と長さが決まっている限定仮足(determinate pseudopod)とに区別される。
多細胞動物においても、マクロファージやニューロンを始めとする遊走性細胞の多くは仮足によって運動する。創傷治癒の過程では成長因子の刺激を受けた繊維芽細胞が糸状仮足(フィロポディア、filopodium)を出して活性化し、損傷部位に移動して増殖することで傷を埋める。神経軸索や樹状突起の先端にある成長円錐からも、膜状仮足(または葉状仮足、ラメリポディア、lamellipodium)や糸状仮足が出て軸索伸長に関わっていると考えられている。ガン細胞の浸潤も膜状仮足の働きによることが知られている。
また仮足によって固形物を包みこんで細胞内に取り入れる現象を食作用といい、様々な原生生物で見られるほか、多細胞生物でもマクロファージのような細胞が食作用を行う。」
3.コロナワクチンの「抗体依存性感染増強(ADE)」との関係
補体系はその免疫反応が過剰になると、多くの病気の原因になるとも考えられています。例えば喘息、糸球体腎炎、様々な関節炎、多発性硬化症、炎症性大腸炎などです。またアルツハイマー病やその他の中枢神経系の病気にも、補体系が関与しているのではないかと見られているようです。
さらに、今回のコロナワクチンでも補体による過剰な免疫反応により「抗体依存性感染増強(ADE)」になるのではないかと懸念されています。
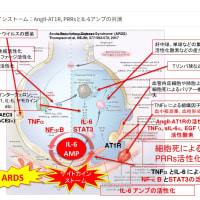
「(2)サイトカインストーム(炎症反応)
コロナ(スパイクタンパク質)抗体とコロナウイルス(スパイクタンパク質)が結合した抗原抗体複合体により、補体が活性化され抗体抗原複合体が攻撃されます。またこの抗原抗体複合体がマクロファージなどFc受容体をもっている細胞とさらに結合すると、サイトカインが過剰に分泌されて炎症反応を引き起こすことがあります。それが続くとサイトカインストームとなり次から次へと炎症が起こり、慢性炎症につながることもあるようです。慢性炎症になると、細胞が壊れて線維化していき、臓器は機能不全になるようです。」
コロナ(スパイクタンパク質)抗体とコロナウイルス(スパイクタンパク質)が結合した抗原抗体複合体により、補体が活性化され抗体抗原複合体が攻撃されます。またこの抗原抗体複合体がマクロファージなどFc受容体をもっている細胞とさらに結合すると、サイトカインが過剰に分泌されて炎症反応を引き起こすことがあります。それが続くとサイトカインストームとなり次から次へと炎症が起こり、慢性炎症につながることもあるようです。慢性炎症になると、細胞が壊れて線維化していき、臓器は機能不全になるようです。」
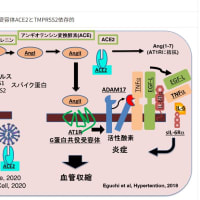
「…やっかいなことにコロナウイルスではACE2を介さずに感染するFc受容体依存性感染が起こり得ます。
ウイルスに結合した抗体が、マクロファージなど免疫細胞の表面にあるFc受容体に結合すると、細胞内にウイルスが侵入します。免疫細胞がもつエンドサイトーシスという細胞外の物質を取り込む作用を利用しています。そうして取り込まれたウイルスが免疫細胞で増殖するとADEが起こります。
…スパイクタンパク質やウイルス、そして特異抗体(特定の抗原に特異的に結合する抗体)がたくさんあるとどのようなことが起きるかというと、抗体を介してスパイクタンパク質やウイルスが結合し合って、団子状態になります。これを抗原抗体複合体と呼びます。
このようにして抗体と新型コロナウイルス(またはスパイクタンパク質)が集まった抗体抗原複合体が形成されると、そこに補体という物質が集まってきて補体自身が活性化されます。活性化した補体は抗原抗原複合体にある細胞膜に穴をあけて壊します。また、抗原抗体複合体がマクロファージなどFc受容体をもっている細胞と結合すると、サイトカインが過剰に分泌され、高熱や激しい炎症反応を起こすことがあります。最悪の場合、サイトカインストーム(サイトカインの大量産生による障害)を引き起こす可能性も出てきます。(『ウイルス学者の絶望』より引用終わり)」
ウイルスに結合した抗体が、マクロファージなど免疫細胞の表面にあるFc受容体に結合すると、細胞内にウイルスが侵入します。免疫細胞がもつエンドサイトーシスという細胞外の物質を取り込む作用を利用しています。そうして取り込まれたウイルスが免疫細胞で増殖するとADEが起こります。
…スパイクタンパク質やウイルス、そして特異抗体(特定の抗原に特異的に結合する抗体)がたくさんあるとどのようなことが起きるかというと、抗体を介してスパイクタンパク質やウイルスが結合し合って、団子状態になります。これを抗原抗体複合体と呼びます。
このようにして抗体と新型コロナウイルス(またはスパイクタンパク質)が集まった抗体抗原複合体が形成されると、そこに補体という物質が集まってきて補体自身が活性化されます。活性化した補体は抗原抗原複合体にある細胞膜に穴をあけて壊します。また、抗原抗体複合体がマクロファージなどFc受容体をもっている細胞と結合すると、サイトカインが過剰に分泌され、高熱や激しい炎症反応を起こすことがあります。最悪の場合、サイトカインストーム(サイトカインの大量産生による障害)を引き起こす可能性も出てきます。(『ウイルス学者の絶望』より引用終わり)」



















※コメント投稿者のブログIDはブログ作成者のみに通知されます