以前、下記の記事等で紹介したエピディオレックス(Epidiolex)に関する評価が、2018年4月19日、米国の医薬品審査を行うFDAの専門委員会で行われ、満場一致でレノックス-がストー症候群とドラベ症候群の治療に対しての承認が推奨されました。
米国における大麻成分を利用した抗てんかん薬、エピディオレックス(Epidiolex)の開発状況について


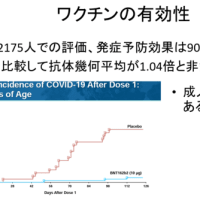
エピディオレックスは2歳以上で使用する経口薬で、これまでの臨床研究では、使用者で痙攣発作の頻度を約40%減らす効果が示されてきた。副作用には、不眠、消化器症状、肝障害等が報告されている。
最終的なFDAによる承認の決定は今年の6月下旬になると予想されている。
もし承認されれば、米国で最初の大麻(マリファナ)成分を使った医薬品となる。
FDA Advisers Recommend Approval of Cannabis-Based Drug for Seizures
Panel recommends FDA approval of epilepsy drug derived from marijuana
FDAで承認されれば、現在、国内で臨床治験を行っているブコラム同様に、医療上の必要性の高い未承認薬・適応外薬の要望募集制度を利用して、国内でのこの薬剤の開発を厚生労働省を通じて検討してもらうことが可能となる。
関連記事