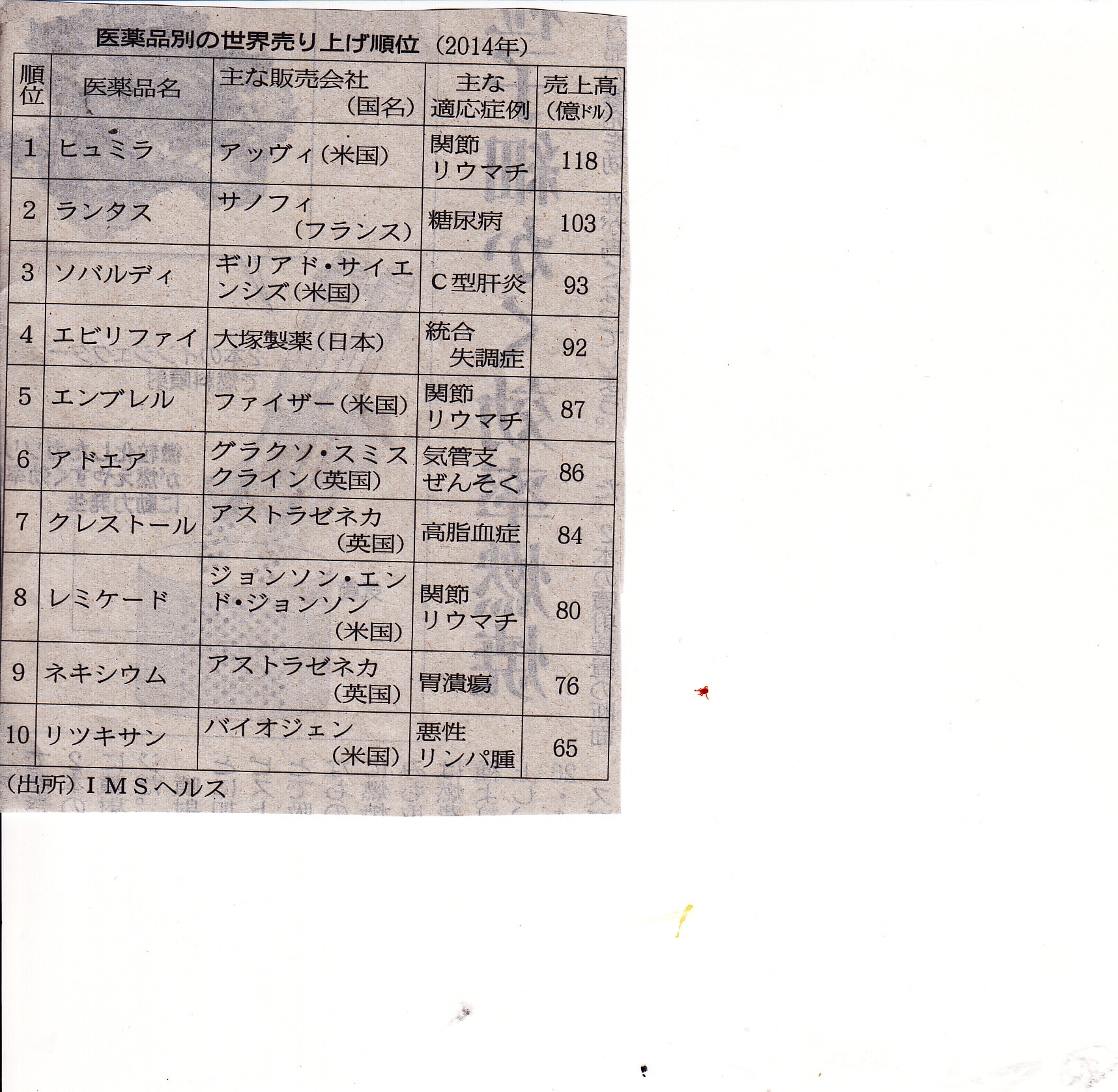
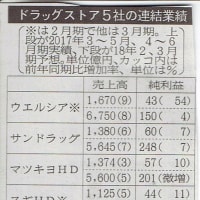
*エピリファイの15/1~3月の売り上は、前年同期比+11%,3851億円、4~12期は5074億円、大塚の全売り上の4割を占める、特許が切れると売り上は最大,10/1に縮小する、
WSJ、米食品医薬品局(FDA)は28日、統合失調症などを治療する非定型抗精神病薬「エビリファイ」(一般名:アリピプラゾール)について、後発薬企業からの4件の簡略承認申請を承認したと発表した。大塚は当局との長期化した異例の法廷闘争を経て、後発版が承認されたことに衝撃を受けている。
大塚HD株価推移 3,811前日比-28.5(-0.74%)
この発表の直後、イスラエルの製薬大手テバ・ファーマシューティカル・インダストリーズは後発版を発売することを明らかにした。
大塚は複雑な規制上の法律を引用して後発版の承認を阻もうとしたが、FDAは大塚の主張を却下し、後発版は承認の基準を満たしているとする判断を示した。
大塚の取り組みが注視されていたのは、これが成功した場合、他の製薬大手が後発版を阻むために同様の戦略を取る可能性があったためだ。安価な後発版の発売が遅れれば、消費者の医療費がかさむことになる。14年のエビリファイの米国売上高は49億ドル(約5838億円)と、大塚にとって巨額の収益がかかる案件でもある。
FDAは昨年、チック症を伴う神経組織の疾患であるトゥレット症候群の小児向け治療にもエビリファイを承認し、同薬を希少病の新薬の開発を促す制度の「オーファンドラッグ」に指定した。このため大塚は米国でさらに7年間の先発権(ODE)保護を取得した。後発版が発売されるのは21年後半以降となった。
ところがFDAは2月、エビリファイをトゥレット症候群の成人向けにも適応を拡大し、大塚を驚かせた。これにより同薬の市場は拡大するものの、FDAの判断は後発版の導入につながるラベル変更の引き金となると大塚は主張する。大塚は、製薬会社が申請していない適応症をFDAが承認することは許されていないと主張し、FDAが後発薬を招き入れようとしているとして提訴した。
FDAは4月に入り、大塚に対して、エビリファイはトゥレット症候群向けにも承認されているが小児に限るとしてそれまでの見解を撤回した。ただトゥレット症候群以外の精神障害を治療する後発版を承認するため、ODEで保護されているトゥレット症候群をラベルから除外する「カーブアウト」アプローチを使う可能性も示唆した。28日の後発版承認はまさにそれだった。
FDAは大塚への書簡で、「後発版エビリファイはトゥレット症候群の小児向けの適応が省かれたラベルとなるが、それ以外の適応症で安全性・有効性は変わらない」と述べた。
*日経の記事は、FDAの大塚への判断には、大塚は市場の独占維持をもくろむもの,だと批判している、これは大塚の提訴レベルとは異なるもので、社会的次元を法律に持ち込むものだ、
*日経、15/5/12