「ワニの涙」の治療について相談を受けました.「ワニの涙」もしくは「ワニの涙症候群」は顔面神経麻痺から回復した患者さんが,食事中に涙を流す症候として有名です.1926年,ロシアの神経病理学者F.A.ボーゴラッドが,論文のタイトルに「ワニの涙症候群」を用いたため,ボーゴラッド症候群とも呼ばれます.顔面神経麻痺の合併症の1つで,発症から6~9ヵ月後に出現し,頻度は3.3%という報告があります.この印象的な名称は「ワニは食事中に泣く」という古い俗説に由来します.1400年に出版され,広く読まれた『ジョン・マンデヴィル卿の航海と旅』という本の一節「その国にはワニがたくさんいる・・・このワニは人を殺し,泣きながら食べるのだ」から広まったとの記載を見つけました.
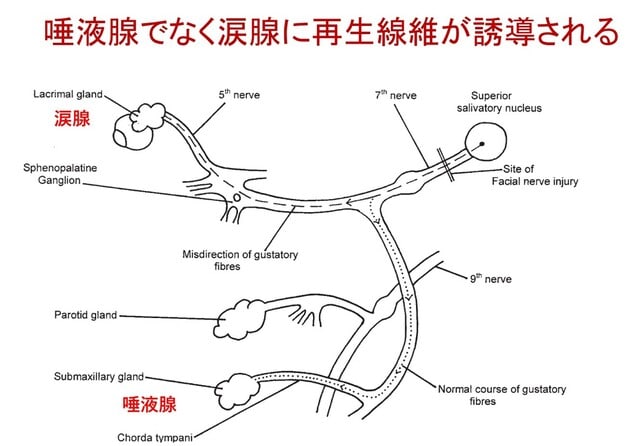
「ワニの涙」のメカニズムは,顔面神経障害後の再生神経線維が,回復過程で,顎下腺から涙腺へと誤って誘導され,その結果,咀嚼や味覚刺激の際に,唾液分泌の代わりに涙液分泌が起こると考えられています.
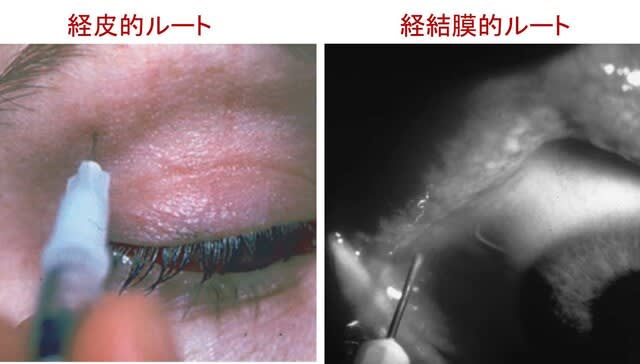
私はこの治療について相談を受けたことは初めてで,調べてみたところ,過去には涙腺の部分切除も行われたようですが,ボツリヌス毒素注射による治療が最も一般的なようです.ただ根拠となっている論文は,対象が4人のみの症例集積研究で,平均20単位のA型ボツリヌス毒素を涙腺に注射したところ,流涙の一部または完全な減少を全例で認めたというものでした.評価は味覚刺激時のシルマーテストを行っています.効果発現は注射から24~48時間後で,4~5ヵ月持続したそうです.経皮的ないし経結膜的に注射できますが,経結膜的ルートのほうが合併症は少ないそうです.★このような治療の経験のおありの先生はおいででしょうか?
Montoya FJ et al. Eye (Lond). 2002 Nov;16(6):705-9.
それにしても「ワニは食事中に本当に泣くのだろうか?」と考えてしまいました.私と同じことを疑問に思った脳神経内科医はやはりいたようで,2006年,D. Malcolm Shaner医師は動物学者に依頼し,カイマンワニ7匹中5匹が涙を流しながら餌を食べることを確認し,逸話が事実であることを論文報告しています!論文の中で「泣くという現象は,食事中,温風がシューという音を出しながら副鼻腔を通ることにより,涙腺が刺激され,目に涙液が送られることで発生した可能性」を議論しています.疑問を徹底的に検証するこの先生の姿勢は嫌いじゃありません(笑).
Shaner DM. et al. BioScience 57;615–617,2007

「ワニの涙」のメカニズムは,顔面神経障害後の再生神経線維が,回復過程で,顎下腺から涙腺へと誤って誘導され,その結果,咀嚼や味覚刺激の際に,唾液分泌の代わりに涙液分泌が起こると考えられています.

私はこの治療について相談を受けたことは初めてで,調べてみたところ,過去には涙腺の部分切除も行われたようですが,ボツリヌス毒素注射による治療が最も一般的なようです.ただ根拠となっている論文は,対象が4人のみの症例集積研究で,平均20単位のA型ボツリヌス毒素を涙腺に注射したところ,流涙の一部または完全な減少を全例で認めたというものでした.評価は味覚刺激時のシルマーテストを行っています.効果発現は注射から24~48時間後で,4~5ヵ月持続したそうです.経皮的ないし経結膜的に注射できますが,経結膜的ルートのほうが合併症は少ないそうです.★このような治療の経験のおありの先生はおいででしょうか?
Montoya FJ et al. Eye (Lond). 2002 Nov;16(6):705-9.

それにしても「ワニは食事中に本当に泣くのだろうか?」と考えてしまいました.私と同じことを疑問に思った脳神経内科医はやはりいたようで,2006年,D. Malcolm Shaner医師は動物学者に依頼し,カイマンワニ7匹中5匹が涙を流しながら餌を食べることを確認し,逸話が事実であることを論文報告しています!論文の中で「泣くという現象は,食事中,温風がシューという音を出しながら副鼻腔を通ることにより,涙腺が刺激され,目に涙液が送られることで発生した可能性」を議論しています.疑問を徹底的に検証するこの先生の姿勢は嫌いじゃありません(笑).
Shaner DM. et al. BioScience 57;615–617,2007