進行性核上性麻痺(PSP)にはさまざまな亜型(異型症候群)があります.前頭葉徴候を主体とするものとして,PSP-F(frontal presentation)やPSP-SL(speech/language disorder)があります.しかし病理学的に診断された症例の検討は極めて稀で,臨床像の経的変化についてはほとんど分かっていません.今回,当科の大野陽哉先生,東田和博先生らが中心となり,PSP-Fの臨床像を報告しました.以下のようなサマリーです.
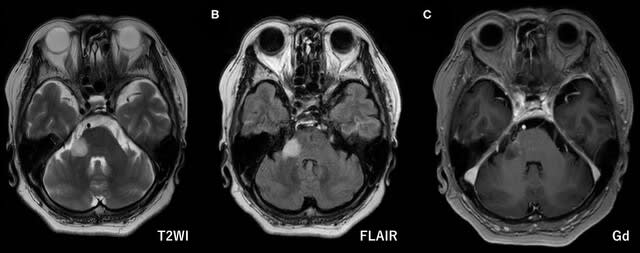
77歳の右利きの男性.69歳から進行性非流暢性失語(PNFA)にて発症.75歳から加速歩行と左上肢の拙劣さ,76歳から脱抑制,77歳で転倒を認めた.77歳時,左上下肢の肢節運動失行,筋強剛,皮質性感覚障害,垂直性核上性注視麻痺を認めた.MDS-PSP基準では,9年をかけてsuggestive of PSP-SLからprobable PSP-Fに移行した(図).頭部MRIでは第3脳室拡大,中脳被蓋萎縮に加え右優位の大脳萎縮を,脳血流シンチでも右前頭・頭頂・側頭葉の集積低下を認めた.病理学的には,前頭葉を中心に4リピート・タウ陽性神経原線維変化,coiled body,tufted astrocyte等を認めた.黒質,青斑核,視床下核のタウ病理は軽度であった.以上より,タウ病理の局在は右弁蓋部から,中心前回,前頭前野,脳幹に波及したものと考えられた.またPSP-Fは交差性失語を呈しうることを示した.

少し解説が必要なのは「交叉性失語」です.つまり右利きの右大脳病変で失語を呈したことを意味します.利き手と反対側が優位脳で言語中枢があるという定説がありますが,第二次世界大戦時,左利きで左脳の戦傷者の失語症が報告され,優位脳と利き手の原則は崩れ,以後,同様の症例が相次ぎました.これら原則に反する失語を「交叉性失語」と呼ぶわけです(また脳に優劣はないので,最近は言語脳と視空間脳のような表現をします).
本論文の強みは,PSP-Fにおけるタウ病理の進展様式を,詳細な症候の観察から考察した点です.CPCの際,大野先生は愛知医大吉田眞理教授にとても褒められていました.専攻医ながら立派な症例報告を書けるようになりつつあり嬉しいです.岐阜は人口当たりの専門医数では最下位ですが,これからどんどん実力のある専門医が育つものと期待しております.
Ono Y, Higashida K, Yoshikura N, Hayashi Y, Kimura A, Iwasaki Y, Yoshida M, Shimohata T. Progressive supranuclear palsy with predominant frontal presentation exhibiting progressive nonfluent aphasia due to crossed aphasia. Neuropathology. 2022 Apr 17.
77歳の右利きの男性.69歳から進行性非流暢性失語(PNFA)にて発症.75歳から加速歩行と左上肢の拙劣さ,76歳から脱抑制,77歳で転倒を認めた.77歳時,左上下肢の肢節運動失行,筋強剛,皮質性感覚障害,垂直性核上性注視麻痺を認めた.MDS-PSP基準では,9年をかけてsuggestive of PSP-SLからprobable PSP-Fに移行した(図).頭部MRIでは第3脳室拡大,中脳被蓋萎縮に加え右優位の大脳萎縮を,脳血流シンチでも右前頭・頭頂・側頭葉の集積低下を認めた.病理学的には,前頭葉を中心に4リピート・タウ陽性神経原線維変化,coiled body,tufted astrocyte等を認めた.黒質,青斑核,視床下核のタウ病理は軽度であった.以上より,タウ病理の局在は右弁蓋部から,中心前回,前頭前野,脳幹に波及したものと考えられた.またPSP-Fは交差性失語を呈しうることを示した.

少し解説が必要なのは「交叉性失語」です.つまり右利きの右大脳病変で失語を呈したことを意味します.利き手と反対側が優位脳で言語中枢があるという定説がありますが,第二次世界大戦時,左利きで左脳の戦傷者の失語症が報告され,優位脳と利き手の原則は崩れ,以後,同様の症例が相次ぎました.これら原則に反する失語を「交叉性失語」と呼ぶわけです(また脳に優劣はないので,最近は言語脳と視空間脳のような表現をします).
本論文の強みは,PSP-Fにおけるタウ病理の進展様式を,詳細な症候の観察から考察した点です.CPCの際,大野先生は愛知医大吉田眞理教授にとても褒められていました.専攻医ながら立派な症例報告を書けるようになりつつあり嬉しいです.岐阜は人口当たりの専門医数では最下位ですが,これからどんどん実力のある専門医が育つものと期待しております.
Ono Y, Higashida K, Yoshikura N, Hayashi Y, Kimura A, Iwasaki Y, Yoshida M, Shimohata T. Progressive supranuclear palsy with predominant frontal presentation exhibiting progressive nonfluent aphasia due to crossed aphasia. Neuropathology. 2022 Apr 17.