今回のキーワードは,人が集まるイベントでは(たとえ誕生日であっても)感染者が増加する,感染6ヶ月後の評価で,Long COVIDによる症状の持続は自宅療養の若年者の52%に見られる,神経症状を認めなくても,全身の炎症は脳内に伝わり,神経変性疾患様の変化をもたらす,成人でも多系統炎症性症候群(MIS-A)が生じうる,SARS-CoV-2ウイルスにより抑制されるオートファジーを標的とする薬剤は,その増殖を抑える,イベルメクチンはCOVID-19 による死亡リスクを62%減少させる,です.
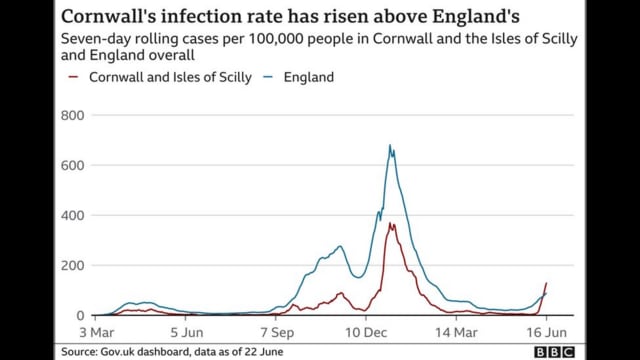
人の集まりでCOVID-19感染が増加する身近な例として,米国から誕生日が報告されました.人の集まりで感染が増加する別の事例として,6月11~13日にG7を行った英国コーンウォールにおける,デルタ株による新規感染者の激増が報道されています(図).英国全体でデルタ株頻度は90%まで増加し,ほぼ置き換わっていますが,ワクチン接種率が80%以上と高いため感染者は増えても死亡者数は増加していない状況のようです.しかしワクチン接種が進んでいない国に,感染率,重症化率とも高いと指摘されているデルタ株が流入すれば甚大な被害がもたらされる可能性が高いと考えられます.「デルタ株の国内流入を防ぐ」ことはオリンピックを安全安心に開催する条件であり,それができるかどうかが問われていると思います.
◆人が集まるイベントでは(たとえ誕生日であっても)感染者が増加する.
人が集まるイベントは,COVID-19感染者を増加させるかどうかを,分かりやすいように誕生日を例として検討した米国からの報告.調査対象となったのは290万世帯.感染状況によっても異なるため,感染状況を10段階に分類して検討した.最も感染状況が不良の地域において,2週間前に誕生日を迎えた世帯は,誕生日がなかった世帯と比較して感染者が31%増加していた.また子供の誕生日後に感染者数は1万人あたり15.8人増加したのに対し,大人の誕生日では5.8人の増加にとどまった(図1).→ 日本と比べて米国では子供の誕生日はまさに一大イベントである.パンデミック禍であっても子供のために行動変容ができていないことを意味している.
JAMA Intern Med. 2021 Jun 21.(doi.org/10.1001/jamainternmed.2021.2915)

◆感染6ヶ月後の評価で,Long COVIDによる症状の持続は自宅療養の若年者の52%に見られる.
ノルウェーでの第1波の際にCOVID-19に罹患したベルゲン地域の312名の患者(自宅隔離患者247名,入院患者65名)を対象として,前向きに長期追跡調査を行った.6ヵ月後の時点で,全患者の61%(189/312)が持続的な症状を呈していた.これらの症状は,初期症状の重症度,回復期の抗体価の上昇,既存の慢性肺疾患と関連していた.16~30歳の重症でない自宅療養の若年層の52%(32/61名)が6ヵ月後でも症状を呈しており,味覚・嗅覚障害(28%,17/61名),疲労感(21%,13/61名),呼吸困難(13%,8/61名),集中力低下(13%,8/61名),記憶障害(11%,7/61名)などの症状を認めた.15歳までの非入院小児も16名中2名(13%)が6か月時点で胃の違和感や味覚・嗅覚障害を呈していた.→ 軽症の若年患者でも,呼吸困難や認知障害が長期に渡って続くリスクがある.若年者でもワクチン接種などの感染対策は重要である.
Nat Med. June 23, 2021.(doi.org/10.1038/s41591-021-01433-3)
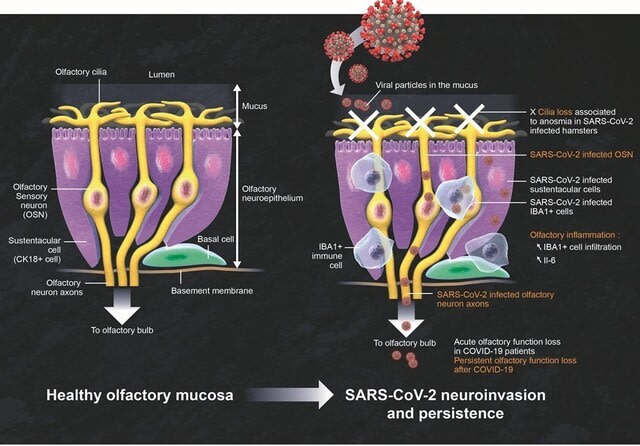
◆神経症状を認めなくても,全身の炎症は脳内に伝わり,神経変性疾患様の変化をもたらす.
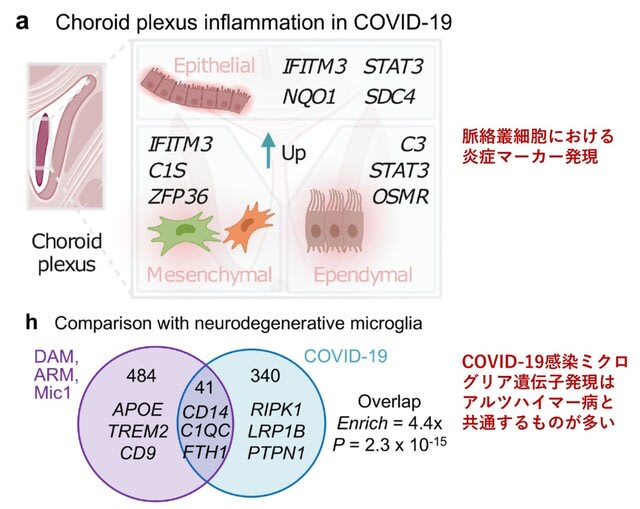
米国スタンフォード大学からの研究.COVID-19患者8名と対照群14名の前頭葉皮質および脈絡叢から得られた65,309個の単一核トランスクリプトームを,シングルセルRNAシーケンサーを用いて比較した.まず脳内にSARS-CoV-2ウイルス感染を示す所見は認めなかった.しかし重症COVID-19で死亡した患者脳には,臨床的に神経症状を認めない場合でも,脳内の炎症に関わる分子マーカーの発現が顕著に認められた.脳外に存在する何らかの血中因子が,血液脳関門を介して脳内に炎症を引き起こすことが示唆された.また,COVID-19に関連したミクログリアやアストロサイトの遺伝子変化は,アルツハイマー病やパーキンソン病などの神経変性疾患で報告されているものと共通する所見であった(図2).さらにCOVID-19患者の大脳皮質の一番外層では,興奮性ニューロンによるシグナル伝達が抑制され,抑制性ニューロンによるシグナル伝達が亢進していた.このようなシグナル伝達の不均衡は,アルツハイマー病などの神経変性疾患と共通していた.またCOVID-19患者脳では通常,健常者では認めないT細胞が有意に増加していた.以上より,SARS-CoV-2ウイルス感染は全身の炎症反応を引き起こし,それが脈絡叢細胞を介して血液脳関門を越えた炎症シグナルをもたらし,脳内の神経炎症や神経変性疾患類似の変化をもたらす可能性がある.COVID-19患者の多くが,脳霧や認知機能障害などの神経系症状を訴えるメカニズムを説明できるかもしれない.
Nature. June 21, 2021.(doi.org/10.1038/s41586-021-03710-0)
◆成人でも多系統炎症性症候群(MIS-A)が生じうる.
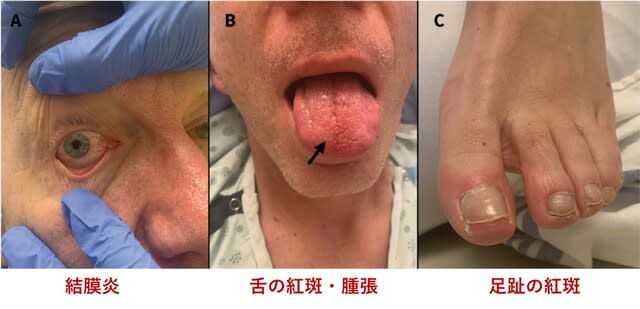
小児 COVID-19 関連多系統炎症性症候群(MIS-C)は,主にSARS-CoV-2に感染した子供や青年に見られる,珍しいが重篤な合併症である.川崎病の主要症状(発熱,発疹,眼球結膜充血,口唇口腔所見,四肢末端の腫脹,頸部リンパ節腫脹)を認める.新しい疾患概念であり,診断が難しく治療法は定まっていないが,病態は多系統にわたり集学的な医療が必要となる.カナダからMIS-Cの診断基準を満たす成人の多臓器炎症症候群(MIS-A;multisystem inflammatory syndrome in adults)60歳男性例が報告された.感染からの回復後(4週後),5日間の息切れ,極度の疲労感,食欲不振,発熱を呈して救急外来を受診した.結膜炎,舌の紅斑・腫脹,足趾の紅斑(図3)や多臓器病変が認められ,MIS-Aと考えられた.アスピリン,ステロイド,免疫グロブリン静注を行ったところ,開始24時間以内に症状の改善がみられ,入院5日目に退院した.過去にも米国疾病管理センター(CDC)はMIS-Aの27名を報告している.
CMAJ June 21, 2021 193 (25) E956-E961(doi.org/10.1503/cmaj.210232)
◆SARS-CoV-2ウイルスにより抑制されるオートファジーを標的とする薬剤は,その増殖を抑える.
「オートファジー」は,細胞が自らの一部を分解する作用(自食作用)のことである.細胞内物質の処理やリサイクルなどにも役立っている.ドイツからの研究で,SARS-CoV-2ウイルス感染は細胞のオートファジーを抑制し,その結果,過剰な炎症反応や自己免疫反応が引き起こされる可能性が報告された.そして複合的な方法でオートファジーを誘導すると,ウイルスの伝播を抑制できることを示した.具体的には,SARS-CoV-2感染細胞ではAKT1のようなオートファジー阻害因子の活性化が生じていること,ならびにオートファジーの開始に関わるタンパク質,膜核形成,隔離膜形成に関わるタンパク質,オートファゴソームとリソソームの融合に関わるタンパク質が減少していることが示された.この結果,隔離膜に取り込まれたオートファジーマーカーであるLC3B-IIとP62が蓄積することが,ハムスターモデルとCOVID-19患者の肺サンプルで確認された.一方,ポリアミンのスペルミジンとスペルミン,選択的なAKT1阻害剤MK-2206,BECN1を安定化剤ニクロサミドは,ウイルス増殖をin vitroで阻害した.つまりオートファジー誘導化合物は治療薬となる可能性があり,とくに駆虫薬であるニクロサミドは有望で,臨床試験がすでに開始されている.
Nat Commun 12, 3818 (2021).(doi.org/10.1038/s41467-021-24007-w)
◆イベルメクチンはCOVID-19 による死亡リスクを62%減少させる.
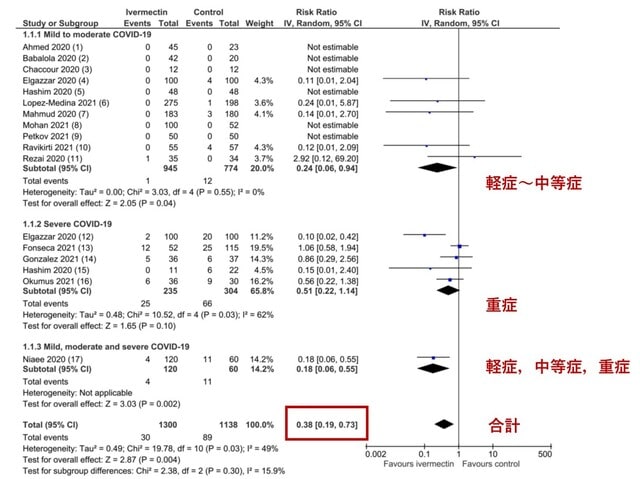
イベルメクチンのCOVID-19に対する有効性をメタ解析により評価した論文が報告された.死亡率の低下,副次的なアウトカム等について評価した.3406名の参加者を対象とした24の無作為化比較試験がレビューの対象となった.最終的に15試験のメタ解析により,イベルメクチン群は,非使用群と比較して,死亡リスクを62%低下させた!(平均リスク比0.38,95%信頼区間0.19-0.73,n=2438,I2=49%,確実性が中程度のエビデンス;図4).イベルメクチンの予防投与により,COVID-19感染が平均86%(95%信頼区間79%~91%)減少した(確実性が低いエビデンス).副次評価項目では「人工呼吸の必要性」についてはイベルメクチンの有益性がない可能性が示唆された(確実性が低いエビデンス).重篤な有害事象はまれであり,コストも安価なことから,イベルメクチンはCOVID-19の治療を大きく変える可能性がある.
Am J Ther. June 17, 2021(doi.org/10.1097/MJT.0000000000001402)
人の集まりでCOVID-19感染が増加する身近な例として,米国から誕生日が報告されました.人の集まりで感染が増加する別の事例として,6月11~13日にG7を行った英国コーンウォールにおける,デルタ株による新規感染者の激増が報道されています(図).英国全体でデルタ株頻度は90%まで増加し,ほぼ置き換わっていますが,ワクチン接種率が80%以上と高いため感染者は増えても死亡者数は増加していない状況のようです.しかしワクチン接種が進んでいない国に,感染率,重症化率とも高いと指摘されているデルタ株が流入すれば甚大な被害がもたらされる可能性が高いと考えられます.「デルタ株の国内流入を防ぐ」ことはオリンピックを安全安心に開催する条件であり,それができるかどうかが問われていると思います.

◆人が集まるイベントでは(たとえ誕生日であっても)感染者が増加する.
人が集まるイベントは,COVID-19感染者を増加させるかどうかを,分かりやすいように誕生日を例として検討した米国からの報告.調査対象となったのは290万世帯.感染状況によっても異なるため,感染状況を10段階に分類して検討した.最も感染状況が不良の地域において,2週間前に誕生日を迎えた世帯は,誕生日がなかった世帯と比較して感染者が31%増加していた.また子供の誕生日後に感染者数は1万人あたり15.8人増加したのに対し,大人の誕生日では5.8人の増加にとどまった(図1).→ 日本と比べて米国では子供の誕生日はまさに一大イベントである.パンデミック禍であっても子供のために行動変容ができていないことを意味している.
JAMA Intern Med. 2021 Jun 21.(doi.org/10.1001/jamainternmed.2021.2915)

◆感染6ヶ月後の評価で,Long COVIDによる症状の持続は自宅療養の若年者の52%に見られる.
ノルウェーでの第1波の際にCOVID-19に罹患したベルゲン地域の312名の患者(自宅隔離患者247名,入院患者65名)を対象として,前向きに長期追跡調査を行った.6ヵ月後の時点で,全患者の61%(189/312)が持続的な症状を呈していた.これらの症状は,初期症状の重症度,回復期の抗体価の上昇,既存の慢性肺疾患と関連していた.16~30歳の重症でない自宅療養の若年層の52%(32/61名)が6ヵ月後でも症状を呈しており,味覚・嗅覚障害(28%,17/61名),疲労感(21%,13/61名),呼吸困難(13%,8/61名),集中力低下(13%,8/61名),記憶障害(11%,7/61名)などの症状を認めた.15歳までの非入院小児も16名中2名(13%)が6か月時点で胃の違和感や味覚・嗅覚障害を呈していた.→ 軽症の若年患者でも,呼吸困難や認知障害が長期に渡って続くリスクがある.若年者でもワクチン接種などの感染対策は重要である.
Nat Med. June 23, 2021.(doi.org/10.1038/s41591-021-01433-3)
◆神経症状を認めなくても,全身の炎症は脳内に伝わり,神経変性疾患様の変化をもたらす.
米国スタンフォード大学からの研究.COVID-19患者8名と対照群14名の前頭葉皮質および脈絡叢から得られた65,309個の単一核トランスクリプトームを,シングルセルRNAシーケンサーを用いて比較した.まず脳内にSARS-CoV-2ウイルス感染を示す所見は認めなかった.しかし重症COVID-19で死亡した患者脳には,臨床的に神経症状を認めない場合でも,脳内の炎症に関わる分子マーカーの発現が顕著に認められた.脳外に存在する何らかの血中因子が,血液脳関門を介して脳内に炎症を引き起こすことが示唆された.また,COVID-19に関連したミクログリアやアストロサイトの遺伝子変化は,アルツハイマー病やパーキンソン病などの神経変性疾患で報告されているものと共通する所見であった(図2).さらにCOVID-19患者の大脳皮質の一番外層では,興奮性ニューロンによるシグナル伝達が抑制され,抑制性ニューロンによるシグナル伝達が亢進していた.このようなシグナル伝達の不均衡は,アルツハイマー病などの神経変性疾患と共通していた.またCOVID-19患者脳では通常,健常者では認めないT細胞が有意に増加していた.以上より,SARS-CoV-2ウイルス感染は全身の炎症反応を引き起こし,それが脈絡叢細胞を介して血液脳関門を越えた炎症シグナルをもたらし,脳内の神経炎症や神経変性疾患類似の変化をもたらす可能性がある.COVID-19患者の多くが,脳霧や認知機能障害などの神経系症状を訴えるメカニズムを説明できるかもしれない.
Nature. June 21, 2021.(doi.org/10.1038/s41586-021-03710-0)

◆成人でも多系統炎症性症候群(MIS-A)が生じうる.
小児 COVID-19 関連多系統炎症性症候群(MIS-C)は,主にSARS-CoV-2に感染した子供や青年に見られる,珍しいが重篤な合併症である.川崎病の主要症状(発熱,発疹,眼球結膜充血,口唇口腔所見,四肢末端の腫脹,頸部リンパ節腫脹)を認める.新しい疾患概念であり,診断が難しく治療法は定まっていないが,病態は多系統にわたり集学的な医療が必要となる.カナダからMIS-Cの診断基準を満たす成人の多臓器炎症症候群(MIS-A;multisystem inflammatory syndrome in adults)60歳男性例が報告された.感染からの回復後(4週後),5日間の息切れ,極度の疲労感,食欲不振,発熱を呈して救急外来を受診した.結膜炎,舌の紅斑・腫脹,足趾の紅斑(図3)や多臓器病変が認められ,MIS-Aと考えられた.アスピリン,ステロイド,免疫グロブリン静注を行ったところ,開始24時間以内に症状の改善がみられ,入院5日目に退院した.過去にも米国疾病管理センター(CDC)はMIS-Aの27名を報告している.
CMAJ June 21, 2021 193 (25) E956-E961(doi.org/10.1503/cmaj.210232)

◆SARS-CoV-2ウイルスにより抑制されるオートファジーを標的とする薬剤は,その増殖を抑える.
「オートファジー」は,細胞が自らの一部を分解する作用(自食作用)のことである.細胞内物質の処理やリサイクルなどにも役立っている.ドイツからの研究で,SARS-CoV-2ウイルス感染は細胞のオートファジーを抑制し,その結果,過剰な炎症反応や自己免疫反応が引き起こされる可能性が報告された.そして複合的な方法でオートファジーを誘導すると,ウイルスの伝播を抑制できることを示した.具体的には,SARS-CoV-2感染細胞ではAKT1のようなオートファジー阻害因子の活性化が生じていること,ならびにオートファジーの開始に関わるタンパク質,膜核形成,隔離膜形成に関わるタンパク質,オートファゴソームとリソソームの融合に関わるタンパク質が減少していることが示された.この結果,隔離膜に取り込まれたオートファジーマーカーであるLC3B-IIとP62が蓄積することが,ハムスターモデルとCOVID-19患者の肺サンプルで確認された.一方,ポリアミンのスペルミジンとスペルミン,選択的なAKT1阻害剤MK-2206,BECN1を安定化剤ニクロサミドは,ウイルス増殖をin vitroで阻害した.つまりオートファジー誘導化合物は治療薬となる可能性があり,とくに駆虫薬であるニクロサミドは有望で,臨床試験がすでに開始されている.
Nat Commun 12, 3818 (2021).(doi.org/10.1038/s41467-021-24007-w)
◆イベルメクチンはCOVID-19 による死亡リスクを62%減少させる.
イベルメクチンのCOVID-19に対する有効性をメタ解析により評価した論文が報告された.死亡率の低下,副次的なアウトカム等について評価した.3406名の参加者を対象とした24の無作為化比較試験がレビューの対象となった.最終的に15試験のメタ解析により,イベルメクチン群は,非使用群と比較して,死亡リスクを62%低下させた!(平均リスク比0.38,95%信頼区間0.19-0.73,n=2438,I2=49%,確実性が中程度のエビデンス;図4).イベルメクチンの予防投与により,COVID-19感染が平均86%(95%信頼区間79%~91%)減少した(確実性が低いエビデンス).副次評価項目では「人工呼吸の必要性」についてはイベルメクチンの有益性がない可能性が示唆された(確実性が低いエビデンス).重篤な有害事象はまれであり,コストも安価なことから,イベルメクチンはCOVID-19の治療を大きく変える可能性がある.
Am J Ther. June 17, 2021(doi.org/10.1097/MJT.0000000000001402)