私どもも協力したIgLON5抗体関連疾患に関する研究がBrain誌に報告されました.本症のHLA関連解析としては最大規模の報告で,研究の強みは複数の異なる民族の患者を組み入れたことです.研究を主導したスタンフォード睡眠医学センターEmmanuel Mignot教授には,留学中,ラボを見せていただいたり,ランチをご馳走になったことがあります.20年後に共同研究をさせていただくとは不思議なご縁だと思いました.
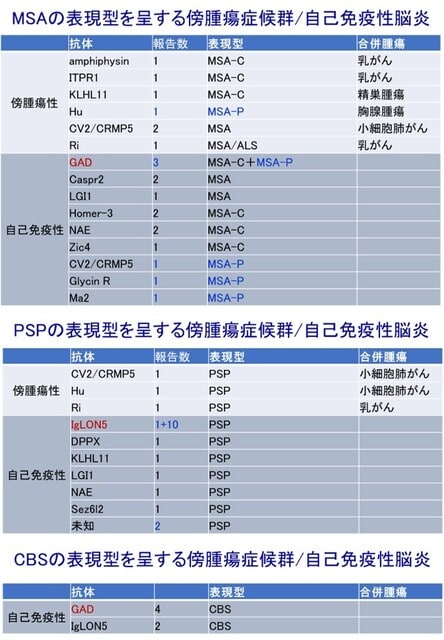
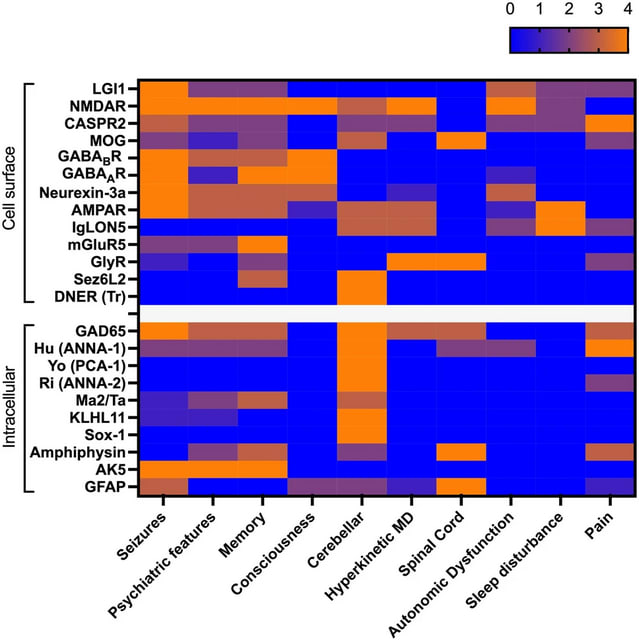
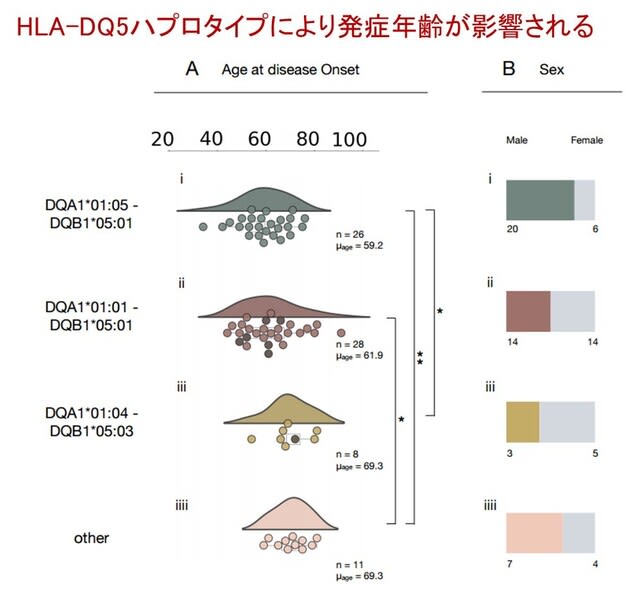
さてIgLON5抗体関連疾患ですが,慢性の経過で睡眠障害,運動異常症,球麻痺などの多彩な表現型を呈し,神経変性疾患との鑑別を要する自己免疫性脳炎です.HLA-DRB1*10:01やDQB1*05:01との関連が報告され,IgLON5抗体の存在とあわせて自己免疫学的機序が示唆されます.本研究の目的は,87人の患者サンプルを用いてGWASとHLA関連解析を行い,HLAペプチド結合候補を調べ,CD4+ T細胞への影響を調べることです.ゲノムワイドな関連を同定するのに87人では力不足に見えますが,HLA遺伝子は多型性が高く,遺伝子内および遺伝子間で強い連鎖不平衡を示すため,サンプルサイズが小さくても強力なマーカーとなります.事実,結果として,HLA-DRよりもHLA-DQとの強い関連が示されました.具体的には3つのHLA-DQ5ハプロタイプ(HLA-DQA1*01:05-05:01,HLA-DQA1*01:01-05:01,HLA-DQA1*01:04-05:03)との関連が,リスクの高い順に全患者の85%(74/87)で認められ,発症年齢に影響していました(図).
つぎにHLA-DQ分子の機能的関連性を,競合結合アッセイで検討しました.IgLON5が3つのリスク関連HLA-DQレセプターすべてに,ネイティブな状態ではなく,いくつかの部位にアスパラギン酸残基が翻訳後修飾(脱アミド化)されたIgLON5ペプチドが結合することが判明しました.この修飾の生理的意味は不明ですが,自己抗原はしばしば翻訳後修飾されることが報告されています(例:関節リウマチでのシトルリン化).HLA-DQ5結合物質として同定された3つの脱アミド化ペプチドは,すべてIgLON5のIg2ドメイン内に認められました.さらにこのIg2ドメインの脱アミド化ペプチドはT細胞を活性化しました.つまり特定のHLA-DQ分子がIgLON5タンパク質の特定のペプチドと結合し,T細胞に提示することが示唆されました.このプロセスが,IgLON5に対する自己免疫反応を引き起こし,病気の発症につながる可能性があります.このような現象の引き金は不明ですが,多発性硬化症におけるEBウイルスや,ナルコレプシーにおけるインフルエンザウイルスなど,いくつかの疾患では外来抗原による分子模倣(molecular mimicry)が強く示唆されています.同様のことがこの疾患でも生じているのかもしれません.
以上,IgLON5抗体関連疾患は主にHLA-DQに関連し,これらの分子により提示される脱アミド化IgLON5配列に向けられたT細胞自己免疫が関与する可能性が初めて示されました.この疾患は表現型が多彩ですが,HLAと表現型の関連をより詳細に検討する必要があると思いました.
Yogeshwar SM, et al. HLA-DQB1*05 subtypes and not DRB1*10:01 mediates risk in anti-IgLON5 disease. Brain. 2024 Mar 1:awae048.(doi.org/10.1093/brain/awae048)
さてIgLON5抗体関連疾患ですが,慢性の経過で睡眠障害,運動異常症,球麻痺などの多彩な表現型を呈し,神経変性疾患との鑑別を要する自己免疫性脳炎です.HLA-DRB1*10:01やDQB1*05:01との関連が報告され,IgLON5抗体の存在とあわせて自己免疫学的機序が示唆されます.本研究の目的は,87人の患者サンプルを用いてGWASとHLA関連解析を行い,HLAペプチド結合候補を調べ,CD4+ T細胞への影響を調べることです.ゲノムワイドな関連を同定するのに87人では力不足に見えますが,HLA遺伝子は多型性が高く,遺伝子内および遺伝子間で強い連鎖不平衡を示すため,サンプルサイズが小さくても強力なマーカーとなります.事実,結果として,HLA-DRよりもHLA-DQとの強い関連が示されました.具体的には3つのHLA-DQ5ハプロタイプ(HLA-DQA1*01:05-05:01,HLA-DQA1*01:01-05:01,HLA-DQA1*01:04-05:03)との関連が,リスクの高い順に全患者の85%(74/87)で認められ,発症年齢に影響していました(図).

つぎにHLA-DQ分子の機能的関連性を,競合結合アッセイで検討しました.IgLON5が3つのリスク関連HLA-DQレセプターすべてに,ネイティブな状態ではなく,いくつかの部位にアスパラギン酸残基が翻訳後修飾(脱アミド化)されたIgLON5ペプチドが結合することが判明しました.この修飾の生理的意味は不明ですが,自己抗原はしばしば翻訳後修飾されることが報告されています(例:関節リウマチでのシトルリン化).HLA-DQ5結合物質として同定された3つの脱アミド化ペプチドは,すべてIgLON5のIg2ドメイン内に認められました.さらにこのIg2ドメインの脱アミド化ペプチドはT細胞を活性化しました.つまり特定のHLA-DQ分子がIgLON5タンパク質の特定のペプチドと結合し,T細胞に提示することが示唆されました.このプロセスが,IgLON5に対する自己免疫反応を引き起こし,病気の発症につながる可能性があります.このような現象の引き金は不明ですが,多発性硬化症におけるEBウイルスや,ナルコレプシーにおけるインフルエンザウイルスなど,いくつかの疾患では外来抗原による分子模倣(molecular mimicry)が強く示唆されています.同様のことがこの疾患でも生じているのかもしれません.
以上,IgLON5抗体関連疾患は主にHLA-DQに関連し,これらの分子により提示される脱アミド化IgLON5配列に向けられたT細胞自己免疫が関与する可能性が初めて示されました.この疾患は表現型が多彩ですが,HLAと表現型の関連をより詳細に検討する必要があると思いました.
Yogeshwar SM, et al. HLA-DQB1*05 subtypes and not DRB1*10:01 mediates risk in anti-IgLON5 disease. Brain. 2024 Mar 1:awae048.(doi.org/10.1093/brain/awae048)