がんの予防や治療における漢方治療の存在意義を考察しています。がん治療に役立つ情報も紹介しています。
「漢方がん治療」を考える
339)膠芽腫(グリオブラストーマ)とFoxO3a
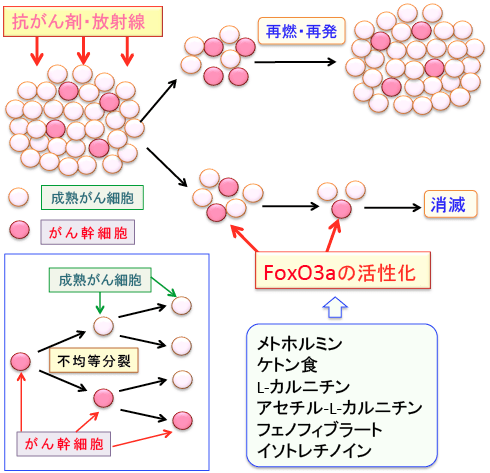
図:膠芽腫(グリオブラストーマ)が再発しやすいのは、がん幹細胞が抗がん剤や放射線治療に抵抗性を示すためである。グリオブラストーマの幹細胞のFoxO3aという転写因子を活性化すると、グリオブラストーマ幹細胞の分化が誘導され、成熟がん細胞と同じように抗がん剤や放射線で死滅しやすくなり、腫瘍形成能を失うので、腫瘍を消滅できるという報告がある。グリオブラストーマ幹細胞のFoxO3aを活性化する方法として、メトホルミン、ケトン食、L-カルニチン、アセチル-L-カルニチン、フェノフィブラート、イソトレチノインなどが報告されており、これらを組み合わせると抗腫瘍効果を高めることができるかもしれない。
339)膠芽腫(グリオブラストーマ)とFoxO3a
【膠芽腫は増殖が早く再発しやすい】
脳には神経細胞と、神経細胞の働きを助ける役割を担っている神経膠細胞(グリア細胞)があります。神経膠細胞から発生する腫瘍を神経膠腫(グリオーマ)と言い、神経膠腫の中で最も悪性度の高い腫瘍が膠芽腫(グリオブラストーマ)です。
膠芽腫は増殖活性が高く、進行が早く、ヒトの悪性腫瘍の中で最も予後不良の腫瘍と言われています。
手術や放射線治療や抗がん剤治療などが行われますが、このような集学的治療をおこなっても平均生存期間は12~14カ月程度であり,治療成績はここ30年以上改善がほとんどないと言われています。
膠芽腫は周囲の脳組織にしみ込むように広がっていくのが特徴で、腫瘍と正常脳との境界が不鮮明となり、そのため手術によって腫瘍を完全に摘出することは極めて困難です。したがって、手術でできるだけ摘出した後に放射線療法と抗がん剤治療が行われます。
しかし、放射線治療や抗がん剤治療によって生き残るがん細胞がいるため、再発しやすいということです。このような「放射線治療や抗がん剤治療によって生き残るがん細胞」として「がん幹細胞」の存在が重要と考えられています。
【がん幹細胞は放射線治療や抗がん剤治療に抵抗性が高い】
組織の細胞には幹細胞(stem cell)と成熟した体細胞が存在します。
組織の幹細胞とは、組織固有の多分化能を有して各臓器・組織を構成する細胞の供給源となる細胞です。
組織幹細胞は自己複製によって幹細胞を維持すると同時に、不均等分裂により一部が自己複製のサイクルから逸脱して成熟細胞へと分化して、組織を構成する細胞(体細胞)を作り出しています。
組織幹細胞は、分裂して自分と同じ細胞を作り出すことができ(自己複製能)、またいろいろな細胞に分化できる(多分化能)という二つの重要な性質を持ち、この性質により、限られた寿命のある体細胞を絶えず供給し、傷ついた組織を修復することができるのです。
がん組織の中には正常組織における幹細胞システムに類似した階層性が存在し、その中にがん幹細胞 (cancer stem cells)と呼べるような細胞が存在して通常のがん細胞を供給しながらがん組織を構成していることが明らかになっています。
すなわち、無限に自己複製を行うがん幹細胞ががん組織中に少数存在し、不均等分裂により一部が自己複製のサイクルから逸脱して分化し通常のがん細胞となっているのです。
多くの場合、このがん幹細胞の起源は通常の組織幹細胞と考えられています。すなわち、組織幹細胞に遺伝子変異が蓄積して、がん幹細胞になるというわけです。

細胞ががん化するためには、複数のがん遺伝子やがん抑制遺伝子に異常が重なる必要があるため、短期間でアポトーシスで死滅する運命の成熟(=分化)した細胞に遺伝子変異が生じても、がん細胞に変化するとは考えにくく、「組織に持続的に存在する幹細胞の遺伝子に変異が蓄積することによってがん細胞(=がん幹細胞)が発生する」と考えられています。
がん幹細胞(cancer stem cell)は腫瘍始原細胞(tumor initiating cell)とも呼ばれ、がん細胞を生み出すもとになる細胞であり、がん組織中に少数(数%程度)存在しています。そして、がん幹細胞は正常な組織幹細胞と同様、特別な微小環境(ニッチ)中に存在し、ニッチより分泌される液性因子などによって、多分化能の維持や分裂増殖が制御されていると考えられています。
通常の抗がん剤治療や放射線治療に対して、成熟したがん細胞が死滅しやすいのですが、がん幹細胞は様々な機序で抵抗性を示します。がん幹細胞が生き残れば、がんはいずれ再燃・再発します。
膠芽腫(グリオブラストーマ)が再発しやすいのは、手術で完全に取りきることが困難なことと、がん幹細胞が放射線治療や抗がん剤で死滅しにくく生き残るためです。
したがって、膠芽腫の再発を防ぎ生存期間を延ばすためには、がん幹細胞の放射線感受性や抗がん剤感受性を高める方法の開発が必要ということになります。(がん幹細胞については163話参照)
【転写因子FOXO3aを活性化すると膠芽腫のがん幹細胞が死滅する】
膠芽腫(グリオブラストーマ)のがん幹細胞の抗がん剤感受性を高める方法として、国立がんセンターと山形大学医学部の研究グループは、FoxO3aという転写因子の活性化が有効であることを示し、FoxO3aを活性化する薬として経口糖尿病薬のメトホルミンの有効性を指摘しています。
この研究の内容に関してはニュースでも紹介されて話題になりましたので、まず、ニュースの記事を引用しておきます。
①2011年9月12日(医療タイムス)
国立がん研究センターは6日、同センターと山形大学医学部との共同研究チームにより、悪性脳腫瘍の再発の根源となるがん細胞の働きを封じる遺伝子を世界で初めて発見したと発表した。がん幹細胞の研究専門誌として伝統を誇るトップジャーナル「Stem Cells」の2011年9月号に公表している。(中略)
ヒトの最難治がんの1つである、悪性脳腫瘍の膠芽腫(こうがしゅ、グリオブラストーマ)では、手術や放射線、抗がん剤による初期治療が奏功し、いったん腫瘍が消失したように見えるケースでも、多くの場合で腫瘍の再発が見られる。最近ではこうした腫瘍の再発は、腫瘍中にごくわずかに存在する、がん幹細胞(グリオブラストーマ幹細胞)が根源となることが分かってきている。
残りの大部分を占めるがん細胞は腫瘍を形成する能力を持たないため、取り残しても再発の恐れはないと考えられ、さらにがん幹細胞と比べると放射線や抗がん剤などの治療が効きやすいことも報告されている。すなわち、このがん幹細胞を絶つことが悪性脳腫瘍の治療には重要となってくる。これは悪性脳腫瘍に限らず、多くのがんに応用可能となる考えだ。
今回の共同チームの研究では、膠芽腫の中に存在するがん幹細胞を腫瘍形成能力を持たないその他大勢のがん細胞に変える遺伝子「FoxO3a」を世界で初めて明らかにし、同時に分子レベルで解明している。がんセンターでは、「今回の成果は、FoxO3aを活性化できる薬剤を探索することによって、悪性脳腫瘍に対する根治療法を開発できる可能性を示唆している」と述べている。
関連論文:FoxO3a functions as a key integrator of cellular signals that control glioblastoma stem-like cell differentiation and tumorigenicity.(FoxO3aは膠芽腫幹細胞の分化と腫瘍形成性をコントロールする細胞内シグナルの主要な調節器として作用する)Stem Cells. 29(9):1327-37. 2011年
②2012/11/16 (日本経済新聞)
http://www.nikkei.com/article/DGXNASDG15056_W2A111C1CR0000/
糖尿病薬、がん治療に効果 山形大と国立がん研究センター:
山形大医学部と国立がん研究センターの共同研究チームは、糖尿病の治療薬「メトホルミン」が、がん治療に効果があることを発見したと発表した。既に治療に使われている薬のため、新薬を開発するよりも短期間での実用化が期待できるという。研究成果は15日付の米科学誌電子版に掲載。
共同研究チームによると、がん治療では腫瘍の再発が課題で、新しい腫瘍をつくる「がん幹細胞」の働きを変えることが重要とされている。
チームのこれまでの研究で、悪性脳腫瘍のがん幹細胞の中にある「FoxO3」という分子が活性化すると、がん幹細胞が再発不可能な細胞に変化することが分かっていた。
今回、研究チームはメトホルミンにFoxO3を活性化させる作用があることを発見。腫瘍細胞を植えたマウスに、10日間メトホルミンを投与したところ、新たな脳腫瘍が形成されることなく、がん幹細胞が消失する効果などが確認できたという。
記者会見した山形大医学部の北中千史教授(分子腫瘍学)は「メトホルミンは全ての人に使える薬ではないが、ほかのがんにも応用できる可能性が示された」と話した。〔共同〕
関連論文:Glioma-initiating cell elimination by metformin activation of FOXO3 via AMPK.(メトホルミンによるAMPKを介したFOXO3の活性化によるグリオーマ始原細胞の排除)Stem Cells Transl Med. 1(11):811-24. 2012年
増殖シグナルの伝達系であるPI3K(phosphoinositide-3-kinase)/Akt/mTOR(mammalian target of rapamycin)経路とMEK(mitogen-activated protein/extracellular signal-related kinase kinase)/ERK(extracellular signal-regulated kinase)経路の両方を阻害するとグリオブラストーマ幹細胞の分化を誘導し、腫瘍形成能を抑制し、抗がん剤や放射線治療の感受性を高めることができることが報告されています。
これらのシグナル伝達系を阻害するとFoxO3aという転写因子が活性化され、このFoxO3aの活性化がグリオブラストーマ幹細胞の分化誘導や腫瘍形成能抑制に関与していることを、これらの研究グループが明らかにしたという内容です。
つまり、膠芽腫幹細胞のFoxO3aを活性化すれば、増殖の能力の無いがん細胞に変化し、再発を予防する効果が高まるという内容です。そして、経口糖尿病薬のメトホルミンがFoxO3aを活性化する作用をもっているので、膠芽腫細胞の治療にメトホルミンが役に立つということです。理論通りであれば、難治性のグリオブラストーマを根治することも可能になりそうです。
メトホルミンがAMP活性化プロテインキナーゼ(AMPK)を活性化し、AMPKがFoxO3aを活性化すること、メトホルミンがAMPKを活性化することは、この報告以前の他の論文にもすでに発表されています。また、まだ動物実験での結果なので、記者会見するほどのインパクトのある研究結果だとは思わないのですが、「治療が困難な膠芽腫の生存率を既存の薬であるメトホルミンで高めることができる」という点が膠芽腫患者に恩恵がある(直ぐにでも応用できる)ので、記者会見する意味があったのかもしれません。
膠芽腫細胞以外でも、メトホルミンががん幹細胞の抗がん剤感受性を高めることが報告されていますので、多くのがんの抗がん剤治療においてメトホルミンの併用は有用だと思います。(308話参照)
【FoxO3aとは】
FoxOは「Forkhead box O」の略で、DNA結合ドメインFOX(Forkhead box)をもつForkheadファミリーのサブグループ“O”に属する転写因子です。
哺乳類では4種類(FoxO1, FoxO3a, FoxO4, FoxO6)あり、線虫ではDaf-16、ショウジョウバエではdFOXOとそれぞれ1種類のみ存在します。
線虫と
ハエと哺乳類において、インスリン/インスリン様成長因子-1(IGF-1)シグナル伝達系は保存されており、FoxO転写因子はこのシグナル伝達系の下流する位置しています。
FoxO1とFoxO3aは約650個のアミノ酸からなる蛋白質で、遺伝子のプロモーター領域のTTGTTTACという配列に結合します。
転写因子というのは特定の遺伝子の発現(DNAの情報を蛋白質に変換すること)を調節している蛋白質で、FoxOはストレス応答、代謝制御、細胞周期、アポトーシス、細胞分化、DNA修復、免疫機能、炎症などに関連する多くの遺伝子の発現を促します。
がん抑制遺伝子としての性格ももっており、FoxOの活性化は一般的に抗がん作用があります。
FoxOはインスリン-PI3K-AKTシグナルによって負に制御されています。
つまり、PI3K-AKTシグナルが活性化されるとAKTによって直接的にリン酸化され、14-3-3というタンパク質と結合し、FoxOの核外移行を促進することでその転写活性は抑制されます。
一方、栄養飢餓状態ではPI3K-AKTの不活性化に伴いFOXOの活性化が誘導されることになります。
一般的に「転写因子FoxOはストレス耐性を高めて寿命延長とがん抑制に関与する」と考えられています。つまり、カロリー制限や糖質制限やAMPK活性化などによる寿命延長や抗がん作用に関与する転写因子として重要な役割を担っています。

図:増殖シグナルによってPI3K/Akt経路やMEK/ERK経路が活性化されるとFoxOはリン酸化されて、核外に移行するので転写活性は不活性化される。核外移行シグナルになるFoxOのリン酸化を阻止するとFoxOの転写活性が作用して、標的遺伝子の発現が誘導される。
【FoxO3aを活性化する方法を複数組み合わせれば、膠芽腫を消滅できるかもしれない】
前述の国立がんセンターと山形大学医学部の共同研究の結果は、グリオブラストーマ幹細胞のFoxO3aを活性化すれば、がん幹細胞の分化を誘導し、腫瘍形性能を低下させ、がんを消滅できる可能性を示しています。
FoxO3aを活性化させる方法として、メトホルミンが有望視されていますが、メトホルミン以外にも、中鎖脂肪ケトン食、L-カルニチンとアセチル-L-カルニチン、フェノフィブラート、イソトレチノインがあります。これらに関しては、すでに解説していますので、簡単に説明しておきます。
①ケトン食はヒストン脱アセチル化酵素を阻害してFoxO3aを活性化する:
ケトン体の一種のβヒドロキシ酪酸がヒストン脱アセチル化酵素を阻害し、Foxo3aやMt2などの酸化ストレス耐性遺伝子のプロモーター領域におけるヒストンの高アセチル化を引き起こし、これらの遺伝子発現を亢進することによって酸化ストレス耐性を高めることが報告されています。(詳しくは322話参照)
血中のβヒドロキシ酪酸が高濃度になるケトン食が、寿命延長やがん抑制に有効である機序として、FoxO3aの活性化が重要な役割を果たしている可能性があります。
脂肪酸のβ酸化が亢進するだけでFoxO3aの活性化が起こることが報告されています。脂肪酸のβ酸化を促進する中鎖脂肪酸と多く使ったケトン食はFoxO3aをさらに活性化する可能性があります。(詳しくは318話参照)
そもそも、ケトン食がグリオブラストーマの増殖を抑えることは臨床試験で明らかになっています。その機序は多様ですが、FoxO3aの活性化も関与しているようです。
②脂肪の燃焼とヒストンのアセチル化を促進するL-カルニチンとアセチル-L-カルニチン:
L-カルニチンは長鎖脂肪酸をミトコンドリアへ運ぶのが主な作用ですが、最近の研究で、「L-カルニチンは内因性のヒストン脱アセチル化酵素の阻害剤で、ヒストンのアセチル化を高めて、がん細胞の増殖を抑制する」ことが示されています。
さらに、アセチル-L-カルニチンのアセチル基が、細胞核のヒストンのアセチル化に使われることが報告されています。
つまり、L-カルニチンとアセチル-L-カルニチンは脂肪酸のβ酸化を亢進する効果と、ヒストンのアセチル化を亢進することによってFoxO3の活性を高める効果があります。(詳しくは313話参照)
③フェノフィブラートは様々なメカニズムでFoxO3Aの活性化を引き起こす。
高脂血症治療薬のフェノフィブラートが膠芽腫(グリオブラストーマ)に対して抗腫瘍効果を示すことが報告されています。
フェノフィブラートはPeroxisome Proliferator-activated Receptor α(PPARα:ペルオキシソーム増殖因子活性化受容体α)に結合してPPARαを活性化します。
PPARαは核内受容体の一種で、ペルオキシソームを増やして脂肪酸のβ酸化を亢進し、グルコースの解糖系を抑制する働きがあるので、がん細胞のワールブルグ効果(酸素がある条件でも、がん細胞はグルコースの嫌気性解糖系でエネルギーを産生していること)を阻害して、がん細胞の増殖を抑える可能性が指摘されています。
フェノフィブラートはPPARα依存性あるいは非依存性の機序で、PI3K/Aktシグナル伝達系の阻害や、転写因子FoxO3Aの活性化を引き起こします。FoxO3Aの活性化はアポトーシスを誘導するBimの発現を亢進し、グリオブラストーマを死滅させるという機序が提唱されています。(詳しくは326話参照)
④ニキビ治療薬のイソトレチノインはFoxO3aを活性化する:
イソトレチノイン(Isotretionin)はレチノイド(ビタミンA誘導体)の一種です。
ビタミンAの体内における活性本体であるAll-trans retinoic acid(レチノイン酸)はレチノイン酸受容体(retinoic acid receptor: RAR)に結合するとホモ二量体を形成し、標的遺伝子のプロモーター領域にあるレチノイン酸応答配列(RARE)に結合して遺伝子転写のスイッチをオンにします。
イソトレチノイン(13-cis retinoic acid)はプロドラッグであり、細胞内でAll-trans RAに変換されて、同様の遺伝子発現の調節を行います。
イソトレチノインは難治性にきびの治療薬として使用されていますが、IGF-1の産生を減少させる作用や転写因子FoxOを活性化する作用が報告されており、がんの治療に利用する研究が行われています。(詳しくは323話参照)
グリオブラストーマ細胞のエネルギー代謝は解糖系に依存度が高いので、解糖系を阻害しながら、増殖シグナル伝達系(PI3K/Akt経路やMEK/ERK経路)の阻害やFoxO3a転写活性の活性化すると抗腫瘍効果を高めることができそうです。
以上のことから、グリオブラストーマの治療において、メトホルミン、中鎖脂肪ケトン食、L-カルニチンとアセチル-L-カルニチン、フェノフィブラート、イソトレチノインを組み合わせると、FoxO3aを効率的に活性化し、抗腫瘍効果を高めることができます。また、2-デオキシ-D-グルコースを併用すると、さらに効果が高まるように思います。
ただし、FoxO3aの活性化が全てのがんにおいて有効というわけでは無いので、注意が必要です。
FoxO3aの標的遺伝子は酸化ストレスに対する抵抗性を高め、ダメージをうけた細胞の修復を促進するなどの作用があるため、抗がん剤によるがん細胞の攻撃からがん細胞を守る可能性も指摘されています。
つまり、がん細胞は生き残りの戦術として、FoxOを活性化して薬剤耐性を獲得している例がいくつも報告されています。
したがって、FoxO3aの活性化を目指した治療は現時点では膠芽腫(グリオブラストーマ)だけに応用する方が良いと思います。
画像をクリックするとサイトに移行します。
新刊紹介:膠芽腫(グリオブラストーマ)の根治を目指す補完・代替医療
本書はプリント・オン・デマンド(Print on Demand)という出版形式で書店では販売していません。アマゾンからの購入になります。
アマゾンからの購入はこちらへ:
| « 338)2-デオ... | 340)大豆製食... » |






