未承認薬と適応外の問題についてパブコメ募集は8月17日までです。
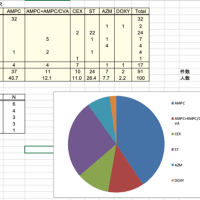
薬剤ごとのソートを(エクセルで)かけると、どれくらいの団体から要望があがっているかという数のビジュアルの問題があるそうなので、「他が出せばいいや」といわず、いろいろなところから出してもらうことも大切。
「要望書」の締め切りのあとに、その検討の会議が開かれます。さらにそのあと、製薬会社がどうするかという問題がありますが・・。
昨年度の検討会会議の資料がWAMネット(資料の宝庫!)にあります。
こんな感じで↓会議が行われています。
-----------------------------------------------------------------------
「第18回 未承認薬使用問題検討会議 議事次第」
平成20年9月29日(月)14:00~16:00九段会館 真珠の間
1.検討する必要のある未承認薬について
2.その他
配付資料一覧
第17回未承認薬使用問題検討会議(平成20年6月30日開催)において状況調査の上、報告することとなった品目について
http://www3.wam.go.jp/wamappl/bb13GS40.nsf/0/3dbcd58e478b1737492574d500073029/$FILE/20081001_3shiryou.pdf
------------------------------------------------------------------------
この前の年の2007年の会議の速記録から一部抜粋しますと、
【中垣審査管理課長】
「・・・要するにたくさんの御要望があり、欧米4カ国を今チェックいただいているわけですけれども、日本でも毎年30から新有効成分を承認しているわけでございますから、たくさんの新薬が向こうで承認されている。その中でもこれは持ってきてほしいというような医療の現場の御意見をまとめるという意味で、そういった前さばきというのが、恐らくこの検討会に一番期待されているのだろうと考えるわけでございます。
そこで先ほどの例ではございませんが、ワーキンググループのレポートというのが、では次にどこへ持っていくかと申し上げますと、機構が最終的にどのようなデータを要求しようかとか、場合によっては優先審査にしようとかいうようなことを判断してまいるわけでございます。そのときに先ほど申し上げましたような厳密な意味ではないにしろ、先生方がおまとめいただいたワーキンググループのレポートというのは、実は大きな意味があるというふうに考えています。
すなわちどのようなデータを要求していくか。さらには優先審査にする、しないということを厚生労働省として医薬品機構として判断するわけでございますが、そのときのよりどころの大きな1つになっているというのが、今の現状なんだろうと思います。
現実問題としてここで早く進めるべきだと言われたものの大半というのは、やはり優先審査の手続を踏んできております。先ほどのエーザイの問題でございますれば、これからワーキンググループでレポートをまとめていただくわけでございますが、しっかりとしたデータがあるということでございますれば、ここで言っているような、少なくとも国内でピボタルな比較試験をやれというような話にはまたなっていかないんだろうと。そういう意味でワーキンググループの評価、あるいはこのワーキンググループの評価を受けたこの検討会の評価というのを、我々は頼るよすがの1つとしているという現状でございます。」
【中垣審査管理課長】
「・・・今正直に申し上げていわゆる優先審査になったものにおきまして、申請から承認まで大体1年ちょっとかかっているのが現状なんだろうと思います。
18年度の処理件数は、承認が確か70件程度、取り下げとか、そういうお断りしたものを入れると大体100件でございました。前年度に比べて3~4割ぐらいの処理能力がアップしております。
そういう点で申し上げますと、医薬品機構の処理能力も少しずつ向上してきているところです。19年度から人員倍増にも取り組むわけでございますから、我々としても早急に欧米に劣らない体制というのをやりたいと思っていますが、いまだある程度の時日がかかっているのも事実でございます。
一方、我々も気にしなければいけませんし、せっかくこういう場を与えていただきましたので、先生方にも申し上げておきますけれども、一部この検討会での結果を見ようという企業があらわれているのも事実であります。すなわち検討会で優先的な取り扱いであるとかデータを省略していいとか言ってくれないかな。その結果を待つまで動きをとめておこうというような話が出てきているのも、事実といってはいけませんが、うわさがあるわけでございます。
したがいまして先生方にお願いをしたいのは、先生方、各学会からいわゆる科学的なバックボーンで議論しておられるわけでございますので、フランクに率直にサイエンティフィックな御議論を賜りたいと思っています。
私が考えるに、企業は企業で自主的に新しいものを国民に提供する。自分たちが、効果、あるいは安全性にも責任を持ってもらうということが基本であることは間違いがないとは思うんですけれども、いろいろ話を聞いていますと、検討会での議論を待っているというようなところもあると思います。そういう意味で申し上げますと、ひとつこれからもサイエンティフィックに率直な御議論を賜ればと思っている次第でございます。」
・・・ということで。
未承認薬使用問題検討会議 第13回速記録平成19年7月30日(月)
http://www.mhlw.go.jp/shingi/2007/07/txt/s0730-7.txt
製薬ギョウカイは「未承認薬開発支援センター」を発足させています。
(2009年6月8日 薬事日報)
http://www.yakuji.co.jp/entry12892.html
8月5日に厚生労働省が開催した「中央社会保険医療協議会」の薬価専門部会で特許期間中の新薬の薬価改定方式について議論されています。
17日までまだ時間があります・・。
薬剤ごとのソートを(エクセルで)かけると、どれくらいの団体から要望があがっているかという数のビジュアルの問題があるそうなので、「他が出せばいいや」といわず、いろいろなところから出してもらうことも大切。
「要望書」の締め切りのあとに、その検討の会議が開かれます。さらにそのあと、製薬会社がどうするかという問題がありますが・・。
昨年度の検討会会議の資料がWAMネット(資料の宝庫!)にあります。
こんな感じで↓会議が行われています。
-----------------------------------------------------------------------
「第18回 未承認薬使用問題検討会議 議事次第」
平成20年9月29日(月)14:00~16:00九段会館 真珠の間
1.検討する必要のある未承認薬について
2.その他
配付資料一覧
第17回未承認薬使用問題検討会議(平成20年6月30日開催)において状況調査の上、報告することとなった品目について
http://www3.wam.go.jp/wamappl/bb13GS40.nsf/0/3dbcd58e478b1737492574d500073029/$FILE/20081001_3shiryou.pdf
------------------------------------------------------------------------
この前の年の2007年の会議の速記録から一部抜粋しますと、
【中垣審査管理課長】
「・・・要するにたくさんの御要望があり、欧米4カ国を今チェックいただいているわけですけれども、日本でも毎年30から新有効成分を承認しているわけでございますから、たくさんの新薬が向こうで承認されている。その中でもこれは持ってきてほしいというような医療の現場の御意見をまとめるという意味で、そういった前さばきというのが、恐らくこの検討会に一番期待されているのだろうと考えるわけでございます。
そこで先ほどの例ではございませんが、ワーキンググループのレポートというのが、では次にどこへ持っていくかと申し上げますと、機構が最終的にどのようなデータを要求しようかとか、場合によっては優先審査にしようとかいうようなことを判断してまいるわけでございます。そのときに先ほど申し上げましたような厳密な意味ではないにしろ、先生方がおまとめいただいたワーキンググループのレポートというのは、実は大きな意味があるというふうに考えています。
すなわちどのようなデータを要求していくか。さらには優先審査にする、しないということを厚生労働省として医薬品機構として判断するわけでございますが、そのときのよりどころの大きな1つになっているというのが、今の現状なんだろうと思います。
現実問題としてここで早く進めるべきだと言われたものの大半というのは、やはり優先審査の手続を踏んできております。先ほどのエーザイの問題でございますれば、これからワーキンググループでレポートをまとめていただくわけでございますが、しっかりとしたデータがあるということでございますれば、ここで言っているような、少なくとも国内でピボタルな比較試験をやれというような話にはまたなっていかないんだろうと。そういう意味でワーキンググループの評価、あるいはこのワーキンググループの評価を受けたこの検討会の評価というのを、我々は頼るよすがの1つとしているという現状でございます。」
【中垣審査管理課長】
「・・・今正直に申し上げていわゆる優先審査になったものにおきまして、申請から承認まで大体1年ちょっとかかっているのが現状なんだろうと思います。
18年度の処理件数は、承認が確か70件程度、取り下げとか、そういうお断りしたものを入れると大体100件でございました。前年度に比べて3~4割ぐらいの処理能力がアップしております。
そういう点で申し上げますと、医薬品機構の処理能力も少しずつ向上してきているところです。19年度から人員倍増にも取り組むわけでございますから、我々としても早急に欧米に劣らない体制というのをやりたいと思っていますが、いまだある程度の時日がかかっているのも事実でございます。
一方、我々も気にしなければいけませんし、せっかくこういう場を与えていただきましたので、先生方にも申し上げておきますけれども、一部この検討会での結果を見ようという企業があらわれているのも事実であります。すなわち検討会で優先的な取り扱いであるとかデータを省略していいとか言ってくれないかな。その結果を待つまで動きをとめておこうというような話が出てきているのも、事実といってはいけませんが、うわさがあるわけでございます。
したがいまして先生方にお願いをしたいのは、先生方、各学会からいわゆる科学的なバックボーンで議論しておられるわけでございますので、フランクに率直にサイエンティフィックな御議論を賜りたいと思っています。
私が考えるに、企業は企業で自主的に新しいものを国民に提供する。自分たちが、効果、あるいは安全性にも責任を持ってもらうということが基本であることは間違いがないとは思うんですけれども、いろいろ話を聞いていますと、検討会での議論を待っているというようなところもあると思います。そういう意味で申し上げますと、ひとつこれからもサイエンティフィックに率直な御議論を賜ればと思っている次第でございます。」
・・・ということで。
未承認薬使用問題検討会議 第13回速記録平成19年7月30日(月)
http://www.mhlw.go.jp/shingi/2007/07/txt/s0730-7.txt
製薬ギョウカイは「未承認薬開発支援センター」を発足させています。
(2009年6月8日 薬事日報)
http://www.yakuji.co.jp/entry12892.html
8月5日に厚生労働省が開催した「中央社会保険医療協議会」の薬価専門部会で特許期間中の新薬の薬価改定方式について議論されています。
17日までまだ時間があります・・。