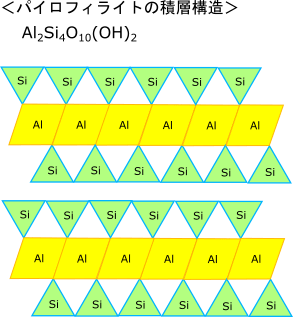
世界の穀倉地帯を形成する「黒土」は、アメリカ農業局の土壌分類ではモリソル、また、ロシア語ではチェルノゼム(チェルノ:黒色、ゼム:土)、カナダではプレーリー土と呼ばれる。いずれも2:1型粘土鉱物であるモンモリロナイトを含み、それが肥沃度の源泉になっていると言われている。モリソルの特徴は「土壌の表面層が冬に凍結して夏に融けること」にあるとされるが、「凍結」によって土壌にどのような変化が現れるのだろうか。粘土鉱物の性質を更に掘り下げて考えてみたい。
先ず、地殻の構成元素について調べた際、ケイ素Siと組み合わさる金属元素が、およそ、アルミニウムAl:鉄Fe:マグネシウムMg = 4:1:1という比率で存在することが分かった。これを踏まえると、土壌を形成する2:1型粘土鉱物は、アルミニウムとマグネシウムだけから成るモンモリロナイトとするよりも、アルミニウム1個を鉄1個に置換した組成を想定した方がより実態に即していると考えられる。そこで、以後は2:1型粘土鉱物の名称についてもモンモリロナイトではなく、粘土鉱物学においてより広い定義で用いられる「スメクタイト」を使用し、Al:Fe:Mg = 4:1:1を前提としたモデルで考えてみる。
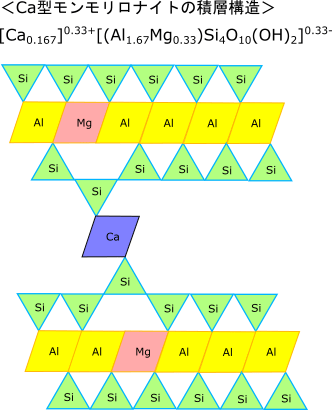
スメクタイトでは、マグネシウムMgが二価陽イオンであるため、セットとなる2つのケイ酸の内の1つがフリーになる。そこにカルシウムCaなどのアルカリがイオン結合することで、2つの2:1層が架橋される。カルシウムCaが押し広げた空間には多数の水分子が収容され、スメクタイトが有する高い養分保持力(CEC:陽イオン交換容量)と水分保持力に繋がる。

では、この基本構造を踏まえた上で、モリソルの「凍結」が何をもたらすか考える。アメリカのグレートプレーンズとカナダのプレーリー、そして、日本でも新潟県、山形県、群馬県にモンモリロナイトが見られるとのことだが、各地域に共通しているのは、大山脈の山麓に位置しミネラルが豊富な地下水(アルカリ性)が存在する、という点である。
凍結期は、植物活動が停止し、土壌表面からの水分蒸発も少ないため、土壌はアルカリ性の水で満たされることになる。すると、大気からの酸素流入がなくなるため、土壌を構成する粘土鉱物(スメクタイト)中の鉄(酸化鉄:三価の陽イオン)は、アース、すなわち大地から電子を与えられて還元鉄(二価の陽イオン)に変化する。これにより、還元鉄はマグネシウムと同じ役割を果たすことになるため、セットとなる2つのケイ酸の内の1つがフリーになってカルシウムCaを引き付ける。そして、2:1層間が架橋され、層間水が発生する。
下図の右側のように、すべての鉄Feが還元されたと仮定すると、スメクタイトのCECは2倍、水分保持力は1.5倍になる。モリソルの凍結は、このような形で土壌肥沃度の向上をもたらすことになると考えられる。

先ず、地殻の構成元素について調べた際、ケイ素Siと組み合わさる金属元素が、およそ、アルミニウムAl:鉄Fe:マグネシウムMg = 4:1:1という比率で存在することが分かった。これを踏まえると、土壌を形成する2:1型粘土鉱物は、アルミニウムとマグネシウムだけから成るモンモリロナイトとするよりも、アルミニウム1個を鉄1個に置換した組成を想定した方がより実態に即していると考えられる。そこで、以後は2:1型粘土鉱物の名称についてもモンモリロナイトではなく、粘土鉱物学においてより広い定義で用いられる「スメクタイト」を使用し、Al:Fe:Mg = 4:1:1を前提としたモデルで考えてみる。
スメクタイトでは、マグネシウムMgが二価陽イオンであるため、セットとなる2つのケイ酸の内の1つがフリーになる。そこにカルシウムCaなどのアルカリがイオン結合することで、2つの2:1層が架橋される。カルシウムCaが押し広げた空間には多数の水分子が収容され、スメクタイトが有する高い養分保持力(CEC:陽イオン交換容量)と水分保持力に繋がる。

では、この基本構造を踏まえた上で、モリソルの「凍結」が何をもたらすか考える。アメリカのグレートプレーンズとカナダのプレーリー、そして、日本でも新潟県、山形県、群馬県にモンモリロナイトが見られるとのことだが、各地域に共通しているのは、大山脈の山麓に位置しミネラルが豊富な地下水(アルカリ性)が存在する、という点である。
凍結期は、植物活動が停止し、土壌表面からの水分蒸発も少ないため、土壌はアルカリ性の水で満たされることになる。すると、大気からの酸素流入がなくなるため、土壌を構成する粘土鉱物(スメクタイト)中の鉄(酸化鉄:三価の陽イオン)は、アース、すなわち大地から電子を与えられて還元鉄(二価の陽イオン)に変化する。これにより、還元鉄はマグネシウムと同じ役割を果たすことになるため、セットとなる2つのケイ酸の内の1つがフリーになってカルシウムCaを引き付ける。そして、2:1層間が架橋され、層間水が発生する。
下図の右側のように、すべての鉄Feが還元されたと仮定すると、スメクタイトのCECは2倍、水分保持力は1.5倍になる。モリソルの凍結は、このような形で土壌肥沃度の向上をもたらすことになると考えられる。