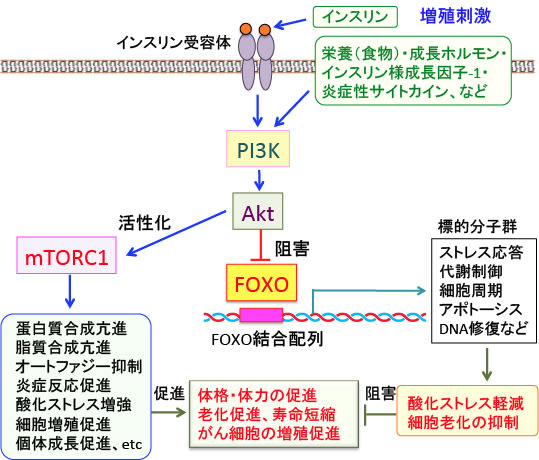
図:インスリンやインスリン様成長因子-1(IGF-1)や豊富な食物や炎症性サイトカインなど様々な増殖刺激によってPI3K/Aktシグナル伝達系が活性化されるとFOXO(Forkhead box O)という転写因子の活性が抑制される。FOXO転写因子が活性化されると酸化ストレスが軽減し、細胞老化が抑制される。Aktの活性化はmTORC1を活性化して蛋白質や脂質の合成を促進し個体の成長や成熟を促進し、体格や体力を高める作用があるが、老化とがん細胞の増殖を促進する作用もある。したがって、PI3K/Aktシグナル伝達系を抑制すると、細胞増殖や個体の成長の面では負に作用するが、FOXO転写因子の活性化とmTORC1の抑制の2つの機序で寿命延長とがん抑制の効果が得られることになる。つまり、食事療法(カロリー制限や糖質制限)や抗炎症作用をもつ食品・サプリメントなどによってインスリン/IGF-1シグナル伝達系やmTORC1活性の抑制とFOXO転写活性の亢進を行うと、がんを予防し、寿命を延ばせるかもしれない。少なくとも、生殖年齢の過ぎた50歳以降は、カロリー制限や糖質制限などによってmTORC1の活性を低下させる方が長生きには効果が期待できる。
390)身長と寿命の逆相関:身長が低いと長生きする
【大きな動物は寿命が長く、太った動物は寿命が短い】
ゾウのように大きな動物は、ネズミのような小さな動物よりも寿命が長いことは良く知られています。一般的に、体の大きな動物ほど寿命が長いことになっています。その一つの理由は、大きな動物ほど成長と性成熟に時間がかかるからです。
しかし、同じ種であれば、太った個体や体格の大きい個体ほど寿命が短いことが多くのデータで明らかになっています。遺伝子改変で体格が大きくなるマウスを作ると、正常のサイズのマウスより寿命が短くなります。体格の大きなマウスは成長速度が促進し、生殖活動も旺盛ですが、活性酸素の産生が亢進し、寿命は短くなります。
犬を例にとると、小型犬と中型犬と大型犬というように大きさによって寿命を比べると、体格の小さい犬ほど寿命が長いことが知られています(下図)。このように同じ種であれば、体格の大きい個体ほど寿命が短い(逆に言うと小さい個体ほど長生きする)ということになります。これは人間でも証明されています(後述)

図:犬を肩高の大きさによって小型犬、中型犬、大型犬、超大型犬に分けると、体が小さいほど寿命が長いことが報告されている。上の図で、10年以上生きる割合(緑とオレンジを合わせた数値)は小型犬が50%以上で、中型犬で約40%、大型犬で約25%、超大型犬で10%程度というデータを示している。15年以上生きる犬は小型犬では10%近くいるが大型犬や超大型犬ではほとんどいない。
【生後すぐの短期間のカロリー制限で寿命が伸びる?】
一般的には、カロリー制限で老化抑制や寿命延長効果を得るためには、カロリー制限を長期間行う必要があると考えられています。しかし、マウスの実験ですが、生後間もない時期の短期間のカロリー制限が寿命を延ばすという報告が最近報告されています。以下のような論文があります。
Long-lived crowded litter (CL) mice exhibit lasting effects on insulin sensitivity and energy homeostasis. (母乳の摂取量の少なかった長生きマウスは、インスリン感受性とエネルギー恒常性において永続的な効果を示す)Am J Physiol Endocrinol Metab. 2014 Apr 15. [Epub ahead of print]
「litter」というのはネズミや犬やブタなどの「ひと腹の子」ということで、一度に何匹も子供を出産する動物で、出産した後に一緒に母親の乳で育つ兄弟ということになります。
「crowded litter」というのは、「母乳を吸う時に混雑する状況にしたひと腹の子」という意味です。この実験では、通常の状態より乳飲み子であるlitterの数を増やすことによって、乳児(生まれてから離乳するまでの約3週間)の段階での栄養摂取を制限しています。つまり、生まれた直後に食事摂取を短期間減らすと、その効果は成長してからも続き、結果的に寿命が延びるという報告です。
【要旨】
哺乳類において出産直後の栄養状態は老化と寿命に影響する。一緒に乳を飲む子供(Litter)の数を増やすことによって栄養摂取を制限する「crowded litter(CL)model」の実験によって、生後3週間の栄養摂取を減らすと平均寿命と最大寿命が延びることが遺伝的に正常なマウスで示されている。
今回の実験では、CLマウスにおいて出生後早い時期の栄養状態がグルコース代謝とエネルギー恒常性にどのような影響を与えるのかを明らかにすることを目的とした。
Litterが8匹の状態をコントロール(対照)にしてlitterを12匹あるいは15匹に増やした場合を比較した。
離乳期から成長した段階において、CLマウス(litterを12から15匹に増やした群 )はコントロール群(litterが8匹)に比較して、顕著に痩せており、酸素消費量が多かった。
6ヶ月齢において、CLマウスは空腹時のレプチンの濃度が低く、低用量のレプチンを注射で投与すると体重減少と食事摂取量の減少はコントロール群よりメスのCLマウスで顕著であった。
22ヶ月齢において、メスCLマウスはコントロール群に比べて脂肪細胞が小さかった。
6ヶ月齢のオスCLマウスではインスリン感受性の亢進を認め、メスCLマウスでは高齢になってインスリン感受性の亢進を認めた。
さらに、膵臓のβ細胞の体積はオスCLマウスにおいて顕著で減少しており、CLマウスではβ細胞の増殖活性の低下を認めた。
以上の結果より、出生後早い時期における栄養摂取の制限は、生涯に渡って代謝に影響し、このことがCLマウスの寿命の延長に関与していることが示唆された。
このマウスの研究では、出生後早期に短期間のカロリー制限で寿命が延びることが示されたということです。
カロリー制限が寿命を延ばすことは酵母、線虫、ショウジョウバエ、マウス、霊長類(アカゲザル)など多くの種で確認されています。
成長してからカロリー制限の寿命延長効果を得るためには長期間に渡ってカロリー制限する必要がありますが、出生直後であれば、短期間のカロリー制限で、長期のカロリー制限と同様の寿命延長効果が一生得られるという結果です。
マウスの赤ん坊は約3週間で離乳を迎えます。母乳で栄養を得ているときに、通常8匹の兄弟のところを12~15匹に増やしています。つまり、母親の乳の8分の1を摂取した群と、母親の乳を12分の1か15分の1を摂取した群を比較しています。
Litterを増やしたグループでは、摂取カロリーが53%~67%に減少することになります。
生後3週間の間の母乳で育っている時期に十分なカロリーが得られないと、体脂肪が少なく、体格の小さいマウスとして成長します。そして、生涯に渡って、体格は小さく、体脂肪は少なく、寿命が延びるという結果です。
生後間もない時期に栄養失調を起こすような食事制限は寿命を短くすると思われますが、栄養失調を来さないレベルの摂取カロリーの減少を出生直後に経験すると、食糧事情が厳しい環境を体が察知して低摂取カロリーで生きていけるように体格を小さくし、代謝を低下させるようなメカニズムが作動するのかもしれません。
【身長が低いほど長生きする】
身長と寿命の関係に関しては相反するデータが出ています。
動物の例で紹介したように、同じ種の中では小さい個体ほど寿命が長いので、人間の場合でも身長と寿命は逆相関すると考えられています。実際に、身長と死亡率(特に、呼吸器系疾患と冠動脈疾患と脳卒中による死亡)との間に逆相関(身長が高いほど死亡率が高い)の関係があることが複数の研究で示されています。
しかし、低身長ほど寿命が短いというデータもあります。開発途上国のような貧困による栄養状態や衛生環境が悪い地域のデータでは、低身長(=栄養不良を意味する)は感染症や心血管疾患の発症率が高く、寿命が短いというデータは納得できます。
しかし、栄養状態や社会環境が悪くない先進国では、低身長ほど様々な疾患の罹患率が低く、寿命が長いというデータが数多く報告されています。
例えば、アメリカのある地域で、白人や黒人や中国人や日本人やラテン系アメリカ人など体格に多様性の高い同じ地域に住む人口集団の解析では、中国人や日本人やラテン系アメリカ人の方が白人や黒人より寿命が長く、それは身長が関連していることが指摘されています。
何千人というプロ野球選手の身長と体重と死亡時の年齢のデータを解析すると身長が高いほど死亡年齢が低いことが示されています。映画スターなどの著名人を対象にした解析でも同様な結果(身長と寿命は逆相関する)ことが示されています。
米国のある研究では、身長が175.3cm以下の男性は身長が175.3cm以上の男性グループに比較して寿命が4.95年長いという報告があります。
身長が170.2cm以下の男性は182.9cmの男性より7.46年長生きするという報告もあります。
低身長と高身長の寿命の差を検討した多くの研究をまとめた論文では、身長が1cm高くなると、0.47~0.51年の寿命の短縮があるという数値が報告されています。180cmの人は160cmの人の平均10年間ほど寿命が短くなるという計算です。
女性が男性よりがんの発生が少なく、寿命が長いのは、男性の方が
mTORC1の活性が高いためだという報告もあります。
mTORC1活性を高めることによって男性は屈強さを得る代わりに寿命を犠牲にしているという考えです。これに関しては
362話で考察しています。
男性は女性より平均して約8.0%程度身長が高く、平均寿命は7.9%短いというデータがあります。
これは平均すると女性は男性より約13cm身長が低く、寿命は6歳ほど長いということです。
この数値は日本人でも当てはまります。1950年と2010年の30歳代の男女の身長差は12~13cm程度です。
2012年の日本人女性の平均寿命は86.41歳で、日本人男性の平均寿命は79.94歳というデータが発表されています。日本の場合、女性の平均寿命が男性より5~7歳長いというのは1965年以降ずっと続いています。1965年は平均寿命がまだ70歳前後のころです。1950年代は平均寿命が60歳代ですが、この頃でも女性の方が3~4歳ほど寿命が長いことがデータで示されています。
日本の最近のがん統計によると、1年間にがんと診断されるのは約75万人で、そのうち男性は約44万人、女性は約31万人となっています。人口10万人あたりの粗罹患率は男性が703.3人、女性は476.7人です。(2008年のデータ)
生涯でがんで死亡する確率は、男性は26%(4人に1人)、女性は16%(6人に1人)というデータもあります。60歳代以降のがんの発生率は男性が女性より顕著に高いのが特徴です。がんの発生率が男性より女性の方がかなり低いという現象は多くの国で確認されています。
このように、女性の方ががんが少なく、寿命が長い理由の一つは、体が小さいからで、その原因がインスリン/インスリン様成長因子-1/mTORC1シグナル伝達系の活性が女性の方が低いからと考えることができます。
同じ身長で比較すると、女性も男性も寿命は同じという報告もあります。つまり、男女を問わず、身長や体格(=インスリン/インスリン様成長因子-1/mTORC1シグナル伝達系)が寿命を決めているという結果です。
【ホノルル・ハート・プログラムのコホート研究】
ハワイで日系移民を対象にしたコホート研究のHonolulu Heart Program/Honolulu Asia Aging Studyは世界的に有名な疫学研究です。
1900年~1919年に生まれたハワイのホノルル在住の8006人の日系アメリカ人を対象に1965年から始まり、ほぼ50年間の追跡が行われています。
このうち約1200人が90歳以上生きており、まだ250人程度が生存しているということです。
このデータの解析でも、身長が低い方が寿命が長いことが明らかになっています。
以下のような論文が最近報告されています。
Shorter Men Live Longer: Association of Height with Longevity and FOXO3 Genotype in American Men of Japanese Ancestry(低身長の男性は長く生きる:日系アメリカ人男性における身長と寿命とFOXO3遺伝子型の関連
PlosOne Published: May 07, 2014 DOI: 10.1371/journal.pone.0094385
ホノルル心臓プログラム(the Honolulu Heart Program)の研究のデータから得られた1915人の非喫煙者の健康な日系アメリカ人を対象に36年間追跡した解析では、エネルギー消費量が平均の15%低いグループでは死亡率が低いことが示されています。
この論文では以下のような図が載っています。この集団では、80歳くらいまでは身長による生存率に差は認められませんが、80歳以降は身長が低い方が長く生きることが示されています。

この論文では、成長の初期の段階で体格が小さいことが80歳以降の寿命の延長に関連しており、寿命に関連する
FOXO3遺伝子の遺伝子型との関連を示唆しています。
FOXO3は転写因子で寿命を延ばす作用があります。このFOXO3遺伝子には一塩基多型(single nucleotide polymorphism:SNP)に基づく活性の違いがあります。このうち、寿命延長に関連したFOXO3遺伝子型を持っている人では、インスリン濃度が低値で、がんも少なく、身長が低い関係があると報告しています。
インスリン/インスリン様成長因子-1のシグナル伝達系の活性が低いと身長や体格は小さくなります。つまり、身長と寿命の逆相関はインスリン/インスリン様成長因子-1のシグナル伝達系、mTORC1活性、FOXO活性で説明できることになります。
身長の高い人や体格の良いひとはカロリー摂取が多いことががんのリスクを高めたり、早死にする原因になっているという指摘もあります。
女性が男性より寿命が長いことも身長との関連が指摘されています。女性において、インスリン/インスリン様成長因子-1(IGF-1)シグナル伝達系の活性の低下は寿命延長と短身長と相関しているという考えです。
大きい人は成長ホルモンやインスリン/インスリン様成長因子-1のシグナル伝達系(最終的にはmTORC1の活性化)が亢進しているから、成長が良いのだけど、これらのシグナル伝達系が亢進すると老化が促進されて寿命が短くなるというメカニズムです。
【カロリー制限による寿命延長効果の進化論的存在意義】
食事からの摂取カロリーを減らすと老化速度が抑制され、寿命が延びることが知られています。
老化の研究で使われる「カロリー制限食」は、栄養失調を来さないで(タンパク質や必須脂肪酸やビタミンやミネラルの不足を起こさないで)摂取カロリーを30から40%程度(場合によっては50%程度)減らす食事です。
カロリー制限は寿命を延ばす最も確実な方法で、このカロリー制限と同じ効果(抗老化や寿命延長効果)を示す薬を
Calorie restriction mimetics (CRM:カロリー制限模倣化合物)と言い、
CRMには2-デオキシ-D-グルコース(
381話)、D-グルコサミン(
387話)、抗糖尿病薬のメトホルミン(
384話)、mTORC1阻害剤のラパマイシン(
383話)、赤ワインに含まれるレスベラトロール、ポリアミンの一種のスペルミジンなどが知られています。
カロリー制限で寿命が延びることが最初に報告されたのは、1935年のことです。
ラットに与えるエサのカロリーを30%減らすと寿命が40%延びたという結果が報告されています。
このようなカロリー制限による寿命延長効果は、酵母、線虫、昆虫、魚、マウスやラットなど多くの生物で認められ、さらに霊長類のアカゲザルでも、カロリー制限によって寿命が延びることが報告されています。
「カロリー制限の寿命延長作用」のメカニズムに関しては、まだ不明な点が多く残されていますが、成長ホルモン/インスリン/インスリン様成長因子-1(IGF-1)のシグナル伝達系やその下流のPI3K/Aktシグナル伝達系やAktによって活性化されるmTORC1(哺乳類ラパマイシン標的タンパク質複合体1)、Aktによって負に制御される転写因子のFOXO(Forkhead box O)などの関与を中心に研究されています。
例えば、FOXO(Forkhead box O)は栄養飢餓時に活性化される転写因子で、ストレス応答、代謝制御、細胞周期、アポトーシス、DNA修復などに関連する多くの遺伝子の発現誘導を促します。がん抑制遺伝子としての性格も持っており、FOXOの活性化は抗がん作用があります。カロリー制限や糖質制限やAMPK活性化などによる寿命延長や抗がん作用に関与する転写因子として重要な役割を担っています。
インスリンが結合して活性化されたインスリン受容体はホソホイノシチド3-キナーゼ(PI3K)というリン酸化酵素を活性化し、これがさらにAktというセリン・スレオニンリン酸化酵素をリン酸化して活性化します。活性化したAktは、細胞内のシグナル伝達に関与する様々な蛋白質の活性を調節することによって細胞の増殖や生存(死)の調節を行います。Aktのターゲットの一つがFOXOで、AktはFOXOの転写活性を抑制します。
また、活性化されたAktはmTORC1を活性化します。mTORC1はタンパク質や脂肪の合成や細胞増殖を促進します。mTORC1が活性化されると体は大きくなりますが、老化が促進され寿命が短くなることが知られています。(
362話参照)
インスリンはmTORC1を活性化し、FOXOを抑制することによって老化を促進すると言えます(トップの図)。
上記のようなメカニズムが現時点では主流ですが、これだけで全てを説明できるわけではありません。実際のところ、そのメカニズムは単純ではありません。
しかし、生物が「カロリー制限によって寿命が延びる」ようなメカニズムを進化の過程で獲得したであろうことは容易に理解できます。このメカニズムを獲得したものが淘汰に生き残ったとも言えます。この生物の生存や種の繁栄においてメリットがあるからです。
全ての生物において、最も優先されるのは種の保存と繁栄です。この種の繁栄に有利な性質が進化の過程で淘汰を生き残ることになります。
食糧が乏しくなるとすぐ死ぬような生き物は進化の過程で簡単に淘汰されます。
栄養やエネルギーの不足に対して抵抗性を持つようなメカニズムを獲得したものが生き残ります。
実際、カロリー制限食では酸化ストレスや栄養飢餓など様々なストレスに対する抵抗性が増すことが知られています。
食糧が乏しい時には、栄養飢餓に対する抵抗性を高め、代謝を抑制して寿命を延ばし、食糧が十分に入手できるようになったときに生殖活動が行えるように、食糧が乏しい条件(カロリー摂取が不足するとき)では寿命を延ばすメカニズムやストレスに対する抵抗性を高めるメカニズムが進化したと言えます。
前述のFOXOは酸化ストレスや飢餓ストレスに対する抵抗力を高める作用があります。栄養飢餓を乗り越えるために進化の過程で獲得したメカニズムです。
食糧が少なくなったとき単に寿命を延ばすだけでなく、食糧が得られるとき生殖活動を再開することが目的であるため、若々しく保つ(老化を抑制する)ことも重要です。
すなわち、カロリー制限は寿命を延ばすだけでなく、体を若々しくする効果もあることになります。
一般的に多くの生物において食糧が絶えず不足ない状態というのは、近代の人類以外にはあり得ません。
人類は1万年前に農耕を始めることによって、食物を安定的に手に入れることができるようになりました。
しかし、気候の変化によっては飢饉を経験します。人類が飢饉を経験しなくなるのは、産業革命後に、農業の機械化によって農産物の生産性が向上し、食物の貯蔵技術の進歩によって長期間の食物の貯蔵が可能になったからです。
食物の豊富な熱帯地方の森林に住んでいれば、食物は豊富に入手できますが、多くの生物は食糧が十分に入手できなくなるリスクの中で生きてきました。
このような状況で、食物の摂取が少なくなったときに種を保存するためにはどうすれば良いか?
食事が不十分なときに、生殖を先延ばしするために、寿命を伸ばす方法が生体内で進化したということです。
食物が入手できるようになったときに生殖を開始します。
したがって、カロリーが十分取れないときは、寿命を伸ばすと同時に老化を抑制して、若々しい状態を保つ必要があるのです。
西洋人において理想の身長は188cmという報告があります。高身長は社会的にはかなりのメリットがあります。近い将来、遺伝子改変や薬を使って、自分の子供の身長を大きくすることを希望する親が出て来る可能性が高いことが指摘されています。そのため、身長と寿命の関連に関する研究が必要という意見があります。その意見では、「体を大きくすることは寿命を犠牲にする」ことを知っておかなければならないと言っています。
高身長の人が寿命を延ばしたければ、インスリン/インスリン様成長因子-1のシグナル伝達系を抑制するしかありません。そのためには、カロリー制限や糖質制限を行うと目的を実行できます。ケトン食も有効です。
長生きしたければ、理論的に正しいことを実行するしかありません。


画像をクリックするとサイトに移行します。