がんの予防や治療における漢方治療の存在意義を考察しています。がん治療に役立つ情報も紹介しています。
「漢方がん治療」を考える
396)ビタミンA(レチノール)はがん幹細胞の増殖を促進する?
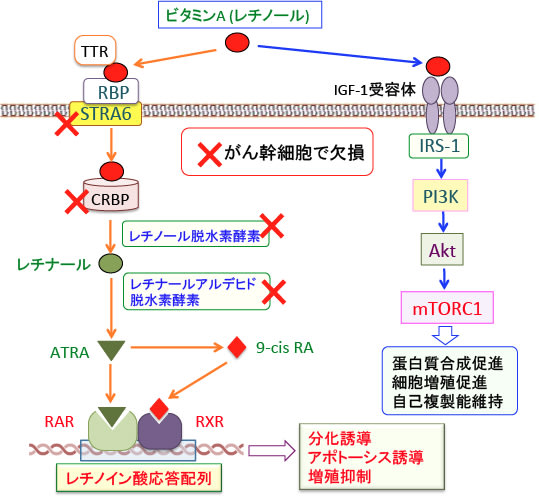
図:ビタミンA(レチノール)はTransthyrenin(TTR)とレチノール結合タンパク(Retinol Binding Protein: RBP)と結合して血中に存在し、細胞膜のSTRA6(Stimulated by Retinoic Acid 6)という受容体を介して細胞内に入る。細胞内では細胞内レチノール結合タンパク(Cellular Retinol Binding Protein: CRBP)に結合し、レチノール脱水素酵素によってレチナール(レチナールアルデヒド)に変換され、さらにレチナールアルデヒド脱水素酵素によってオール・トランス・レチノイン酸(ATRA)に変換される。ATRAはイソメラーゼで9-シス・レチノイン酸(9-cis RA)に変換される。ATRAはレチノイン酸受容体(RAR)に結合し、9-cis RAはレチノイドX受容体(RXR)に結合して標的遺伝子のレチノイン酸応答配列に結合して遺伝子転写を促進する。その結果、がん幹細胞の分化誘導、アポトーシスの誘導、細胞増殖抑制などの抗腫瘍効果を発揮する。一方、ビタミンAにはレチノイン酸を介さない直接作用もあり、その一つがインスリン様成長因子-1(IGF-1)受容体を刺激してインスリン基質-1(IRS-1)を介してPI3K/Akt/mTORC1シグナル伝達系を活性化し、その結果、タンパク質合成促進、細胞増殖促進、がん幹細胞の自己複製能の維持という作用が現れる。がん幹細胞において、レチノイン酸(ATRAと9-cis RA)が合成されてレチノイン酸標的遺伝子の発現が亢進するとがん幹細胞としての自己複製能や増殖能は維持できず、最終分化を誘導されると死滅する。そのため、がん幹細胞では、ビタミンAを取り込むSTRA6や細胞内でレチノールをレチノイン酸に変換するために必要な酵素や細胞内レチノール結合タンパク(CRBP)が欠損している。ビタミンAや体内でビタミンAになるベータカロテンを多く摂取するとがん幹細胞の増殖を促進する可能性が指摘されている。
396)ビタミンA(レチノール)はがん幹細胞の増殖を促進する?
【ベータカロテンとレチノールとレチノイン酸の関係】
まず、ビタミンAの代謝と作用について簡単に説明します。
ビタミンAは別名をレチノール(retinol)と言い、脊椎動物の発生過程、細胞分化、生殖、視覚、免疫系の調節などに重要な働きを行っているビタミンです。
レチノールは細胞内で代謝されてレチノイン酸に変換され、レチノイン酸が細胞核内の受容体に結合することによって遺伝子発現を誘導して様々な作用を発揮します。レチノイン酸によって細胞分化や増殖に関連する500以上の遺伝子が誘導されると言われています。
レチノイン酸に変換されて遺伝子発現を介して作用を発揮する以外に、レチノイン酸に依存しないビタミンA(レチノール)による直接作用もあります(後述)。
ベータカロテンは体内でビタミンAに変換されます。ベータカロテンやビタミンA(レチノール)は食品から摂取され、レチノールは肝臓で貯蔵されて必要に応じて血中に放出され、血清濃度は1~2μMの範囲で維持されています。
細胞内に取り込まれたレチノールはまずレチノール脱水素酵素によってレチナールアルデヒド(レチナール)に変換され、さらにレチナールアルデヒド脱水素酵素によってオール・トランス・レチノイン酸(All-Trans Retinoic Acid:ATRA)になり、イソメラーゼで9-シス・レチノイン酸(9-cis RA)になります。ATRAと9-cis RAが遺伝子発現に関与します。(下図)
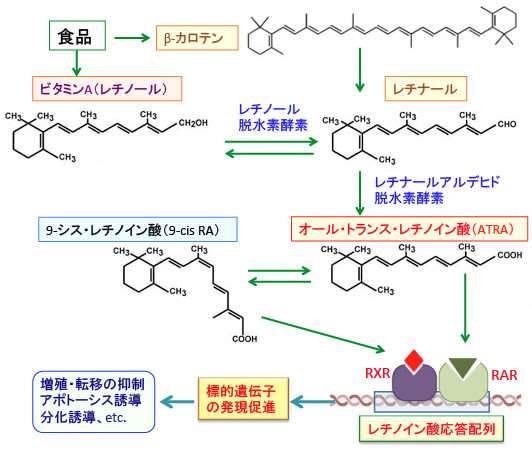
All-trans-RAは全ての不飽和炭化水素鎖がトランス型になっているレチノイン酸で、9-cis-RAというのは9番目の炭素のところでシス型の構造になっているレチノイン酸という意味です。
この構造の違いによって分子式(C20H28O2)は同じでも立体的な大きさに違いが生じるので、RARとRXRの2つの受容体のリガンド結合部位への親和性が異なるということです。
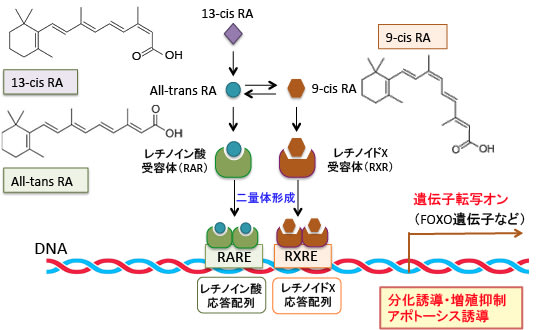
レチノイドによって発現が調節される遺伝子は、細胞の分化や増殖や死(アポトーシス)の制御に重要な働きを担っているため、その機能異常は細胞のがん化に関連し、ある種のがんに対してレチノイドが効く場合があります。
例えば、レチノイン酸の二重結合がすべてトランス型になったall-trans retinoic acid(ATRA)は急性前骨髄球性白血病の特効薬になっています。急性前骨髄球性白血病は白血球に分化する途中の骨髄細胞が腫瘍化した白血病で、オールトランスレチノイン酸によって途中で止まった分化を誘導することによって増殖能を失わせ、死滅させることができるのです。
また、RXRαのアゴニストとして合成された非環式レチノイドが肝臓がんの再発を予防する効果が報告されています。このように、幾つかのがんにはレチノイドは増殖抑制や分化誘導やアポトーシス誘導などの抗がん作用を示します。
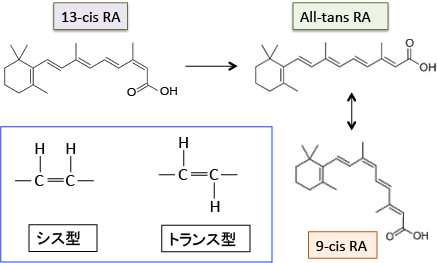
難治性にきびの治療に用いられている13-cisレチノイン酸(イソトレチノイン)は、体内でAll-trans レチノイン酸に変換されて効果を発揮します(下図)。All-trans レチノイン酸は9-cis レチノイン酸に変換します。これらのレチノイドは単独では抗腫瘍効果は弱いのですが、他の治療との組合せで抗腫瘍効果が高まることが報告されています。
しかし、予想に反してベータカロテンの摂取が喫煙者で肺がんの発生が増えるという事実が明らかになりました。ベータカロテンが喫煙者に肺がんの発生を促進するというのがはっきりしたのは1996年です。米国国立がん研究所は1996年初頭に「ベータカロテンの栄養補助剤は、がん予防効果がないだけでなく、肺がんのリスクを高めるおそれがある」と発表しています。
細胞内でレチノールをオール・トランス・レチノイン酸(ATRA)や9-シス・レチノイン酸(9-cis RA)に変換できれば、ATRAや9-cis RAの遺伝子転写活性によって、細胞分化が誘導されて幹細胞は成熟細胞に変化します。
がん幹細胞の増殖を抑制する目的では、活性型のオールトランス・レチノイン酸か体内でATRAに変換される13-cis レチノン酸(イソトレチノン)の使用が有効ということになります。
また、がんの代替医療では、ベータカロテンの大量摂取を目的としたニンジンジュースの大量飲用が広く行われていますが、最近のがん幹細胞の研究やビタミンA(レチノール)の代謝の研究は、ベータカロテンの大量摂取は「がん幹細胞の増殖を促進する」という可能性を指摘していることを知っておく必要があります。
| « 395)ビタミンD... | 397) 漢方がん... » |



