がんの予防や治療における漢方治療の存在意義を考察しています。がん治療に役立つ情報も紹介しています。
「漢方がん治療」を考える
547) がん検診の不都合な真実(その3):がん検診ががん患者を作り出している
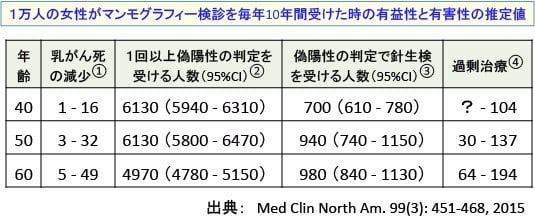
図:1万人の女性が1年に1回のマンモグラフィー検診を10年間受けた場合、乳がんによる死亡が防げる人数は40歳で1〜16人、50歳で3〜32人、60歳で5〜49人と推定されている(①)。しかし、10年間の間に1回以上の偽陽性の判定(乳がんでないのに乳がんの疑いの診断)を半数以上の人が受け(②)、1000人前後は乳がんではない(偽陽性)のに針生検(バイオプシー)を受ける(③)。がんという診断が確定すると手術などの治療を受けるが、この中には放置しても症状を起こすことも無く、死亡の原因になることもない非常に増殖の遅い乳がんが含まれている(④)。この過剰診断・過剰治療の数は年齢が高いほど多い。10年間マンモグラフィー検診を受けると100人から200人に一人が無駄な治療を受けることになる。乳がん死亡の減少は試験によって開きがあるが、厳密にランダム化された3件の臨床試験では、乳がん死を減らす効果が無いという結果が出ている。さらに、マンモグラフィー検診には全死因死亡の数を減らす効果はない。()内は95%信頼区間(95%CI)
547) がん検診の不都合な真実(その3):がん検診ががん患者を作り出している
【がん検診の感度を上げると選択性が低下し過剰診断が増える】
どんなに食生活や生活習慣に注意しても、発がんリスクを3分の1くらいに減らせるのが限界です。酸素呼吸をする限り体内では活性酸素が発生しDNAに変異を起こしています。毎日数千億という数の細胞が分裂して新しい細胞に置き換わっていますが、ある一定の確率でDNA複製のエラー(変異)が発生します。
宇宙線や紫外線や食品由来の発がん物質など、避けることが困難な発がん要因が多数存在します。
がんになった人の3分の1以上は、「運が悪くてがんになった」と言えます。
そこで、症状がまだでない小さい段階でがんを発見して除去すれば、がん死を防げる可能性が高くなります。それを理論的根拠にしているのが「がん検診」です。
画像診断法などの診断技術の発展によって数mmの小さい腫瘍性病変が数多く見つかるようになりました。例えば、ヘリカルCTを用いれば、胸部X線検査の10倍以上の異常を発見できます。しかし、これらの小さな病変の多くが放置してもよい病変であることが明らかになっています。
がんを早期に発見するために診断技術を上げれば上げるほど、治療の必要のない病変が見つかるというジレンマが発生しています。
がん検診は、「がんは放置すると進行し致死的となる」という前提を根拠にしていますが、放置しても致死的とはならないがんも数多く存在します。
増殖が極めて遅いがんでは、症状が発現する前に他の原因で死亡してしまう可能性が高くなります。老衰で死亡した人を解剖すると、がんが発見されることが多くあります。このようながんを診断し治療することは、受診者にとって不利益につながります。
がん検診による過剰診断のデメリットについて十分に理解しておく必要があります。
【がんの進行は極めて不均一】
がん検診によって過剰診断が起こる原因は主に2つあります。第一に、「がん」の中に非常に増殖の遅いものがあるという点です。第二に、画像検査や腫瘍マーカーなど腫瘍性病変を発見する診断法の検出感度が上昇していることです。
その結果、診断法の検出感度が上がるほど、治療が必要ながんを検出する選択性が低下することになります。本来なら治療が必要でなかったがんを無理矢理見つけて、無駄な検査や治療を行っていることが多いのです。
画像検査や症状からがんが疑われても、最終的ながんの診断は、組織の病理検査によって行われます。組織を顕微鏡でみて診断する病理検査によって、がんの組織型や悪性度や浸潤・転移の有無などが診断されます。
がん細胞の「顔つき(異型の度合い)」や周囲組織への浸潤の所見から、そのがん細胞の悪性度もだいたい見当がつきます。細胞分裂に関連するタンパク質の発現レベルから増殖活性を評価することもできます。
ここで重要なことは、形態学的な異型の程度(グレード)や、増殖活性や、周囲組織や脈管への浸潤の程度は、がんによって極めて異なることです。
同じ「がん」という診断でも、進行の早いがんと進行の遅いがんがあります。放置しても寿命を全うできるような遅行性の腫瘍性病変もあれば、数mmの大きさの段階ですでに全身に転移するものや、1ヶ月で2倍以上に成長するような増殖速度の速いがんもあります。(図)

図:がんによって進行の速度は異なる。増殖の早いがんは、早期に症状がでて死に至る(①)。増殖の遅いがんは、症状が出て死に至るまでに長い年月がかかる(②)。増殖が非常に遅いがんは、がんによる症状が出るレベルに増大する前に他の原因で死亡する(③)。病理学的にがん細胞の特徴を示しても、ある一定の大きさから増大しない非進行性のがんがある(④)。この場合は放置しても症状もでないし、死亡の原因になることもない。自然に縮小や消失することもある(点線)。(参考:J Natl Cancer Inst. 102: 605-613, 2010年)
スクリーニングで検出される腫瘍の増殖活性が低い場合(グリソンスコアが3+3以下の前立腺がんのような場合)、スクリーニングの有益性は恐らく全く無いと言えます。むしろ、治療に伴う合併症や副作用の出現を考えると、総合的には有害とさえ言えます。問題は、検診ではこのような増殖活性の低い腫瘍が見つかる確率が高いということです。
その理由は増殖活性の高い腫瘍性病変はスクリーニングの間の期間に増殖して症状が出て見つかりますが、増殖の遅い腫瘍性病変ほど検診でひっかかりやすいと言えます。つまり、検診によるスクリーニングは増殖活性の低い腫瘍を多く見つけている可能性があります。(546話参照)
このような増殖活性の低い腫瘍は、腫瘍の種類によって頻度は異なりますが、全てのがんの15~75%を占めていると考えられています。
また、早期の腫瘍は自然退縮する場合があることも知られています。
このような症状を出すことも進行がんになることもない腫瘍の割合が非常に少なければ、がん検診による過剰診断の問題は許容できます。しかし実際は、このような進行しないがんがかなりの数で存在することが明らかになっています。
このような増殖の遅いがんを検診によって見つけて、無駄な治療が行われている例が多いことが問題になっています。
【検診が始まってから過剰診断が問題になった】
先ほど図で、非常に遅い腫瘍(③)や非進行性の経過をとる腫瘍(④)は、症状が出ないので、通常は見つかりませんが、がん検診で小さな病変を発見できるようになると、これらの無害な腫瘍性病変ががんと診断されて、治療が行われる可能性があります。
医学の教育では「がん(悪性新生物)は進行性に増大して致死的である」と教えられます。この言葉は、検診によるがんのスクリーニングが始まるまでは真実でした。がんによる症状が出てから、がんの診断が行われていたからです。
症状を起こすまで成長する(できる)腫瘍は、その後も進行性に増大して、致死的経過をとる確率は高いと言えます。
がん検診が行われなければ、症状の出る大きさに増大する腫瘍(図の①と②)しか「がん」と診断されません。必然的に「症状がでる大きさまで増大しない腫瘍(図の③と④)は検査も治療も行われることはありません。
つまり、「がんは進行性で致死的である」という考えは、検診によって小さい増殖の遅い腫瘍性病変をみつけるようになってから、真実とは言えなくなりました。がん検診によって、放置してもよい腫瘍性病変まで治療の対象になってきたからです。
がん検診が無かった時代には、放置しても問題ない増殖活性の低い腫瘍は症状を出さないので、発見されることも治療されることもありませんでした。
しかし、検診が行われるようになると、この自然経過での選択が行われないため、治療しなくても良いものまで発見されて治療されるようになってきました。
最近の多くの研究で、検診による過剰診断がかなり多いことが明らかになっています。
ある論文では、マンモグラフィーで発見された乳がんの25%、胸部X線検査や喀痰検査で発見された肺がんの50%、PSA検査で発見された前立腺がんの60%は過剰診断であると推定しています。過剰診断は治療の必要のないがんを発見して、がん治療を行っていることを意味します。(J Natl Cancer Inst. 2010 May 5;102(9):605-13.)

図:がん検診が行われなければ、症状の出る大きさに増大する腫瘍(①と②)しか「がん」と診断されない。③や④の経過をとる腫瘍は、症状が出ないので、通常は見つからない。がん検診で小さな病変を発見できるようになると、これらの無害な腫瘍性病変ががんと診断されて、治療が行われる可能性がある。
【成人のほぼ100%に潜在性の甲状腺がんが見つかる】
エコー検査などの診断法の進歩が増殖活性の低い甲状腺がんの発見を増やしていることが指摘されています。
1975年から2009年までの間にアメリカ合衆国では甲状腺がんの罹患率が約3倍に増えています(10万人あたり4.9人から14.3人に増加)。しかしながら、甲状腺がんによる死亡者の数はほぼ一定です(10万人当たりの甲状腺がんによる死亡者数は0.56から0.52とほぼ一定)。
この罹患率の増加の原因は2cm以下の小さい乳頭がんの発見によるものであることが指摘されています。この小さい乳頭がんは甲状腺がんの中で最も増殖活性の低い腫瘍です。
フィンランドの成人の研究では、剖検において甲状腺を2.5mmの間隔でスライスして病理検査をすると、生前に甲状腺疾患の既往がない人の36%において、一つ以上の乳頭がんが発見されました。
2.5mmのスライスでは2.5mm以下の小さな乳頭がんの見逃しもあるので、実際の頻度はもっと高いと言えます。
この論文の著者は、甲状腺のスライスの間隔をもっと短くして徹底的に検査すると、100%近くに乳頭がんが見つかると結論づけています(Cancer.56(3):531-538, 1985年 )
アメリカ合衆国の成人人口のうち、甲状腺に触知できる結節性病変が見つかる率は4~7%に過ぎませんが、超音波で検査すると約50%の人に小さな結節性病変が見つかるという報告があります。
他の報告をまとめると、50~70歳の人には、潜在性の小さな甲状腺がんを含めて、甲状腺がんを持っている確率は36~100%で、一生の間に甲状腺がんで死亡する確率は0.1%と計算されています。
つまり、放置してもよい潜在性の甲状腺がんを全て検出して甲状腺がんと診断して治療すると、99.7~99.9%が過剰治療になる計算です。
1980年代中頃からの超音波検査と針生検の急速な広がりによって、検診による小さな甲状腺がんの発見が増えましたが、その多くは治療の必要ないものであることが指摘されています。
超音波で初めて検出されるような触知できないレベルの甲状腺がんのほとんどは、非常に増殖活性が低い腫瘍性病変であるので、超音波による検診は中止すべきだという放射線専門医の意見があります。つまり、甲状腺がんをエコーで検出する検診はほぼ無駄な医療行為だと結論づけられます。
米国予防医学専門委員会(The U.S. Preventive Services Task Force)は、予防医学専門の医師や疫学研究者などから構成される委員会で、予防医学に関する有効性のエビデンスを検討し、診療における提言を出しています。
この米国予防医学専門委員会は2017年5月に、無症状の成人に対して、頸部触診や超音波を用いた甲状腺がんのスクリーニングを推奨しない(推奨度D)とする勧告を発表しています。
米国予防医学専門委員会は、アルファベット5段階(A、B、C、DまたはI)で推奨グレードを割り当てています。
グレードAは「十分な有益性がある(推奨する)」、グレードBは「中等度の有益性がある(推奨する)」、グレードCは「無症状に人には有益性は少ない(推奨しない)」、グレードDは「有益性が全くないか、むしろ有害性が有益性を上回る(反対する)」、グレードIは「有用性と有害性のバランスを評価するには十分なデータが無い」と定義されています。
推奨グレードがDというの「甲状腺がんの検診は有害性が有益性を上回る」という十分なエビデンスがあるということです。
(ただし、小児期の頭頸部への放射線被曝歴、甲状腺がん家族歴、家族性甲状腺髄様がん、多発性内分泌腫瘍症候群2A/2B型など、甲状腺がんの危険因子を有する患者には適用しないことが明記されています)
【高齢者の前立腺がんの半分以上はほとんど進行しない】
前立腺がんはがんの中でも過剰診断と過剰治療のリスクが最も高い腫瘍です。
剖検では多くの男性の前立腺に腫瘍がしばしば見つかり、高齢者ほどそれらの腫瘍の増殖活性は低く、60歳以上では50~60%はほとんど進行しない「潜在がん(occult cancer)」と言われています。
事故で亡くなった人や他の病気(前立腺がん以外の疾患)で亡くなった男性の剖検では、60歳以上では30~70%の率で前立腺がんが見つかっています。しかし、男性において一生の間に転移を有する前立腺がんが発見されたり前立腺がんで死亡する率は4%程度です。これは、潜在がんを含め全ての前立腺がんを検出すると、その87~94%が過剰診断になることを意味します。
PSAを頻回に測定し、前立腺から10~12カ所のバイオプシー(生検)を行い、場合によっては何回も生検(針を刺して組織を採取して病理学的に検査する方法)を行うことによって、小さな低悪性度の腫瘍がしばしば発見されます。
このようにして発見された前立腺がんの場合、単に経過観察を行い、明らかに悪性度のグレードが高くなったり腫瘍体積が大きくなった時のみ治療を行うという治療方針で、5年生存率は99%、10年生存率は97%であったという報告があります。この結果は、これらの前立腺がんの増殖活性が極めて低いことを示唆しています。
PSAによる前立腺がんの検診では、67%が過剰診断という報告があります。
このような前立腺がんは増殖活性が極めて低いのに、90%以上で放射線治療や手術が行われ、治療に伴うなんらかの合併症や後遺症(性機能や排尿機能の障害、胃腸障害など)は15~20%の患者で起こっています。さらに、放射線治療による2次がんの発生リスクや、治療に伴う費用も増えています。
頻回に生検を行えば、費用や不安が増えるだけでなく、細菌感染によって敗血症を引き起こすリスクもあります。
低悪性度の前立腺がんは直ぐに治療を開始するのではなく、経過観察をしてその増殖活性を見極めてから治療を選択すれば、過剰治療による合併症や後遺症の発症リスクを低下できることは確かです。
【ヘリカルCTによる肺がん検診は過剰診断が多い】
肺がんは多くの国でがん死亡原因のトップに位置しています。診断時に70%の患者はステージ3か4の状態にあり、このような進行した場合の5年生存率は10%以下です。
一方、ステージ1の5年生存率は70%前後で、ステージ2の5年生存率は40%程度です。
この事実は、肺がんを早期に診断して治療を行う方法が肺がんによる死亡を減らすことを示唆しています。
しかしながら、肺がん検診や剖検の研究結果は、検診で見つかった肺がんの多くは「増殖活性が低い」腫瘍であり、増殖が早いと診断された肺がんでも、その20~25%は過剰診断と推定されています。
米国での肺がん検診(胸部X線と喀痰細胞診)の臨床試験では、検診で見つかった90例中46例(51%)が過剰診断と報告しています。(J Natl Cancer Inst 98(11): 748-756, 2006年)
日本における低線量のヘリカルCTを用いた検診では、胸部X線検査の約10倍の検出感度が報告されています。
この検診を開始して3年後の時点で、喫煙者と一度も喫煙したことのない人(喫煙非経験者)の2群間で肺がんの検出率はほぼ同じでした。
多くの疫学研究から、喫煙者の肺がん発生率は喫煙非経験者の15倍高いという結果が得られているので、このヘリカルCTの検診で、喫煙者と喫煙非経験者の肺がん発見率が同じというのは、かなりの数(90%以上)が過剰診断の可能性が示唆されます。
実際、低線量ヘリカルCTの検診を受けたグループでは、39%が何らかの異常所見を指摘され、精密検査でその96%が偽陽性(実際はがんでないということ)であったという報告があります。
直径が1cm以下の結節の場合、がんである確率は1.5%に過ぎないという結果が報告されています。
そのため、米国予防医学専門委員会(US Preventive Services Task Force)は、「低線量ヘリカルCTによる検診は、一般的には有益性が有害性に勝っているという判断が正当化されているが、これはがん専門の医療機関で、肺がんのリスクが非常に高い集団を対象にした場合しか当てはまらない」と結論しています。さらに「低悪性度の病変を見つけることの有益性のみでなく、その有害性(検査行為による合併症、放射線被曝、QOLに対する影響など)」について患者に説明することを推奨しています。
【マンモグラフィー検診で発見される乳がんの4分の1は過剰診断】
がん検診の有効性を評価するために、検診を受けた群と受けなかった群に無作為に分け、長期間に渡って追跡調査する研究が行われています。
検診が有効であれば、「検診群は初期のがんの発見が増え、進行したがんの発見数は減る」という結果になるはずです。
もし、検診で見つかったがんが全て進行がんになるのであれば、長期間追跡すれば、検診を受けなかった群と受けた群ではがんの発生数は同じになるはずです。(ただし、検診群では初期のがんが多いという違いはあるはずです。)
45~69歳の約42000人を対象に、マンモグラフィーによる検診を受けた群と受けなかった群に分けて、ランダム化二重盲検試験を行った結果が報告されています。
15年後の乳がん発生数は検診群が741例、非検診群が626例で、非検診群に比べて検診群では115例多くの乳がんが見つかっています。
単純に計算すると、検診群で見つかったがんの約16%(741例中115例)が過剰診断ということになります。
しかし、マンモグラフィーによる検診群に分けられた人のなかには、マンモグラフィーではなく、臨床症状で見つかった人たちがいます。つまり、検診群でも、検診で見つかったのは477例で、264例は症状が出てから乳がんの診断がついています。したがって、検診のみで見つかった477例中の115例(24%)が過剰診断という計算が正しいということになります。
つまり、「45~69歳の女性をマンモグラフィーで検診するとがんと診断された4人に一人が過剰診断の可能性がある」という結果です。(BMJ. 2006 Mar 25; 332 (7543): 689-92.)
米国からの報告では、1983年以降、浸潤性乳がんの罹患率は増加しています。特に、低悪性度の性質をもった浸潤性乳がんの発生頻度が増えています。
低悪性度の乳がんの診断数の増加は、検診による過剰診断が原因であることは十分に認識されていますが、その程度は過小に見積もられているという指摘があります。検診によって過剰診断されている症例は、前述のように25%程度ではなくもっと多いという指摘があります。
検診で発見された浸潤性乳がんのうち、30%くらいは極めて悪性度の低い(ultra-low risk)腫瘍であることが、腫瘍組織の分子解析が示されています。
【若い人の乳がん検診は有害】
マンモグラフィ(Mammography)とは、乳房専用のレントゲン検査のことで、専用のX線装置で乳房を圧迫しながら撮影します。触っても判らない小さな乳がん、しこりを作らない乳がん、乳がんの可能性のある石灰化を見つけることができ、乳がんの早期診断に使われています。
「マンモグラフィによる乳がん検診を受けましょう」というような乳がん検診キャンペーンが行われていますが、それに対して科学的エビデンスが無いという反対意見が多くあります。特に20~30代の若い人への乳がん検診の有効性に科学的根拠はなく、不必要な検査につながるなど不利益が大きいことが指摘されています。
米国予防医学専門委員会は2009年11月にガイドラインを改訂し、40~49歳の女性に対するマンモグラフィによる定期的な乳癌検診を、「推奨B:有益性は中程度」から「推奨C:推奨しない。実施には個々人に対し考慮が必要」に引き下げました。
マンモグラフィ検診には乳がん死亡率15%減というメリットがありますが、偽陽性による過剰治療などのデメリットを重視して「推奨しない」という評価になったのです。
米国予防医学専門委員会は50~74歳のマンモグラフィー検診を推奨しています。検診によるメリットが最も大きいのは60~69歳の女性です。50歳未満は有害性のデメリットが大きいので推奨しないという結論です。
出産能力がある年代の女性では、乳腺が発達しているため、マンモグラフィで正常な乳腺と乳がんを見分けることが難しく、偽陽性・偽陰性の率が高くなります。そのため現在、40歳未満の女性にはマンモグラフィは推奨されていません。
40代、50代と年を経るに従って乳腺は衰えて検査は行いやすくなりますが、40~49歳の女性におけるマンモグラフィによる検診には議論があります。日本では40歳以上のマンモグラフィーを推奨しています。
また、米国予防医学専門委員会のガイドラインでは、1年に1回のスクリーニングより2年に1回のスクリーニングの方が有益性が高いと提言しています。
毎年の検診と2年に1回のスクリーングの比較では、がん死亡に対する効果は同じでした。しかし、過剰診断は2年に1回の方が少ないことが示されたからです。
日本ではがん検診の不利益や有害性については、受診者に正確に伝える努力はまだ足りないという指摘があります。
【乳がん検診で多くの人が不要な切除を受けている】
マンモグラフィ(乳房X線撮影法)による乳がん検診の利益と有害性に関して多くのランダム化比較試験が行われており、様々な評価が報告されています。
多くの論文の中で最も信頼できると思われるコクラン・コラボレーション(The Cochrane Collaboration)による最新のレビューを紹介します。(Cochrane Database Syst Rev. 2013 Jun 4;(6):CD001877.)
コクラン・コラボレーションというのは、治療や予防に関する医療技術を評価する世界各国の研究者が参加しているプロジェクトです。無作為化比較試験を中心に、世界中の臨床試験の結果を収集し、試験の質的評価を行い、統計学的に統合して、その結果を医療関係者や医療政策決定者や消費者に届け、合理的な意思決定に供することを目的としています。
コクラン・コラボレーションの最近の報告では、マンモグラフィによる乳がん検診を受けたグループと、マンモグラフィ無実施のグループを比較したランダム化試験の中から、バイアスのある試験(臨床試験の対象となった集団の抽出に偏りがある)を除外し、適格と評価された臨床試験に含まれる39歳から74歳の約60万例の女性を分析の対象としました。
適切にランダム化された3件の試験では、13年目の乳がん死亡率の有意な低下を示しませんでした(相対リスク:0.90、95%信頼区間:0.79~1.02)。4件の準ランダム化試験(ランダム化が十分でない)では、乳がん死亡率の有意な低下を示し、相対リスクは0.75(95%信頼区間:0.67~0.83)でした。
全7件の試験を統合した乳がん死亡の相対リスクは0.81(95%信頼区間は 0.74~0.87)でした。
適切にランダム化された試験では、10年後の乳がんを含むがん死亡率(相対リスク:1.02、95%信頼区間: 0.95~1.10)、または13年後の全死亡率(相対リスク:0.99、95%信頼区間:0.95~1.03)に対して乳がんスクリーニングの効果を認めませんでした。
この論文の著者らの結論は「マンモグラフィーによる乳がんのスクリーニングによって乳がんの死亡率が15%減少し、過剰診断と過剰治療が30%起こると推定される」というものでした。
マンモグラフィによる乳がんのスクリーニングは、乳がん死亡率を低下させる可能性があります。このレヴューでは「乳がん死亡率が15%減少する」と推定しています。しかし、適切にランダム化された3件の臨床試験の結果だけを対象にすると、13年目の乳がん死亡率、10年後の全がん死亡率、13年後の全死亡率は有意な低下は認められていません。
乳がんによる死亡を一人減らすために、スクリーニングを受けていなければ診断されなかった10人の健康女性が不必要に治療されています。さらに、偽陽性所見(がんで無いのにがんと間違われた)のため、200人を超える女性が何カ月も不安などの著しい心理的ストレスを経験するというデメリットがあるという結論です。
スクリーニングに参加するかどうか決める前に利益と有害性の両方について十分な情報が確実に与えられるようにすべきだと提言しています。
つまり、マンモグラフィーによる乳がん検診には、無視できない有害性があることを知っておく必要があるということです。
さらに、乳がん治療の大幅な進歩と乳がんに関する意識が高まったため、最近のスクリーニングの絶対的効果は以前よりも小さい可能性が高いと記載されています。
進行した乳がんの発生数はスクリーニングによってほとんど減少しておらず、過剰診断が増えていると言っています。
最近は乳がんの死亡率が低下していますが、これは検診による早期発見による恩恵ではなく、治療法の発達の寄与が大きいという意見が優勢です。
JAMAの2014年の論文では、「年齢によって有益性は異なり、1万人の女性が1年に1回のマンモグラフィー検診を10年間受けたとして、避けられる(防げる)乳がん死は、40から49歳で5人、50から59歳で10人、60から69歳で42人」と推定されています。」(JAMA. 2014 Apr 2;311(13):1327-35.)
乳がんを早い段階(小さい)段階で見つけるメリットはあります。早期に小さい段階で発見されれば、より少ない治療で済みます。
腫瘍が小さく、転移がない状態であれば、乳房温存手術の適用率が高く、補助化学療法の必要性も低下します。
検診で小さい段階で発見されれば、乳房全摘やリンパ節廓清や補助化学療法などの治療の必要性が減少します。
しかし、米国のデータでは、検査を受けた人の10%くらいが偽陽性(乳がんでないのに「乳がんの疑い」と判定される)の判定を受けています。
1万人の女性が1年に1回のマンモグラフィー検診を10年間うけると、その10年間に一度は偽陽性の判定を受けるのが4970人から6130人と推定されています。つまり10年間スクリーニングを受けると約半分の人が少なくとも1回は偽陽性の判定で、再検査を受け、そのうちの700から980人が不必要なバイオプシー(針生検)を受けています。
1万人の女性が毎年1回のマンモグラフィー検診を10年間受けると、30〜194人が過剰診断で不必要な治療を受けると推定されています。(トップの図)
しかし、現時点では、どのがんを放置して良いのか判断が困難です。強いて言えば、腫瘍が小さくて、病理検査で異型度のグレードが1か2で、ホルモン受容体(エストロゲン受容体やプロゲステロン受容体)が陽性のものは生物学的な悪性度が低く、放置しても良い可能性が高いと言えます。しかし、断定は困難です。
乳がんと診断されれば、治療するしかありません。したがって、がん検診を受ければ一定の割合で過剰診断と過剰治療が起こるのは避けられないのです。
【小さいがんは増殖が遅いから小さい】
一般に、小さいがんほどリンパ節や他臓器への転移が少なく、治療後の再発率が低く、予後が良好です。
この事実に対して、医者や研究者やがん患者を含めてほとんどの人は「がんがまだ小さい早い段階で発見して治療をしたから予後が良いのだ」と考えます。
「がんが小さい=早期発見」だと考えています。大きくなる前に発見して治療したから予後が良いと考えます。
しかし、もう一つの考え方があります。
小さながんの多くは、「早く発見されたから小さい」のではなく、「生物学的に悪性度が低く、増殖が非常に遅いので、大きながんにはならないので小さい」という考えです。
小さいがんは増大速度が遅いので小さい段階で見つかるものが多いという考えです。
がん検診が行われていない時代は、進行性に増大するがんしか見つかりませんでした。このような進行性に増大するがんの多くは死に至るようながんです。
そこで、大きくなる前に発見して小さい段階で治療すれば、がんの治療成績は向上するはずだという仮説のもとに初まったのががん検診です。
早期発見・早期治療が有効なのは、がんの多くが進行性に増大し、悪化する場合です。この場合は、小さい段階に発見して手術で切除することは有益だと言えます。
しかしもし、1cmくらいのがんのうち増大して死に至るようながんに進行するのが半分だとすると、残り半分の治療は無駄な治療になります。
がん検診というのは、「多くのがんは進行性に増大して死に至る」という前提で始まった一つの大きな実験です。しかし、この実験は前提が間違いだった可能性が最近指摘されるようになったのです。
つまり、「がんの多くは進行性に増大して死に至る」というのは間違いのようだと、多くの研究者が気づき始めたのです。
発見された小さながんの多くは、「早く発見されたから小さい」のではなく、「生物学的に悪性度が低く、増殖が非常に遅いので、大きながんにはならない」ので小さいのだ、という結論です。
小さながんを切除して治療を行えば、一般に予後は良好です。これは早期に治療を受けたからではなく、もともと生物学的に大人しいがんであったという考え方です。
今月のNew England Journal of Medicineに以下のような論文が報告されています。
Are Small Breast Cancers Good because They Are Small or Small because They Are Good?(小さな乳がんは小さいからタチが良いのか、タチが良いから小さいのか?)N Engl J Med. 2017 Jun 8;376(23):2286-91.
乳がんの生物学的な悪性度はグレード分類とエストロゲン受容体(ER)とプロゲステロン受容体(PR)の発現で大まかに評価できます
グレード分類はがん細胞の顔つきの悪さの程度です。核異型や核分裂像などで判断します。グレード1〜3の3段階に分けます。グレード1は低異型度で、グレード3は高異型度で、グレード2はその中間です。
エストロゲン受容体(ER)とプロゲステロン受容体(PR)の発現量が多い乳がんは分化度が高く(正常細胞に近い)、ホルモン受容体を発現していない乳がんは一般に分化度が低い(悪性度が高い)と考えられます。
グレード1や2でホルモン受容体の発現の多い乳がんは生物学的に悪性度が低い(予後が良好)と言え、グレード3でホルモン受容体の発現が無い乳がんは悪性度が高い(予後不良)と言えます。
この論文では、米国のイェール大学(Yale University)の研究チームは、サーべイランス・疫学・最終結果(Surveillance, Epidemiology, and End Results:SEER)のデータベースから、2001〜2013年に診断された浸潤性乳がんを対象にして、3つの生物学的因子(悪性度[グレード]、エストロゲン受容体[ER]、プロゲステロン受容体[PR])に基づく12の組み合わせを用いて、次の3つの予後グループに分類しました。
(1)生物学的にfaborable(タチが良い):グレード1/ER陽性/PR陽性、グレード1/ER陽性/PR陰性、グレード 1/ER陰性/PR陽性の3群で13万1,896例
(2)生物学的にunfaborable(タチが悪い):グレード 2/ER陰性/PR陰性、グレード 3/ER陰性/PR陰性、ゲレード 3/ER陽性/PR陰性、グレード 3/ER陰性/PR陽性の4群で13万5,388例
(3)他のすべての群は「中間的」とみなされた。31万8,325例
faborableというのは「好意的」という意味ですが、がん細胞の性質が大人しく、増殖が遅く、予後が良く、生存率が高いグループです。
Unfaborableは「好意的でない」という意味で、悪性度が高く、生存率が低く、予後が悪いグループです。
このように分類して、腫瘍の大きさによって、タチの良い(予後良好な)乳がん(faborable)とタチが悪い(予後が悪い)乳がん(unfaborable)とその中間の乳がんの分布を比較しています。
その結果、40歳以上の女性では、予後良好な「生物学的favorable」な乳がんは、最大径が1cm以下の腫瘍の38.2%を占めましたが、5cm以上の腫瘍では9.0%と少数でした。
これに対し、予後不良な「生物学的unfavorable」な乳がんは、1cm以下の腫瘍では14.1%に過ぎず、5cm以上の腫瘍の35.8%を占めました。
40歳未満の女性でも、同様の傾向がみられましたが、生物学的favorable例が占める割合は40歳以上の約半分であり、unfavorable例の割合がより高い結果でした。
つまり、若い人の乳がんは予後不良な「タチの悪い(生物学的unfavorable)」乳がんが多いという結果です。
40歳以上の場合は、腫瘍が小さいほど予後良好な「タチの良い(生物学的favorable)」乳がんが多く、腫瘍が大きくなるにしたがって、予後不良な「タチの悪い(生物学的unfavorable)」乳がんの比率が増えています。(下図)

図:腫瘍の大きさによる生物学的性状の違い:小さい腫瘍は予後良好なタチの良い(favorable)性質の腫瘍が多く、大きい腫瘍は予後不良なタチの悪い(unfavorable)性質の腫瘍が多い。(出典:N Engl J Med. 2017 Jun 8;376(23):2286-91.)
増殖が早く予後の悪いがんでは過剰診断は稀ですが、増殖が遅く予後の良いがんでは過剰診断が多くなります。
過剰診断は生物学的favorable例が53%、中間例が44%、生物学的unfavorable例が3%という推定を出しています。
生物学的に悪性度が低く(favorable)小さな乳がんは、患者の生存中に大きな腫瘍に進行する可能性は低く、大きな乳がんはすべての小さな腫瘍が進行したのではなく、一部の生物学的に不良な小さながんから進行することが示唆されると考察しています。
マンモグラフィーが始まってから小さい腫瘍の発見が増えていますが、大きいがんの数は減っていないという報告があります。
がんが小さい段階で発見して切除すれば、大きいがんや進行したがんが減るはずですが、そのような効果は認められていません。
マンモグラフィーで見つけている小さいがんは、放置しても増大しないものが多く含まれていると考えるのが妥当かもしれません。
【若い人のがんの増殖が速いのは「増殖が速いから若い段階で見つかった」ため】
若い人に発生するがんは増殖が速いことが知られています。その理由は、「増殖が速いから若い段階で見つかる」ということです。
1個のがん細胞が発生してから、それが臨床的に見つかるまでに10年から20年くらいかかります。増殖の非常に遅いがんでは30年以上かかっている場合もあります。
1個のがん細胞が10億個(約1グラム)になるのに30回分の体積倍加時間を必要とします。(230が約10億)
体積倍加時間が1年だと1グラムに達するのに30年かかります。このようながんだと、見つかってから放置しても10年以上は生存できます。
一方、増殖の速いがんでは数年で臨床症状を引き起こすまで成長します。体積倍加時間が1ヶ月だと30ヶ月で1グラムになり、33ヶ月で約10グラム、37ヶ月で100グラム、40ヶ月で約1kgに成長します。
30歳でがん細胞が発生したと仮定すると、60歳以上で発見されるようながんはもともと増殖が遅いがんであり、予後は良好です。
30歳でがん細胞が発生して35歳で発見されるようながんはかなりタチが悪いがんということになります。
したがって、若い人のがんは一般的に増殖が速く、悪性度が高く、予後が悪いのです。

図:多くのがんは発生してから発見される大きさに成長するまでに10〜30年くらいかかっている。中には増殖速度が極めて速いがんが存在する。そのような増殖の速いがんは、歳が若い段階で発見され、予後は悪い。例えば、腫瘍組織の体積が2倍になる体積倍加時間(Doubling Time)が1年の場合は、発見されるまでに30年かかり、1kgに達するのに40年かかる。一方、体積倍加時間が1ヶ月の増殖の速いがんでは、30ヶ月で発見され、40ヶ月で1kgに達する。したがって、若い人のがん(年齢が若い段階で発見されたがん)は増殖速度が速く、悪性度が高く、浸潤や転移が多く、予後不良のことが多い。
【増殖活性の低い「がん」の病名を変える提案がなされている】
様々なレベルの腫瘍性疾患が「がん(癌)」という病名に包括されています。放置すれば(あるいは治療しても)確実に致死的に進行する悪性度の高いものから、極めて増殖活性や転移能が低いため放置しても死に至らないものもあります。
「がん」という病名を告げられると、ほとんどの患者さんは、そのがんは進行性に増殖し、他の臓器に転移し、そして死につながると思い込みます。多くの医者も同様に考えているので、その考えに従って、患者の治療を行います。
しかしながら、すべての腫瘍が進行性に増殖し死につながるような結果を引き起こすわけではないので、現行の「がん」という病名で一括されている不均一な疾患を適切に区別する必要性が指摘されています。
増殖活性の低い遅行性の腫瘍から、増殖の早い腫瘍が、同じ「がん(cancer)」という名称で呼ばれていることが問題だという指摘です。
2012年3月8~9日に、米国がん研究所(National Cancer Institute)で「がんの過剰診断(cancer overdiagnosis)」に関する問題を検討する会議が行われ、「上皮起源の遅行性病変(indolent lesion of epithelial origin)」、略してIDLEという用語が提案されています。
このような修正が必要な根拠は、悪性度や増殖活性の低い遅行性病変は比較的多く見つかり、がん検診でこれらの遅行性病変を臨床的ながんと過剰診断して、それが過剰治療を引き起こしているからです。
検診(スクリーニング)による本物のがんの検出感度を高めるための努力と同じくらいに、低悪性度のIDLEs(上皮起源の遅行性病変)や放置しても進行しないような潜在的がんを検出しないように、スクリーニングのガイドラインを訂正されるべきであると提言しています。
「がん」という診断になれば、医者はそれを早期に検出し治療する責任があります。しかし、「がん」と呼ばれている腫瘍性病変の中には、実際はがんとしての性質(進行性に増大したり転移する性質)を持っていないようなものもあります。
このような遅行性の腫瘍性病変の名前を変えれば、医者はそのような病変に対して生検(バイオプシー)を繰り返したり治療をすぐに開始する必要が無くなり、経過観察や非浸襲的な治療によってより賢明なアプローチができるようになります。
がん細胞の遺伝子異常の状況は、がんの種類(原発臓器)の違いによって異なり、同じ種類でも個人間で違いがあり、さらに同じがん組織の中でも極めて不均一性があります。
がんの進行の状況もがんの種類によって異なります。増殖速度が非常に遅い腫瘍から早期に転移する腫瘍もあります。
遅行性病変か進行性腫瘍かといった腫瘍のタイプを見極め、過剰診断や過剰治療を避けて適切で有効な治療を行うことができれば、がんによる死亡や検診による副作用を減らし、スクリーニングの総合的な有効性を高めることができます。しかし、腫瘍のタイプを区別できなければ、スクリーニング自体が有害になる場合もあります。検診ではこのような増殖活性の低い腫瘍が見つかる確率が高いのが問題になっています。
このような増殖活性が低く転移を起こすリスクが極めて低い腫瘍性病変の検出が増えているので、このような病変に対しては「がん(cancer)」という用語の代わりに「IDLE(上皮性起源の遅行性病変)」という用語を使用することが提案されています。
最近、PSAによる前立腺がんの検診やヘリカルCTでの肺がん検診などで、小さながんが発見されて、どのようにするべきかという相談が増えています。このような検診では、治療しなくても良いものが多いという医学的根拠を認識しておくことが大切です。検診で見つかった「がん」で無駄な心配をしている方が増えているようにも思います。
私はがん予防を長く研究してきましたが、最近は「早期診断・早期治療でがん死が少なくなる」というのは間違っているように思っています。臨床的ながんを治す治療法の研究の方が重要だと思います。ステージ4の進行がんの治療成績が30年間以上もほとんど進歩が無いことの方が問題です。
最近、有名人ががんになったり、がんで死んだりすることが話題になり、がん検診の推進を主張する意見が時々みられます。先週もワイドショーなどで「若い人も検診を受けた方が良い」という意見をコメンテーターが言っていたのを何回か見ました。
ある選挙で「がん検診受診率100%」を公約にした有名なジャーナリストもいました。
しかし、がん検診の安易な推進は、無駄な医療費と治療の必要のないがん患者を増やすデメリットが想像以上に大きいことを理解しておく必要があります。特に若い人ほどデメリットを多く受けます。
がん検診の理論的根拠である「全てのがんは進行性に増大して致死的になる」という仮説は間違っていること、「増殖の速いがんはがん検診では見つからない」という事実を理解することが重要です。
| « 546) がん検診... | 548) シンバス... » |



