がんの予防や治療における漢方治療の存在意義を考察しています。がん治療に役立つ情報も紹介しています。
「漢方がん治療」を考える
464)進行乳がんの代替医療(その4):ジクロロ酢酸とヒドロキシクエン酸とαリポ酸とメトホルミン

図:がん細胞ではグルコースの取込みと解糖系が亢進し、乳酸の産生が増えている(ワールブルグ効果)。ピルビン酸をアセチルCoAに変換するピルビン酸脱水素酵素の活性を高めてミトコンドリアでの代謝を活性化するとがん細胞の増殖を抑制できる。ピルビン酸脱水素酵素を活性化する物質としてジクロロ酢酸ナトリウムやアルファリポ酸がある(①)。TCA回路で生成されたクエン酸はアセチルCoAに変換されて脂肪やコレステロールの産生に使われる。クエン酸をアセチルCoAに変換するATPクエン酸リアーゼを阻害すると、がん細胞で亢進している脂肪酸合成を抑制できる。ATPクエン酸リアーゼの阻害剤としてヒドロキシ・クエン酸がある(②)。さらに解糖系を阻害する2-デオキシグルコース(③)や酸化的リン酸化を阻害するメトホルミン(④)を併用すると、がん細胞における解糖系と脂肪合成とメバロン酸経路を阻止して増殖を抑えることができる。
464)進行乳がんの代替医療(その4):ジクロロ酢酸とヒドロキシクエン酸とαリポ酸とメトホルミン
【ジクロロ酢酸はクエン酸を増やして抗がん剤感受性を高める】
以下のような論文が最近報告されています。
Dichloroacetate restores drug sensitivity in paclitaxel-resistant cells by inducing citric acid accumulation. (ジクロロ酢酸はクエン酸の蓄積を引き起こすことによって、パクリタキセル耐性細胞における薬剤感受性を復元する) Mol Cancer. 2015; 14: 63. (Published online 2015 Mar 19. )
パクリタキセル(商品名はタキソール)は細胞の微小管に結合して脱重合を阻害することで、がん細胞の分裂を阻害する抗がん剤です。
がん細胞ではミトコンドリアでの酸化的リン酸化が低下しており、これが抗がん剤で死ににくい理由の一つと考えられています。
細胞死の実行にはミトコンドリアの働きが必須なため、ミトコンドリアの活性が低下していると細胞死の実行が起こりにくいと考えられています。そのため、がん細胞はミトコンドリアを使わない糖代謝を行っていると考えられています。
がん細胞の糖代謝の最大の特徴は、酸素が利用できる状況でもミトコンドリアでの酸化的リン酸化を使わないで、酸素を使わない解糖系でグルコースを分解してATPを産生している点です。これをワールブルグ効果と言います。
ミトコンドリアでの酸化的リン酸化を抑制しておれば死ににくくなるので、がん細胞はエネルギー産生の効率より、死ににくくすることを優先して酸素を使わない解糖系でエネルギーを産生していると解釈できます。
ジクロロ酢酸はピルビン酸脱水素酵素キナーゼの活性を阻害して、ピルビン酸脱水素酵素を活性化し、ピルビン酸からアセチルCoAの合成を促進し、ミトコンドリアでの酸化的リン酸化を亢進する働きがあります。(下図)
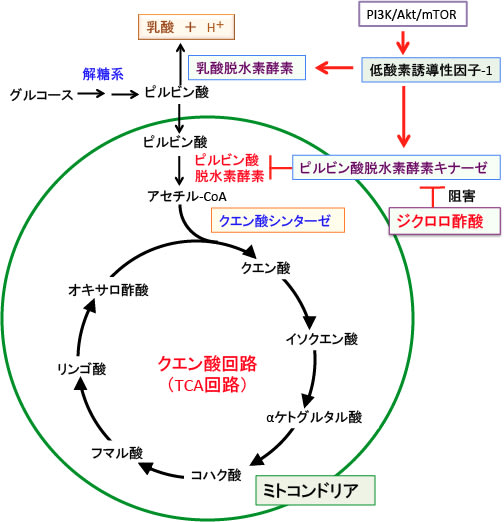
図:グルコース(ブドウ糖)は細胞質での解糖系でピルビン酸になり、ミトコンドリアに入ってピルビン酸脱水素酵素でアセチルCoAに変換され、オキサロ酢酸とアセチルCoAが反応してクエン酸になってクエン酸回路(TCA回路)で代謝される。がん細胞では低酸素誘導性因子-1(HIF-1)の作用でピルビン酸脱水素酵素キナーゼの活性が亢進してピルビン酸脱水素酵素の活性が抑制されているので、ミトコンドリアでの糖代謝が抑制されている。一方、HIF-1は乳酸脱水素酵素の発現を亢進してピルビン酸を乳酸に代謝している。ジクロロ酢酸はピルビン酸脱水素酵素キナーゼの活性を阻害してピルビン酸脱水素酵素の活性を高め、ミトコンドリアでのピルビン酸の代謝を促進する。その結果、がん細胞における乳酸産生(好気的解糖)を抑制する。
上の図のように、ジクロロ酢酸はピルビン酸からアセチルCoAへの変換を亢進し、クエン酸を増やします。クエン酸はミトコンドリアでTCA回路で代謝される他に、ミトコンドリアから細胞質に移行して、脂肪酸などの合成に使用されます。
さらに、細胞質でクエン酸が多くなるとクエン酸は解糖系を抑制する作用があります(後述)。
この論文では、パクリタキセル耐性のがん細胞ではミトコンドリアでの酸化的リン酸化が低下し、細胞内のクエン酸のレベルが低いことを指摘しています。
そこでジクロロ酢酸を投与すると、がん細胞の細胞質でクエン酸が蓄積し、解糖系の阻害が起こり、さらに抗がん剤耐性を引き起こすP糖タンパク質の活性を阻害して、パクリタキセルに対する耐性を抑制できると報告しています。
ジクロロ酢酸が抗がん剤治療の効果を高めることは多くの研究で明らかになっています。そのメカニズムとしては、ミトコンドリアの酸化的リン酸化を亢進して活性酸素の産生を高めることが指摘されています。
さらに、クエン酸が蓄積することも重要だとこの論文は報告しています。
ミトコンドリアを活性化すると抗がん剤感受性を高めることができることは他にも多くの報告があります。
いずれにしても、ジクロロ酢酸を抗がん剤治療に併用する根拠は十分にあるようです。
(ジクロロ酢酸ナトリウムの使用法はこちら)
低酸素誘導性因子-1(HIF-1)を阻害する方法としてジインドリルメタンやシリマリンがあります。 mTORの阻害剤としてラパマイシンがあります。これらを併用すると、ジクロロ酢酸の抗腫瘍効果をさらに高めることができます。(364話参照)
【クエン酸はホスホフルクトキナーゼをフィードバック阻害する】
解糖系やTCA回路や電子伝達系に関与する酵素の一部は、アロステリック制御によって調節されています。
アロステリック制御というのは、酵素にある物質が結合すると構造変化が起こって機能が変化する現象です。
代謝系のある段階の反応が、その系の下流の産物によって阻害されることをネガティブフィードバック調節と言います。
代謝経路でその後に続く産物が高濃度に存在すると、その代謝系での反応がそれ以上必要ないので、酵素活性を阻害して反応を止める制御です。
解糖系の律速段階の1つのホスホフルクトキナーゼ(フルクトース-6-リン酸をフルクトース-1,6-ビスリン酸に変換)は、
最終生成物のATPによりフィードバック阻害を受け、ADPもしくはAMPによって活性化されます。
そして、このホスホフルクトキナーゼはTCA回路(クエン酸回路)の産物であるクエン酸によってもフィードバック阻害を受けます。
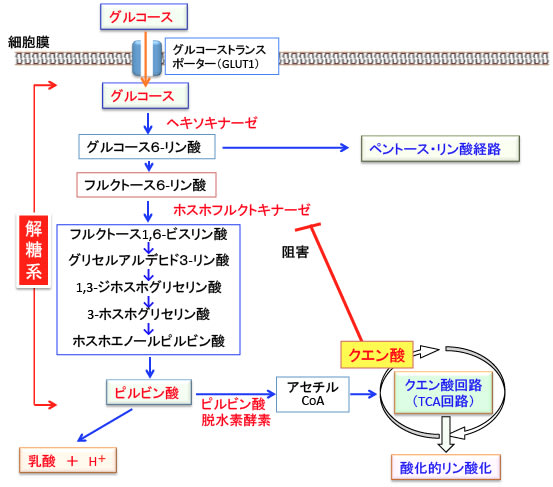
図:クエン酸回路(TCA回路)の産物であるクエン酸は解糖系のホスホフルクトキナーゼをフィードバック阻害する作用がある。
クエン酸による解糖系阻害によるがん治療の可能性を解説した論文はいくつかあります。以下のような論文があります。
Effect of citrate on malignant pleural mesothelioma cells: a synergistic effect with cisplatin.(悪性胸膜中皮腫に対するクエン酸の効果:シスプラチンとの相乗効果)Anticancer Res. 29(4):1249-54.2009年
抗がん剤抵抗性のヒト中皮腫細胞株を使った培養細胞レベルでの実験で、クエン酸を添加するとアポトーシスが誘導されること、抗がん剤のシスプラチンの効果を高めることが報告されています。そのメカニズムとして解糖系のフルクトキナーゼの活性を阻害することによってATPの産生が減少することを挙げています。
Citrate induces apoptotic cell death: a promising way to treat gastric carcinoma?(クエン酸はアポトーシスによる細胞死を誘導する:胃がん治療への可能性?)Anticancer Res. 31(3):797-805.2011年
前の論文と同じ研究グループからの報告です。2種類の胃がん細胞株を用いた実験で、クエン酸が胃がん細胞にアポトーシスを誘導することを報告しています。
Understanding the central role of citrate in the metabolism of cancer cells.(がん細胞の代謝におけるクエン酸の中心的役割の理解) Biochim Biophys Acta. 1825(1):111-6. 2012年
同じ研究グループからの総説です。クエン酸を多く摂取するとがん治療に役立つことを解説しています。 このようにクエン酸は解糖系のフルクトキナーゼをフィードバック阻害するので、ATP産生を抑制することになります。
【クエン酸は脂肪酸合成に使われる】
食事から摂取したグルコース(ブドウ糖)は、解糖系を経てミトコンドリアのクエン酸サイクル(TCA回路)によりエネルギー(ATP)に変換されます。
生成したエネルギーは体が必要とするエネルギーとして利用され消費されますが、その消費量が少ない場合には、グルコースはクエン酸に変換された後、ミトコンドリアを出て脂肪合成の場である細胞質へ移行し、アセチルCoAを経由して脂肪酸そして脂肪、あるいは、コレステロールに変換され、体内に蓄積されます。
アセチルCoAはミトコンドリアを通過できないのですがクエン酸は通過できます。TCAサイクルでできたクエン酸がミトコンドリアの外に出て、ATPクエン酸リアーゼによって脂肪の合成に使用されます。(下図)。

図:TCA回路で作られるクエン酸から脂肪合成を行う最初のステップに働く酵素がATPクエン酸リアーゼ。 がん細胞は細胞の数を増やすために脂肪合成が亢進しており、ATPクエン酸リアーゼの活性が高くなっている。ATPクエン酸リアーゼを阻害すると、脂肪の合成を阻害し、がん細胞の増殖を抑えることができる。
がん細胞では脂肪酸の新規合成が盛んです。
脂肪酸合成酵素(fatty acid synthase: FASN)をはじめ、幾つかの脂質代謝酵素ががんの発生や悪性化を促進することが知られており、これらががん治療の新たな標的分子となる可能性が期待されています。
特にATP クエン酸リアーゼの阻害が、がん治療に有効という報告があります。
クエン酸からアセチルCoAに変換する酵素がアデノシン3リン酸クエン酸リアーゼ(ATP:citrate oxaloacetate lyase, EC 4.1.3.8)です。
糖質を摂取し過ぎると肥満になり易い理由は、グルコースがTCA回路でクエン酸になって、これがATPクエン酸リアーゼで脂肪酸に変換されるからです。
がん細胞が分裂して細胞を増やすためには、DNAや細胞膜など多くの細胞成分を合成する必要があります。脂肪も細胞を作るのに必須で、そのため、脂肪合成に重要な酵素であるATPクエン酸リアーゼは多くのがん細胞で活性が亢進していることが報告されています。
したがって、ATPクエン酸リアーゼの阻害は、がん細胞の増殖を抑制する効果が期待できます。実際に、培養がん細胞を使った実験や、移植腫瘍を使った動物実験などで、ATPクエン酸リアーゼの阻害ががん細胞の増殖を抑制する効果があることが報告されています。
ATPクエン酸リアーゼの阻害剤として、ガルシニア・カンボジアに含まれる(-)-ヒドロキシクエン酸があります。
【ATPクエン酸リアーゼを阻害するヒドロキシクエン酸】
ガルシニア・カンボジア(Garcinia cambogia)の果皮に多量に含まれる(-)-ヒドロキシクエン酸((-)- Hydroxycitric acid、HCA)は、クエン酸より水酸基(-OH)を一つ多く持っている点が違うだけで化学構造が類似しているため、ATPクエン酸リアーゼの酵素活性を競合阻害することが知られています。
ガルシニア・カンボジアはインドや東南アジアに生育する常緑樹で、5~9月頃にオレンジ大の大きさで黄色からやや赤みがかった実をつけます。果実や果皮は柑橘類に似た強い酸味を有し、熟果は果物として生食されるほか、果皮や実は乾燥させて貯蔵し、カレーの酸味付けや魚の塩蔵保存などにも用いられ、長年にわたりスパイスとして利用されています。
インド伝統医学のアーユルヴェーダでは消化を助け食欲を抑える薬として使用されています。
乾燥したガルシニアの果皮には10~30%ものヒドロキシクエン酸を含まれています。
ヒドロキシクエン酸は分子内に不斉炭素を有するため4つの異性体が存在しますが、ATPクエン酸リアーゼの阻害効果を持つのは(-)-ヒドロキシクエン酸(HCA)のみです。
ガルシニア・カンボジアの果皮あるいはヒドロキシクエン酸は脂肪の合成を阻害するので、肥満抑制効果が期待されてダイエットのサプリメントに利用されています。さらに近年、がんの治療にも役立つことが報告されています。

図:熱帯植物ガルシニア・カンボジアの果実に多く含まれる(-)-ヒドロキシクエン酸はクエン酸と競合阻害することによってATPクエン酸リアーゼを阻害することができる。
【アルファリポ酸とヒドロキシクエン酸の併用は抗がん作用を強める】
アルファリポ酸は、多数の酵素の補助因子として欠かせない体内成分で、特にTCA回路(クエン酸回路)のピルビン酸脱水素酵素複合体の補助因子として、ミトコンドリアでのエネルギー産生に重要な役割を果たしています。
糖代謝の促進や抗酸化作用があるので、ダイエット効果や抗老化や美容を目的としたサプリメントとしても人気があります。
一方、ヒドロキシクエン酸は、ガルシニア・カンボジアの果皮に多量に含まれる成分で、クエン酸より水酸基(OH)を一つ多く持っている点が違うだけで化学構造が類似しているため、ATPクエン酸リアーゼの酵素活性を競合阻害することが知られています。
ATPクエン酸リアーゼ(ATP citrate lyase)は細胞内でクエン酸から脂肪合成を行う最初のステップに必要な酵素で、ATPクエン酸リアーゼを阻害すると脂肪の合成が阻害されます。
したがって、ヒドロキシクエン酸も体脂肪を減らすサプリメントとして人気があります。
ダイエット効果のあるこれら2種類のサプリメント(アルファリポ酸とヒドロキシクエン酸)が、がん治療においても効果があることが報告されています。
その理由は、細胞内の物質代謝やエネルギー産生において、正常細胞とは異なるがん細胞の特徴にあります。
その特徴とは、1)ピルビン酸脱水素酵素の活性低下と、2)ATPクエン酸リアーゼの活性亢進です。
がん細胞では、ピルビン酸脱水素酵素の活性が低下し、その結果、ミトコンドリアでのTCA回路と酸化的リン酸化による酸素を使ったエネルギー産生(ATP産生)が低下し、酸素を使わない解糖系でのエネルギー(ATP)産生が亢進しています。
がん細胞では、酸素が十分にある状態でも、酸素を使わない嫌気性解糖系でのエネルギー産生(ATP産生)が亢進していることを約80前にオットー・ワールブルグが発見し、ワールブルグ効果として知られています。
また、ATPクエン酸リアーゼの活性亢進は、がん細胞が分裂して細胞を増やすときに必要な脂肪の合成を高めるためと考えられます。
したがって、ATPクエン酸リアーゼの活性を阻害すると、脂肪の合成が阻害されてがん細胞の増殖を抑えることができます。
さらに、ピルビン酸脱水素酵素の活性を高め、ATPクエン酸リアーゼの活性を阻害して、ミトコンドリアでのTCA回路と酸化的リン酸化が正常化すると、がん細胞はアポトーシスを起こしやすくなることが知られています。

図:がん細胞では解糖系が亢進し、ピルビン酸脱水素酵素の活性が低下し、ATPクエン酸リアーゼの活性が亢進している。ピルビン酸脱水素酵素の活性を高めるアルファリポ酸と、ATPクエン酸リアーゼを阻害するヒドロキシクエン酸を併用すると、がん細胞の増殖を抑えることができる。抗がん剤治療と併用して抗腫瘍効果を高めることができる。
ピルビン酸脱水素酵素の活性を高めるアルファリポ酸と、ATPクエン酸リアーゼの活性を阻害するヒドロキシクエン酸を併用すると、がん細胞の増殖を抑えることが推測されます。
実際に、この仮説を検証している研究グループがあり、その研究結果によると、『アルファリポ酸とヒドロキシクエン酸の併用は通常の抗がん剤に匹敵する抗がん作用を示す』『アルファリポ酸とヒドロキシクエン酸の併用は抗がん剤の効き目を高める』という結果が得られています。以下のような論文があります。
A combination of alpha lipoic acid and calcium hydroxycitrate is efficient against mouse cancer models: preliminary results. (αリポ酸とヒドロキシクエン酸カルシウムの組み合わせは担がんマウスの実験にて有効:基礎研究の結果)Oncol Rep. 23(5):1407-16. 2010年
【要旨】 がん細胞におけるエネルギー代謝の異常については多くの検討がなされている。我々は、がん細胞において異常を起こしている2つの酵素、1)がん細胞で活性が低下しているピルビン酸脱水素酵素と、2)多くのがんで過剰に発現しているATPクエン酸リアーゼ(ATP citrate lyase)に注目して研究を行っている。
αリポ酸はピルビン酸脱水素酵素の補酵素であり、ヒドロキシクエン酸はATP クエン酸リアーゼの阻害剤である。この2つのサプリメントの組み合わせは、強い抗がん作用を持っている可能性がある。
そこで、培養がん細胞を使ってαリポ酸とヒドロキシクエン酸の抗がん作用における相乗効果を検討した。
αリポ酸は用量(0.1 ~10μM)およびがん細胞の種類に応じてがん細胞の数を10~50%減少させた。
ヒドロキシクエン酸は10~500μMの濃度でがん細胞の数を5~60%減少させた。
ヒドロキシクエン酸とαリポ酸を同時に投与すると、抗腫瘍効果は相乗的に増強し、8μMのαリポ酸と300μMのヒドロキシクエン酸の併用でがん細胞は72時間後に100%死滅した。
健常なマウスに、常用される量のヒドロキシクエン酸とαリポ酸を同時に投与しても、毒性は認められなかった。 マウスのがん細胞(膀胱がん細胞MBT-2、メラノーマ細胞B16-F10、ルイス肺がんLL/2)をマウスに移植した実験モデルで、ヒドロキシクエン酸とαリポ酸の組み合わせによる抗腫瘍効果を検討した。
この組み合わせは、腫瘍の縮小や生存期間の延長において、シスプラチンや5-FUなどの通常の抗がん剤と同じレベルの抗腫瘍効果を示した。
基礎実験のレベルではあるが、培養細胞と動物を使った実験の結果から、αリポ酸とヒドロキシクエン酸の組み合わせは有効ながん治療となる可能性が示唆された。臨床試験を行う価値がある。
Adding a combination of hydroxycitrate and lipoic acid (METABLOC ) to chemotherapy improves effectiveness against tumor development: experimental results and case report.(抗がん剤治療にヒドロキシクエン酸とリポ酸を併用すると抗腫瘍効果を高める:実験結果と症例報告)Invest New Drugs. 30(1):200-11. 2012年
【要旨】 がん細胞における代謝の異常は、オットー・ワールブルク(Otto Warburg)によって80年以上前に指摘され、ワールブルグ効果(Warburg effect)として知られているが、最近まであまり注目されていなかった。
しかし、近年、がんの診断や治療との関連において、がん細胞における代謝やエネルギー産生の異常が注目されるようになった。
著者らは、がん細胞の代謝異常の鍵となる酵素であるATPクエン酸リアーゼとピルビン酸脱水素酵素の活性に作用するヒドロキシクエン酸とアルファリポ酸の抗腫瘍効果に関して基礎研究の結果を報告している。
すなわち、3種類のマウスのがん細胞株を使った実験では、ヒドロキシクエン酸とアルファリポ酸の組み合わせは、通常の抗がん剤治療と同等の効果を発揮した。
今回の研究は、通常の抗がん剤治療(特にシスプラチン)の抗腫瘍効果に対して、ヒドロキシクエン酸とアルファリポ酸の組み合わせを併用した場合の影響を明らかにする目的で行った。
マウスのがん細胞(LL/2肺がん細胞、MBT-2膀胱がん細胞)を移植したマウスに、通常の抗がん剤(シスプラチンかメソトレキセート)を投与する実験で、アルファリポ酸とヒドロキシクエン酸を組み合わせた製剤を投与した。
シスプラチンまたはメソトレキセートを単独で使用した場合、あるいはアルファリポ酸+ヒドロキシクエン酸を投与した場合に比べて、シスプラチン(またはメソトレキセート)+アルファリポ酸+ヒドロキシクエン酸の3種類を併用した場合は抗腫瘍効果が著明に増強した。(アルファリポ酸+ヒドロキシクエン酸は、シスプラチンあるいはメソトレキセートの抗腫瘍効果を相乗的に高めた)
肝臓転移を有する膵臓がん患者(80歳女性)に、ジェムシタビン(ジェムザール)とアルファリポ酸とヒドロキシクエン酸を併用した治療を行ったところ、顕著な抗腫瘍効果を得ることができた。
動物実験と膵臓がんの症例の経験から、通常の抗がん剤治療に、アルファリポ酸とヒドロキシクエン酸を併用して投与すると、抗腫瘍効果を高めることができることが示唆された。
Metabolic treatment of cancer: intermediate results of a prospective case series.(がんの代謝治療:症例検討の中間報告)Anticancer Res. 2014 Feb;34(2):973-80.
【要旨】
研究の背景:ヒドロキシクエン酸とアルファリポ酸の組合せが、マウスの実験モデルで腫瘍の増殖を抑制することが複数の研究グループから報告されている。
症例検討:全ての患者は標準的な抗がん剤治療が無効になり、緩和ケアを提案された段階であった。全身状態はKarnofsky performance statusの評価で50から80の間であった。生命予後は2ヶ月から6ヶ月と予測されていた。
抗がん剤抵抗性の転移を有する進行がん患者10例を対象に代謝治療を行った。
アルファリポ酸は600mgを静脈注射し、ヒドロキシクエン酸は500mgを1日3回服用し、低用量ナルトレキソン療法(5mgのナルトレキソン)を就寝時に服用した。
原発は肺がん(2例)、大腸がん(2例)、卵巣がん(1例)、食道がん(1例)、子宮肉腫(1例)、胆管細胞がん(1例)、耳下腺がん(1例)、原発不明(1例)であった。全ての患者は強い抗がん剤治療を受け、効果が認められなくなった状況にあった。
結果:副作用は極めて軽度で一過性の吐き気と嘔吐のみであった。2例は進行して2ヶ月以内に死亡した。2例は標準的な抗がん剤治療に代謝治療を併用し、そのうち1例は顕著な腫瘍縮小を認めた。その他の症例は、病状安定か進行が遅くなった。
結論:この代謝治療は副作用がほとんどなく、抗がん剤治療に抵抗性の進行がん患者に有用であることが示唆された。通常の抗がん剤治療と併用することによって、その抗腫瘍効果を高める可能性が示唆された。これらの臨床経験は今までの動物実験の結果と同じであった。ランダム化臨床試験を行う価値がある。
まだ、予備的な臨床試験の段階ですので、その有効性は確定できませんが、ピルビン酸脱水素酵素の活性を高め、ATPクエン酸リアーゼの活性を阻害する方法は抗がん作用が期待できます。
ジクロロ酢酸はアルファリポ酸と同様にピルビン酸脱水素酵素複合体を活性化します。
さらに、解糖系を阻害する2-デオキシグルコース、メトホルミンを併用するとがん細胞の増殖を抑えることができます。 また、メバロン酸経路を阻止するスタチン(特に脂溶性の
シンバスタチン)の併用も有効です。 脂溶性スタチンは乳がん治療後の再発率を低下させることが報告されています。(404話参照)
がん細胞における代謝異常を特徴を利用する治療は副作用が少なく、がん細胞の増殖を抑えることができます。
ケトン食、ジクロロ酢酸、αリポ酸、メトホルミン、2-デオキシグルコース、ジインドリルメタン、シリマリンの組合せは相乗効果が期待できます。(トップの図と下図参照)
この方法は乳がん以外の多くのがんでも有効です。

★ トリプル・ネガティブ乳がんで死なないためには、治療の早い段階から、エビデンスに基づいた補完・代替医療を利用することが重要です。トリプル・ネガティブ乳がんの補完代替医療については以下のサイトでまとめています。
http://www.f-gtc.or.jp/TNBC/Triple_Negative_Breast_Cancer.html
| « 463)進行乳が... | 465) 進行乳が... » |






