がんの予防や治療における漢方治療の存在意義を考察しています。がん治療に役立つ情報も紹介しています。
「漢方がん治療」を考える
251)アルテミシニンとトゥーユーユー(Tu Youyou)博士とラスカー賞
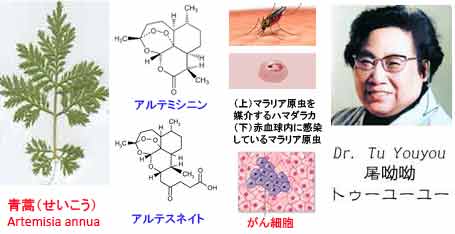
図:古くからマラリアの治療に利用されてきた青蒿(Artemisia annua)という薬草から分離されたアルテミシニン(Artemisinin)とその誘導体(アルテスネイトなど)は、現在マラリアの治療薬として世界中で使用されている。さらに、抗がん作用があることから、がんの代替医療にも使用されている。アルテミシンを発見した女性科学者の屠呦呦(Tu Youyou)博士が、本年度のラスカー賞を受賞した。
251)アルテミシニンと屠呦呦(トゥーユーユー)博士とラスカー賞
【アルテミシニンの発見者がラスカー賞を受賞】
9月13日の朝刊(読売新聞)に以下のような小さな記事が載っていました。
『ラスカー賞に中国人』米国で最も権威のある医学賞とされる「ラスカー賞」が12日発表され、臨床医学賞に中国中医科学院(北京)のトゥーユーユー(屠呦呦)博士(81)が選ばれた。中国人の受賞は初めて。屠博士は1970年代、漢方薬で使う薬草から様々な化学物質を抽出、マラリア治療薬「アーテミシニン」を発見した。
この新聞記事以前に、屠呦呦博士とアーテミシニン(アルテミシニンとも書く)のことを聞いた(読んだ)ことがある日本人は極めて少ないと思います。
アルテミシンはマラリアの治療薬で、マラリアの存在する地域では薬として良く知られています。しかし、日本では現在マラリアという病気はほとんど存在しないので、アルテミシンを知っている医者や薬剤師も稀です。
私は、9年ほど前からアルテミシニンをがんの代替医療に使用しており、アルテミシン関連の論文で屠呦呦博士の話も知っていたので、この記事を読んだとき非常に感慨深く思った次第です。
ネットで「トゥーユーユー」で検索しても屠呦呦博士を記載したサイトはありませんし、「屠呦呦」で検索すると中国語のサイトは多数ヒットしますが、日本語のサイトはヒットしません。「Tu Youyou」で検索すると、多数のサイトがヒットしますが、ラスカー賞受賞関係が多く、最近まではあまり注目されていなかったようです。ユーチューブに屠呦呦博士のインタビュー動画があり、アルテミシニン発見のことを言っています。
ラスカー賞(アルバート・ラスカー医学研究賞)はアメリカ医学会最高の賞で、「アメリカのノーベル生理学・医学賞」とも呼ばれ、医学関係ではノーベル賞に次ぐ権威ある賞です。ラスカー賞を受賞した人のうち68人がさらにノーベル生理学・医学賞を受賞しています(2003年の段階)。
日本では、利根川進博士が1987年にラスカー賞とノーベル生理学・医学賞を受賞している他、6名がラスカー賞を受賞しており、iPS細胞を開発した京都大学の山中伸弥教授も2009年に受賞しています。つまり、ラスカー賞を受賞するというのは、医学の領域でノーベル賞に匹敵するほどの業績を上げたということを意味します。
マラリアは全世界で年間3 ~ 5億人が感染し、100 - 150万人の死者があると報告されています。つまり、マラリアに対して極めて有効なアルテミシンの発見によって、毎年何百万人もの人の命が救われているので、「アルテミシニンの発見」がラスカー賞に値するということです。
今まで薬草から何万種類(あるいはそれ以上の)成分が分離・同定されていますが、それが多くの人の命を救うものであれば、ラスカー賞やノーベル賞に値するということです。
【伝統医学からみつかったアルテミシン】
伝統医学や民間療法で使用されている薬草から活性成分を見つけ、それを医薬品として開発する研究は、中国のみならず日本を含め世界中で行われています。
現在西洋医学で使用されている医薬品の中には、病気の治療に古くから経験的に使用されていた植物や薬草から見つかったものがたくさんあります。
例えば、鎮痛剤のアスピリン(アセチルサリチル酸)はヤナギの樹皮に含まれるサルチル酸(19世紀に分離)が原型で、その副作用を軽減するためにアセチル化して合成された薬剤です。ヤナギの樹皮の鎮痛作用は古代ギリシャ時代から知られており、紀元前400年ごろ「医学の父」と呼ばれるヒポクラテスが、解熱鎮痛の目的でヤナギの樹皮を使用していたという記録があります。
気管支拡張剤として使用されるエフェドリンは、生薬のマオウ(麻黄)から1885年(明治18年)に長井長義博士が抽出しましたが、麻黄は葛根湯や小青竜湯など風邪や喘息などに使用する漢方薬に使用されており、その鎮咳作用や気管支拡張作用は2000年以上前から経験的に知られていました。
このように何千年も前から経験的に病気の治療に用いられていた薬草から見つかった医薬品の例はその他にも数多くありますが、アルテミシンおよびその誘導体のアルテスネイトもそのような薬の一つです。
アルテミシニン(Artemisinin)は青蒿(セイコウ:Artemisia annua)というキク科の薬草から分離された成分で、現在ではマラリアの特効薬として使用されています。Artemisia annuaの和名は「クソニンジン」と言い、世界中に分布しています。
青蒿という生薬は、中国医学でマラリアなど様々な感染症や炎症性性疾患の治療に古くから使用されていました。1972年に中国の湖南省長沙市の郊外で発掘された馬王堆漢墓は2100年以上前に作られた墓(古墳)ですが、その中から見つかった「五十二病方」という医書の中に、青蒿が記載されています。
このように中国医学では古くからマラリアなどの感染症の薬として青蒿が利用され、1970年代には中国の研究者によってその薬効成分のアルテミシニン(Artemisinin)、およびその誘導体のアルテスネイト(Artesunate)やアルテメーター(Artemether)が分離され、抗マラリア薬としての有効性が臨床試験で確認されました。
マラリアは、熱帯・亜熱帯地域の70ヶ国以上に分布し、全世界で年間3~5億人、死者は100~150万人と言われる感染症ですので、その治療薬としてのアルテスネイトなどのアルテミシニン誘導体の開発は、ある本では「伝統薬から開発された医薬品としては、20世紀後半における最大の業績」という表現がなされているほど、医学において重要な成果だと言われています。つまり、アルテスネイトなどのアルテミシニン誘導体の開発は、19世紀に分離されたサリチル酸やエフェドリンなどと匹敵する成果だと認識されているのです。
アルテスネイトは分子の中に鉄イオンと反応してフリーラジカルを産生するendoperoxide bridge を持っています。マラリア原虫が感染した赤血球中では、マラリア原虫によって赤血球中のヘモグロビンが分解してフリーの鉄が蓄積し、その鉄とアルテスネイトが反応してフリーラジカルが発生してマラリア原虫を死滅させると考えられています。
【アルテミシニンおよびその誘導体の抗がん作用】
アルテミシニンおよびその誘導体はマラリアの薬として開発されましたが、がんの代替医療でも10年くらい前から話題になっています。
がん細胞も細胞内に鉄を多く含むことが知られています。鉄は細胞増殖に必要で、がん細胞はトランスフェリンレセプターを多く発現して鉄を多く取り込んでいます。細胞分裂の早いがん細胞ほど鉄を多く取り込んでいると言われています。
がん細胞はスーパーオキシド・ディスムターゼ(SOD)やカタラーゼやグルタチオンペルオキシダーゼなどの抗酸化酵素の発現が少なく、酸化ストレスに対する抵抗力(抗酸化力)が低下していると言われています。そしてがん細胞は鉄を多く含むので、がん細胞内の鉄と反応してフリーラジカルを発生するアルテミシニンやアルテスネイトは、正常細胞を傷つけずにがん細胞に選択的に障害を与えることが推測されています。
実際に、培養がん細胞を使った実験でアルテミシニンやアルテスネイトががん細胞を死滅させる事や、がん細胞を移植した動物実験で、がんを縮小させる効果が報告されています。抗がん剤に抵抗性のがん細胞にも効果が得られることが報告されています。
さらに、抗腫瘍作用を示す投与量で、正常細胞に対する毒性が低く、副作用がほとんど無いという特徴を持っています。アルテスネイトは昔からマラリアの治療に使われていた生薬の成分で、その安全性や副作用が軽度であることが確かめられています。
最近の研究では、アルテスネイトは多彩な作用メカニズムで抗腫瘍効果を発揮することが報告されています。がん細胞内でフリーラジカルを産生して酸化ストレスを高める以外に、血管新生阻害作用、DNAトポイソメラーゼIIa阻害作用、細胞増殖や細胞死のシグナル伝達系に影響する作用などが報告されています。
アルテミシニン誘導体の抗がん作用に関する最近の研究として以下のような報告があります。
1)進行した非小細胞性肺がんの抗がん剤治療にアルテスネイトを併用すると抗腫瘍効果が高まることが、中国で行われたランダム化比較試験で報告されています。
進行した非小細胞性肺がんに対するビノレルビンとシスプラチンを併用した抗がん剤治療に、アルテスネイトを併用した場合の安全性と有効性を検討する目的で、120例の非小細胞性肺がん患者を対象にランダム化比較試験が行なわれています。
病勢コントロール率(著効+有効+不変の患者の割合)はアルテスネイト併用群が88.2%でコントロール群が72.7%で統計的に有意な差(P<0.05)が認められました。さらに、無進行期間は、アルテスネイト併用群が24週に対してコントロール群が20週で、これも統計的に有意な差でした(P<0.05)。
</font>両群の間で副作用(骨髄抑制や消化器症状など)の程度には差は認められませんでした。
この臨床試験の結論として、非小細胞性肺がんのビノレルビンとシスプラチンを使った抗がん剤治療にアルテスネイトを併用すると副作用を増強することなく、抗腫瘍効果を高めることが示されました。
Journal of Chinese Integrative Medicine(中西医結合学報)6(2): 134-138. 2008
2)アルテスネイトは膵臓がん細胞に、複数の作用機序で抗腫瘍効果を示すことが報告されています。
アルテスネイトはがん細胞内に多く蓄積している鉄と反応してフリーラジカルを産生してがん細胞を死滅させます。フリーラジカルによる細胞内小器官や膜の破壊によって起こる細胞死は、そのダメージが軽度の場合はアポトーシスが誘導され、ダメージが強い場合は壊死に近い細胞死が引き起こされると考えられます。
ヒト膵臓がん細胞株を用いた細胞培養の実験で、アルテスネイトはトポイソメラーゼIIaを阻害し、多くの細胞内シグナル伝達系に作用して、膵臓がん細胞の増殖を抑制し、アポトーシスを誘導する作用が認められています。
Biochem Pharmacol. 2009 Aug 1;78(3):273-83.
3)アルテスネイトは膵臓がん細胞を移植したマウスの実験モデルで腫瘍を縮小する効果が報告されています。
100mg/kg(腹腔内投与)のアルテスネイトの抗腫瘍効果は同じ投与量のジェムシタビン(gemcitabine)とほぼ同じレベルでした。しかし、ジェムシタビン投与マウスは体重が平均25%減少し、副作用によって活動性が低下し、18日目には5匹中2匹が死亡しました。一方、アルテスネイトは100mg/kgの投与でも、毒性はほとんど認められませんでした。
Cancer Chemother Pharmacol. 65(5):895-902. 2010
アルテスネイトの抗腫瘍効果の作用機序から、嫌気性解糖系を阻害する半枝蓮を使った漢方薬、がん細胞のミトコンドリアでの活性酸素の産生量を高めるジクロロ醋酸ナトリウム、がん組織内で過酸化水素の発生を高める高濃度ビタミンC点滴療法などと併用すると、さらに抗腫瘍効果を高めることができると考えられます。
(アルテスネイトの抗がん作用の詳細はこちらへ)
このように、伝統薬から様々な病気の治療に有効な薬が開発されています。「漢方薬は効かない」という先入観を持っている医者も多いのですが、数千年に渡って伝えられている伝統薬は「効果があるから生き残っている」という点と「伝統薬や民間薬から多くの医薬品が開発されている」という点を理解する必要があると思います。
| « 250)食品や生... | 252)なぜ無駄... » |



