Today, the U.S. Food and Drug Administration issued an emergency use authorization for the investigational antiviral drug remdesivir for the treatment of suspected or laboratory-confirmed COVID-19 in adults and children hospitalized with severe disease. While there is limited information known about the safety and effectiveness of using remdesivir to treat people in the hospital with COVID-19, the investigational drug was shown in a clinical trial to shorten the time to recovery in some patients.
“FDA’s emergency authorization of remdesivir, two days after the National Institutes of Health’s clinical trial showed promising results, is a significant step forward in battling COVID-19 and another example of the Trump Administration moving as quickly as possible to use science to save lives,” said HHS Secretary Alex Azar. “NIH, FDA, and scientists across America and around the world have worked tirelessly with patients to get us this new potential treatment for COVID-19. The seamless cooperation between government and private industry under the President’s all-of-America approach to COVID-19 is getting treatment options to patients in record time.”
The emergency use authorization allows for remdesivir to be distributed in the U.S. and administered intravenously by health care providers, as appropriate, to treat suspected or laboratory-confirmed COVID-19 in adults and children hospitalized with severe disease. Severe disease is defined as patients with low blood oxygen levels or needing oxygen therapy or more intensive breathing support such as a mechanical ventilator.
“From day one, the FDA has been committed to expediting the development and availability of potential COVID-19 treatments. Today’s action is an important step in our efforts to collaborate with innovators and researchers to provide sick patients timely access to new therapies where appropriate, while at the same time supporting research to further evaluate whether they are safe and effective,” said FDA Commissioner Stephen M. Hahn, M.D. “There’s tremendous interest among all parties to identify and arm ourselves with medicines to combat COVID-19, and through our Coronavirus Treatment Acceleration Program, the FDA is working around-the-clock and using every tool at our disposal to speed these efforts.”
Based on evaluation of the emergency use authorization criteria and the scientific evidence available, it was determined that it is reasonable to believe that remdesivir may be effective in treating COVID-19, and that, given there are no adequate, approved, or available alternative treatments, the known and potential benefits to treat this serious or life-threatening virus currently outweigh the known and potential risks of the drug’s use.
The EUA also requires that fact sheets that provide important information about using remdesivir in treating COVID-19 be made available to health care providers and patients, including dosing instructions, potential side effects and drug interactions. Possible side effects of remdesivir include: increased levels of liver enzymes, which may be a sign of inflammation or damage to cells in the liver; and infusion-related reactions, which may include low blood pressure, nausea, vomiting, sweating, and shivering.
Following the declaration by the Secretary of HHS that circumstances exist justifying the emergency use of unapproved products, the FDA may issue an emergency use authorization to allow unapproved medical products or unapproved uses of approved medical products to be used in an emergency to diagnose, treat, or prevent serious or life-threatening diseases or conditions caused by chemical, biological, radiological and nuclear threats when there are no adequate, approved, and available alternatives.
The issuance of an EUA is different than FDA approval. In determining whether to issue an EUA, the FDA evaluates the available evidence and carefully balances any known or potential risks of any unproven products with any known or potential benefits of making them available during the emergency.
The EUA was issued to Gilead Sciences Inc. The FDA previously allowed for study of the investigational drug under clinical trials, as well as expanded access use for individual patients and through a multi-patient expanded access program coordinated by Gilead.
The EUA will be effective until the declaration that circumstances exist justifying the authorization of the emergency use of drugs and biologics for prevention and treatment of COVID-19 is terminated and may be revised or revoked if it is determined the EUA no longer meets the statutory criteria for issuance.
The FDA, an agency within the U.S. Department of Health and Human Services, protects the public health by assuring the safety, effectiveness, and security of human and veterinary drugs, vaccines and other biological products for human use, and medical devices. The agency also is responsible for the safety and security of our nation’s food supply, cosmetics, dietary supplements, products that give off electronic radiation, and for regulating tobacco products.
https://www.fda.gov/news-events/press-announcements/coronavirus-covid-19-update-fda-issues-emergency-use-authorization-potential-covid-19-treatment

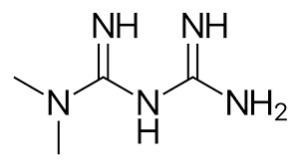
remdesivir
レムデシビルで入院期間が短縮
米国食品医薬品局(FDA)は5月1日、レムデシビルをCOVID-19(新型コロナウイルス感染症)で入院治療が必要な成人、および子供の患者に対し使用できるよう、緊急使用許可を発表した。(注1)レムデシビルは米バイオ医薬品大手のギリアド・サイエンシズ社がエボラ出血熱治療用に開発した抗ウイルス作用のある治験薬。
以前に報告した通り、今年2月からCOVID-19治療への有効性と安全性を調べるランダム化二重盲検比較臨床試験が開始されていた。
米で新型コロナウイルス治療のランダム化試験はじまる
レムデシビルを使った臨床試験は、米国内の47カ所の医療機関および、日本の国立国際医療研究センターを含むアジアやヨーロッパにある21医療機関でも実施されている。1000人以上を登録しているこの大規模な臨床試験はまだ終了しておらず、最終的な結果はでていない。しかし試験実施機関からは独立した立場の委員会が参加患者400人の初期データを見て、明らかな効果を認めた。
具体的には、レムデシビルの投与を受けた患者では、プラセボ投与の患者と比べ入院期間が平均で15日間から11日間に短縮された。この臨床試験は重症のCOVID-19患者を対象にしている。多くは人工呼吸器をつけており体への負担が重く、4日間の短縮は、大きな改善と言える。
臨床試験で有意な恩恵が示される

Anthony Stephen Fauci
国立アレルギー感染症研究所(NIAID)のアンソニー・ファウチ所長は、この初期の結果について「この薬はウイルスをブロックすることが示された。明らかに有望であり、プラセボ投与を受けている患者にも、すぐにレムデシビルを使わせる倫理的義務がある」と述べている。
緊急使用許可は、あくまでも臨床試験の初期のデータをもとづいて判断されたもので、通常のFDA承認ではない。最終的に承認するには、引き続き臨床試験を行い、データを詳しく検討する必要がある。
レムデシビルは、血中酸素濃度が下がり、病院での酸素療法や人工呼吸器が必要な重症のCOVID-19患者に点滴で投与される。副作用には、肝臓の炎症を示す肝酵素の上昇や血圧低下、悪心、吐き気、悪寒や発汗などあるという。
レムデシビルの臨床試験を2月に始めたネブラスカ大学医療センターのAndre Kalil医師は、レムデシビルの投与で回復が早まっただけでなく、「COVID-19の死亡率が4%下がった。回復時間の短縮と生存の改善を考えれば、非常に有望な薬だ」と述べている。また次の段階では、レムデシビルと抗炎症薬との併用による臨床試験に進むという。(注2)
臨床試験でも迅速に判断できることも
トランプ大統領は、「時間のかかる臨床試験など待っていられない」として、抗マラリア薬を適応外使用でCOVID-19の治療に使うよう推奨する発言をしていたが、FDAはその後、心拍の異常など深刻な副作用が報告されているとして、臨床試験または医師が経過観察できる病院でのみ使うよう警告した経緯がある。(注3)
新型コロナウイルス感染症には、有効性が確認されFDAが正式承認した治療薬がない。FDAは「コロナウイルス治療迅速プログラム」を設定し、できる限り早く、新たな治療薬の有効性と安全性を判断できるよう取り組んでいる。4月19日時点では、72の治験薬について臨床試験を行っており、さらに211の治験薬が臨床試験を開始する計画を持っている。(注4)
参考リンク
注1 レムデシビルの緊急使用許可に関するFDA発表(英文リンク)
注2 レムデシビルに関するネブラスカ・オマハのテレビ局KETVの報道(英語)
注3 FDAのヒドロキシクロロキンの使用に関する警告(英語)
注4 FDAのコロナウイルス治療迅速プログラムについて (英語)
https://news.yahoo.co.jp/byline/katasekei/20200502-00176443/
片瀬ケイ 米国がんサバイバー通信
https://news.yahoo.co.jp/byline/katasekei/
東京生まれ。日本での記者職を経て、1995年より米国在住。米国の政治社会、医療事情などを日本のメディアに寄稿している。2008年、43歳で卵巣がんの診断を受け、米国での手術、化学療法を経てがんサバイバーに。のちの遺伝子検査で、大腸がんや婦人科がん等の発症リスクが高くなるリンチ症候群だったことが判明した。海外のがん情報をインターネットで日本人向けに紹介する「海外がん医療情報リファレンス」にも翻訳協力している。また共訳書に『RPMで自閉症を理解する』がある。なお、私は医療従事者ではありません。病気の診断、治療については必ず医師にご相談下さい。

Kei KATASE
วันนี้สำนักงานคณะกรรมการอาหารและยาแห่งสหรัฐอเมริกาได้ออกใบอนุญาตใช้ยาฉุกเฉินสำหรับผู้ติดยาเสพติดยาต้านไวรัสเพื่อการรักษาผู้ป่วย COVID-19 ที่ได้รับการยืนยันหรือสงสัยในห้องปฏิบัติการในผู้ใหญ่และเด็กที่เข้ารับการรักษาในโรงพยาบาลด้วยโรครุนแรง ในขณะที่มีข้อมูลที่ จำกัด เกี่ยวกับความปลอดภัยและประสิทธิผลของการใช้ยา remdesivir ในการรักษาผู้ป่วยในโรงพยาบาลด้วย COVID-19 แต่ยาที่ใช้ในการวิจัยแสดงให้เห็นในการทดลองทางคลินิกเพื่อลดระยะเวลาในการฟื้นตัวในผู้ป่วยบางราย
“ การอนุมัติ remdesivir ขององค์การอาหารและยาฉุกเฉินสองวันหลังจากการทดลองทางคลินิกของสถาบันสุขภาพแห่งชาติแสดงให้เห็นถึงผลลัพธ์ที่มีแนวโน้มเป็นก้าวสำคัญในการต่อสู้กับ COVID-19 และอีกตัวอย่างหนึ่งของการบริหารทรัมป์เคลื่อนไหวเร็วที่สุดเท่าที่เป็นไปได้ อเล็กซ์ Azar เลขานุการ HHS กล่าว “ NIH, FDA และนักวิทยาศาสตร์ทั่วอเมริกาและทั่วโลกทำงานร่วมกับผู้ป่วยอย่างไม่รู้จักเหน็ดเหนื่อยเพื่อรับการรักษาที่มีศักยภาพใหม่สำหรับ COVID-19 ความร่วมมือที่ราบรื่นระหว่างภาครัฐและภาคเอกชนภายใต้แนวทางทั้งหมดของประธานาธิบดีแห่งอเมริกาในการใช้ COVID-19 กำลังได้รับทางเลือกในการรักษาผู้ป่วยในเวลาที่บันทึก”
การอนุญาตการใช้เหตุฉุกเฉินอนุญาตให้แจกจ่ายยาในสหรัฐอเมริกาและให้ยาทางหลอดเลือดดำโดยผู้ให้บริการด้านสุขภาพตามความเหมาะสมในการรักษาผู้ป่วย COVID-19 ที่ได้รับการยืนยันหรือสงสัยในห้องปฏิบัติการในผู้ใหญ่และเด็กที่รักษาด้วยโรครุนแรง โรคที่รุนแรงหมายถึงผู้ป่วยที่มีระดับออกซิเจนในเลือดต่ำหรือจำเป็นต้องได้รับการบำบัดด้วยออกซิเจนหรือมีการหายใจที่เข้มข้นเช่นเครื่องช่วยหายใจเชิงกล
“ ตั้งแต่วันแรกองค์การอาหารและยามุ่งมั่นที่จะเร่งการพัฒนาและความพร้อมของการรักษา COVID-19 ที่มีศักยภาพ การกระทำของวันนี้เป็นขั้นตอนสำคัญในความพยายามของเราในการร่วมมือกับนักประดิษฐ์และนักวิจัยเพื่อให้ผู้ป่วยที่ป่วยสามารถเข้าถึงการรักษาใหม่ที่เหมาะสมในขณะที่ในขณะเดียวกันก็สนับสนุนการวิจัยเพื่อประเมินเพิ่มเติมว่าปลอดภัยและมีประสิทธิภาพหรือไม่ . Hahn, MD“ มีความสนใจอย่างมากในทุกฝ่ายในการระบุและใช้อาวุธของเราในการต่อสู้กับ COVID-19 และผ่านโปรแกรมเร่งความเร็วการรักษา Coronavirus ของเรา FDA ทำงานตลอดเวลาและใช้เครื่องมือทุกอย่างเพื่อกำจัด ความพยายามเหล่านี้”
จากการประเมินเกณฑ์การอนุมัติการใช้งานฉุกเฉินและหลักฐานทางวิทยาศาสตร์ที่มีอยู่ก็พิจารณาแล้วว่ามีเหตุผลที่เชื่อได้ว่า remdesivir อาจมีประสิทธิภาพในการรักษา COVID-19 และการรักษาทางเลือกที่ไม่เพียงพอได้รับการอนุมัติหรือใช้ได้ ผลประโยชน์ที่เป็นที่รู้จักและมีศักยภาพในการรักษาไวรัสที่ร้ายแรงหรืออันตรายถึงแก่ชีวิตในขณะนี้มีมากกว่าความเสี่ยงที่เป็นที่รู้จักและมีศักยภาพของการใช้ยา
EUA ยังต้องการเอกสารข้อเท็จจริงที่ให้ข้อมูลสำคัญเกี่ยวกับการใช้ remdesivir ในการรักษา COVID-19 เพื่อให้บริการแก่ผู้ให้บริการด้านสุขภาพและผู้ป่วยรวมถึงคำแนะนำในการใช้ยาผลข้างเคียงที่อาจเกิดขึ้นและปฏิกิริยาระหว่างยา ผลข้างเคียงที่เป็นไปได้ของ remdesivir รวมถึง: เพิ่มระดับของเอนไซม์ในตับซึ่งอาจเป็นสัญญาณของการอักเสบหรือทำลายเซลล์ในตับ; และปฏิกิริยาที่เกี่ยวข้องกับการแช่ซึ่งอาจรวมถึงความดันโลหิตต่ำ, คลื่นไส้, อาเจียน, เหงื่อออกและตัวสั่น
หลังจากที่เลขาธิการ HHS ประกาศว่าสถานการณ์นั้นมีเหตุผลในการใช้ผลิตภัณฑ์ที่ไม่ได้รับการอนุมัติฉุกเฉิน FDA อาจออกหนังสืออนุญาตการใช้ฉุกเฉินเพื่ออนุญาตผลิตภัณฑ์ทางการแพทย์ที่ไม่ผ่านการอนุมัติหรือการใช้ผลิตภัณฑ์ทางการแพทย์ที่ไม่ผ่านการอนุมัติเพื่อใช้ในการวินิจฉัยวินิจฉัย หรือป้องกันโรคหรือเงื่อนไขที่ร้ายแรงหรือเป็นอันตรายถึงชีวิตที่เกิดจากภัยคุกคามทางเคมีชีวภาพรังสีและนิวเคลียร์เมื่อไม่มีทางเลือกที่เพียงพอได้รับการอนุมัติและพร้อมใช้งาน
การออก EUA นั้นแตกต่างจากการอนุมัติของ FDA ในการพิจารณาว่าจะออก EUA หรือไม่ FDA จะประเมินหลักฐานที่มีอยู่และพิจารณาความเสี่ยงที่อาจเกิดขึ้นได้ของผลิตภัณฑ์ที่ไม่ผ่านการพิสูจน์ด้วยความระมัดระวังหรือผลประโยชน์ใด ๆ
EUA ออกให้กับ Gilead Sciences Inc. ก่อนหน้านี้ FDA อนุญาตให้ศึกษายาที่ใช้ในการทดลองภายใต้การทดลองทางคลินิกรวมถึงการขยายการเข้าถึงการเข้าถึงสำหรับผู้ป่วยแต่ละรายและผ่านโปรแกรมการเข้าถึงแบบขยายหลายผู้ป่วยซึ่งประสานงานโดย Gilead
EUA จะมีผลจนกว่าจะมีการประกาศว่าสถานการณ์มีความชอบธรรมในการอนุญาตให้ใช้ยาและชีววิทยาในกรณีฉุกเฉินเพื่อป้องกันและรักษา COVID-19 จะถูกยกเลิกและอาจถูกแก้ไขหรือเพิกถอนหากมีการพิจารณาว่า EUA ไม่ตรงตามเกณฑ์ทางกฎหมายอีกต่อไป สำหรับการออก
FDA ซึ่งเป็นหน่วยงานภายในกระทรวงสาธารณสุขและบริการมนุษย์ของสหรัฐอเมริกาปกป้องคุ้มครองสาธารณสุขด้วยการรับรองความปลอดภัยประสิทธิผลและความปลอดภัยของยามนุษย์และสัตวแพทย์วัคซีนและผลิตภัณฑ์ชีวภาพอื่น ๆ สำหรับการใช้งานของมนุษย์และอุปกรณ์ทางการแพทย์ หน่วยงานยังรับผิดชอบด้านความปลอดภัยและความมั่นคงของแหล่งอาหารเครื่องสำอางในประเทศของเรา