15.構造の複雑な炭化水素
――――――――――――――――――
既述のページへのリンク: ①炭素という名称の起源 ②炭素の認識:木炭は何故炭素なのか ③元素としての炭素の性質 ④炭素の誕生 ⑤宇宙の炭素 ⑥原始太陽系の炭素 ⑦炭素と有機物 ⑧炭素原子とメタン分子 ⑨炭化水素分子内での炭素の結合 ➉分子内での炭素と酸素の共有結合 ⑪窒素の形成と水素と炭素と酸素 ⑫窒素を含んだ有機化合物と無機化合物 ⑬星(恒星)と炭素 ⑭炭化水素分子内での炭素―炭素結合と電子 ⑮複雑な構造の炭化水素、⑯複素環式化合物、⑰炭素化合物の多様性、⑱炭素原子と星間分子
――――――――――――――――――
炭素はビッグバン後の第一世代の星形成に際してトリプルアルファ反応によって合成され、宇宙における星形成時の元素合成の初期から存在した。従って炭素と水素で形成される炭化水素分子も宇宙の星形成の早い段階から存在した可能性がある。炭素原子は単結合、二重結合、三重結合によって幾つでもお互いに結合することが可能なため、小さな炭化水素分子でも様々な構造のものが存在する。結果として、多種多様な炭化水素分子が星形成の初期から形成された可能性はある。
分子は原子と原子が電子を介して結合することによって形成される。炭素と水素が結合して形成される炭化水素は有機化合物の基本骨格を形成する分子である。基本的な炭化水素の骨格は一本の鎖状に炭素と炭素が結合した分子である。この炭素鎖が枝分かれした分子も鎖状炭化水素であり、様々な構造のものが存在するが、直鎖炭化水素の誘導体として命名する。命名に際しては、分子内の最も長い直鎖部分を母体(主鎖)とする。母体となる炭化水素の名称の前に、枝となる炭素鎖(側鎖)の基名とその数を接頭語として加える。側鎖の結合する位置は、主鎖の端から順番に付けられた炭素の番号で示すが、主鎖の番号を付けるには側鎖の位置が最小となる側から始める。
2個以上の側鎖がある場合には、二通りの付け方が可能となる場合が多い。その場合で、最初の側鎖の位置番号が同じ場合には、それに続く側鎖の位置番号の最初の数が小さくなる方向を選ぶ。異なった複数の側鎖が存在する場合には、基名のアルファベット順にならべる。枝のある不飽和炭化水素は、二重結合および三重結合の最多数を含む炭化水素鎖を主鎖とし、その誘導体として命名する。最多数の不飽和結合を含む鎖が幾通りもあるときには、その鎖の中で最多数の炭素原子を持つ鎖、それでも同じなら最多数の二重結合を持つ鎖を優先する。以下にその例を示す。

炭素鎖の両端が結ばれると脂環式化合物と呼ばれる環状構造を持つ分子が形成される。複数の環が2個またはそれ以上の原子を共有している脂環炭化水素は「橋かけ環炭化水素」と呼ばれる。環が二つ(二環系炭化水素)の場合、環を形成するすべての炭素数に相当する直鎖炭化水素名に接頭語「ビシクロ」をつけ、2個の橋頭炭素原子を結ぶ三つの橋のそれぞれに含まれる炭素原子の数を大きいものから順に括弧に入れて示す。位置番号は橋頭の一つから始め、最長の橋を通って第二の橋頭に至り、そこから2番目に長い橋を通って第一の橋頭に戻り、最後に最短の橋を通って第二の橋頭に戻って終わる。不飽和の橋かけ環炭化水素は単環炭化水素と同様に命名し、不飽和結合が最小の位置番号を持つようにする。三環系炭化水素は接頭語として「トリシクロ」を用いる。以下に例を示すが、小さい分子でもかなり複雑な表現となる。化合物名が2行にわたって書かれている場合は、下行は慣用名である。
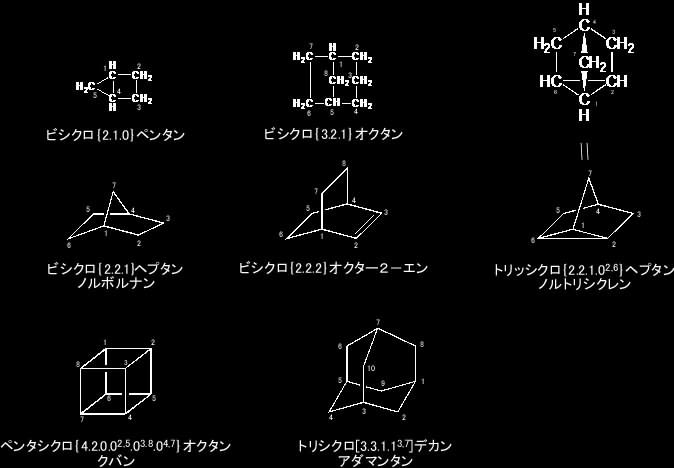
括弧内の橋かけ炭素数の肩に付けられた数字は、橋頭位置以外で結ばれている炭素の位置を表している。ノルトリシクレンの場合トリシクロの接頭語で三つの環で構成されていることを示し、7個の炭素原子で形成された飽和炭化水素であるのでヘプタンとなる。角括弧内の[2.2.1.02,6] は一番目の橋頭炭素から2個の炭素を介した橋を通って二番目の橋頭炭素に到達し、そこから2個の炭素を通して一番目の橋頭炭素に戻り、さらに1個の炭素を介して二番目の橋頭炭素に達し、それ以外に2位と6位の炭素が直接結ばれていることを意味している。アダマンタンも同様に命名され、トリシクロ[3.3.1.13,7]デカンとなる。この場合、分子全体が10個の炭素で構成されており、一番目の橋頭炭素(炭素1)から3個の炭素による一番目の橋を通って二番目の橋頭炭素(炭素5)に到達し、そこから3個の炭素を通って一番目の橋頭炭素(炭素1)に戻り、さらに1個の炭素を介して二番目の橋頭炭素(炭素5)に達する。そして炭素3と炭素7が1個の炭素を介して結ばれていることを意味している。ノルボルナンとノルトリシクレンは慣用名であるが、クバン(キュバン)とアダマンタンは、そのままIUPACの正式名称として使われる。通常の構造式では特にその存在を強調したい場合以外は炭素と水素の元素記号は省略され、直線の角や末端には炭素が存在し、水素はその炭素の結合状態に応じた数だけ結合していることが前提とされる。アダマンタンの構造を出発点としてsp3炭素の結合が隙間なく実質的に無限に三次元的に広がったものがダイヤモンドである。
橋かけ環炭化水素は二つの脂環式炭化水素が2個以上の炭素を共有しているが、1個しか共有していない場合はスピロ炭化水素と呼ばれる。スピロ炭化水素は、橋かけ炭化水素と同様に全炭素原子数と同じ数の炭素を持つ直鎖炭化水素名に「スピロ」の接頭語を付けて命名する。環を結合している炭素(スピロ原子という)と連結している各環の炭素原子の数を小さい物から順に括弧に入れて示す。この示し方は、橋かけ環炭化水素の場合と逆になる。これに従って位置番号の付け方も逆で、小さい環を優先させ、スピロ原子の次の原子から始め、スピロ原子を通り第二の環を回って終わる。不飽和結合の表示方法は橋かけ環炭化水素と同じである。以下に例疎示す。

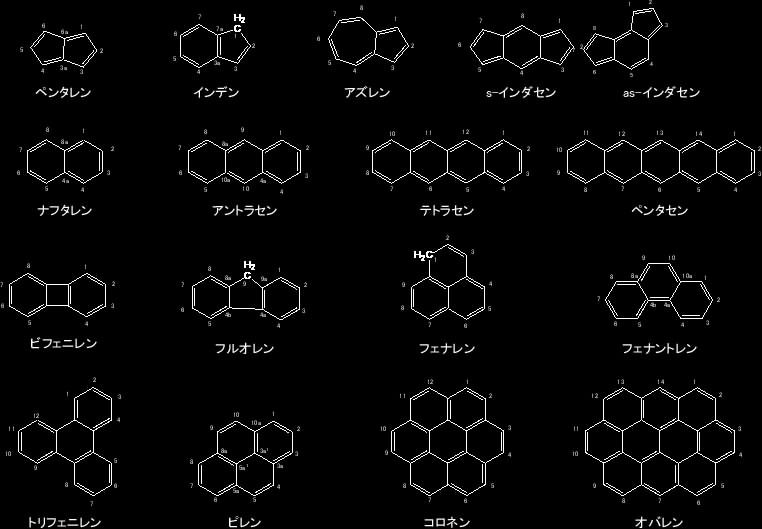
同一分子内に二重結合と単結合が交互に存在すると共役系が形成され、構造式では単結合で表されている結合にもπ電子が拡散し、共役系全体にπ電子の非局在化が生じる。環状の分子の骨格部分にπ電子が非局在化し、単なる共役系から推定される性質と大幅に異なる性質を示すようになった分子が芳香族化合物である。ベンゼンはその基本的化合物で、π電子が各炭素原子に完全に均等に分布した分子である。複数の炭化水素の環が縮合した構造を持っている化合物を縮合多環炭化水素と言う。単結合だけで表すと同じ骨格に見える縮合多環化合物の中では、最多数の二重結合をもつ化合物に「エン」の接尾語を付け、命名の基礎化合物(基礎成分)とする。下表に示された35種の化合物が基礎成分として分子固有の名称を使うことがIUPACの規則で決められている。

これらの化合物は芳香族性を有する。その一部を以下に示が、二重結合に関しては、共鳴極限構造の一つだけを示すのが通常である。コロネンやオバレンの構造が二次元的に実質的に無限大に広がったものがグラフェンであり、そのシートが無数に重なったものがグラファイトである。
上表の35種の縮合多環炭化水素以外の縮合多環炭化水素の命名法はIUPACの規則で定められている。例を以下に示すが、これらの。全ての縮合多環炭化水素は、上表の35種の化合物を基礎成分として、これに他の成分を接頭語として付けて命名する。ただし、基礎成分にはできるだけ多くの環を含むものを選ぶ。環の数が同じ基礎成分の場合は上表の化合物番号の大きいものを優先する。付け加える成分はできるだけ簡単なものとする。付け加える成分を表す接頭語は、成分炭化水素名の接尾語の「エン(ene)」を「エノ(eno)」に変えて作るが、ベンゾ、ナフト、アントラなどは省略形の接頭語を使う。下図の構造を持つ化合物はフェナントレンが基礎成分であるが二通りの取り方が可能で、片方の取り方では付加成分はナフタレンとなり、もう片方では2個のベンゼンとなる。ベンゼンの方が構造的に簡単なのでこちらを付加成分(ジベンゾ)とする。

異性体を区別するために、基礎成分の周囲の辺にアルファベットの記号をつけ、縮合の起こっている辺を括弧に入れて示す。アルファベットの記号は基礎成分の1,2の辺をaとし、基礎成分の番号に従って周囲を回る。ただし、位置番号のない炭素を含む辺にもアルファベットの記号をつける。付け加える成分の構造の中で縮合位置を示す必要がある場合には、付加成分のほうの位置番号を使って、アルファベット記号の前につける。この場合付加成分の番号を並べる順序はアルファベット記号を付ける方向と一致させる。言葉では分かりにくいので、下図に例を示す。

縮合多環系の炭素に位置番号をつけるには次の規則に従う。まず、最多数の環が水平に並び、他の環の最多数が上右四半分にくるようにむける。このように配置した構造式で、最も上で最も右側にある環の中で縮合に関与していない炭素を1とし、時計回りに番号をつける。2個以上の環に共通な炭素には番号を付けない。番号を付ける必要がある場合には、直前の炭素番号にa、b、cなどを添えて表す。以下に例を示す。点線は基本となる最多数の環の中央に上下左右にひかれており、付け加える成分は最多数が右上四半分くるようにしてある。この番号付けの規則は、アントラセンとフェナントレン以外のすべての縮合環系に適用する。

アントラセンとフェナントレンの位置番号は以下の通りである。この二つの例外は、IUPAC2013の勧告が出る前に、従来の炭素番号が非常に多くの分野で使用されているため混乱を避けるために設けられたものと考えられる。

一つの名称が、最多数の非集積二重結合を持つ互いに異性体となる2種以上の縮合環系に等しく適用され、かつ構造中にある1個またはそれ以上の水素原子の位置を示すことによって異性体の区別ができる場合には、このような炭化水素のおのおのについて、その位置番号とイタリック大文字Hを用いて名称を作る。このHを指示水素と呼ぶ。以下にその例を示す。インデンもフルオレンも基礎成分として認められており、特に指示水素を示さない。

星間分子として報告されている縮合多環炭化水素にナフタレンがある。
















※コメント投稿者のブログIDはブログ作成者のみに通知されます