既述のページへのリンク: ①炭素という名称の起源 ②炭素の認識:木炭は何故炭素なのか ③元素としての炭素の性質 ④炭素の誕生 ⑤宇宙の炭素 ⑥原始太陽系の炭素 ⑦炭素と有機物 ⑧炭素原子とメタン分子 ⑨炭化水素分子内での炭素の結合 ➉分子内での炭素と酸素の共有結合 ⑪窒素の形成と水素と炭素と酸素 ⑫窒素を含んだ有機化合物と無機化合物 ⑬星(恒星)と炭素 ⑭炭化水素分子内での炭素―炭素結合と電子 ⑮複雑な構造の炭化水素、⑯複素環式化合物、⑰炭素化合物の多様性、⑱炭素原子と星間分子
------------------ーーーーーーーーーーー
炭素という名称は木炭に由来し、物体としての炭(スミ)の本質を構成する物質を意味する。一方、地上の物体の最小基本単位は原子である。従って炭素という元素の最小単位は炭素という名称の原子ということになる。異なった性質の元素を構成する原子は、それぞれ実体が異なっている。ところが、すべての原子は、共通したより小さい要素によって組立てられている。それらの要素は、陽子(プロトン)や中性子(ニュートロン)や電子(エレクトロン)と呼ばれ、それぞれp、n、e-の記号であらわされる。これらの要素のそれぞれは、すべての元素において共通している。異なる元素の間では、1つの原子に含まれるこれらの構成要素の数が異なっているのである。
元素としての化学的性質は原子を構成する陽子の数が基本となっている。中性子や電子の数も物質としての物理的性質に大きく影響するが、陽子の数が同じ原子は、同じ名前の元素である。原子の空間的中心部分を陽子と中性子が占め原子核と呼ばれる。電子は、原子核の空間に対して、相対的にはるか離れた位置に存在し、その重さ(質量)は陽子や中性子と比較するとはるかに軽い(小さい)。
炭素の原子を構成する陽子の数は6個の陽子である。ちなみに、水素、ヘリウム、窒素、酸素の原子を構成している陽子の数は、それぞれ、1個、2個、7個、8個である。これらの陽子の数は原子番号と呼ばれるものに相当し、元素の周期表にはこの番号順に配列されている。実在する全ての元素に固有の名前とその名前にちなんだ記号(元素記号)が付けられているが、その名の由来はまちまちである。
では、ほぼ100パーセント炭素によって構成されている炭(すみ)の場合、個々の炭素原子が1個ずつばらばらの状態で寄せ集められているのであろうか。否である。地球上の元素で1個の独立した原子として安定に存在するのは、希ガスと呼ばれるグループ(周期表では第18族元素として纏められている)に属する6種類の元素(ヘリウ:He、ネオン:Ne、アルゴン:Ar、クリプトン:Kr、キセノン:Xe、ラドン:Rn)に限られている。その他の元素が単一の原子として独立して存在するのは、非常に特殊な条件下においてである。地球における通常の条件下では、希ガス以外の元素は何らかの結合によって自分と同じ種類の元素や自分と異なった種類の元素と結ばれて、より安定な物質として存在している。それぞれの元素の原子と原子を結び付けているのは電子である。本来、それぞれの元素の原子は、元素に固有の電子をもっている。その数は原子の持つ陽子の数と同じで、電気的に陽性の陽子と陰性の電子が釣り合って、1個の原子として電気的に中性を保っている。中性子はその名の通り電気的に中性で、原子の重さには大きく影響するが、電気的性質には影響しない。
一般に原子は希ガスと同じ数の電子を持った状態の方がエネルギー的により安定な状態を作れる。そのため、自分以外の原子と電子を融通しあって、見かけ上希ガスと同じ数の電子を持って安定化しようとする。このことによって、原子間の結合が形成されるが、その結合は、電子の融通の仕方によって、共有結合、イオン結合、金属結合に分けられる。
例えば、ナトリウム(Na)の原子と塩素(Cl)の原子によって形成されている食塩(塩化ナトリウム)の場合は、それぞれの原子が希ガス元素と同じ数の電子を持とうとするため、それぞれの原子の陽子の数と電子の数が違ってくる。具体的には、ナトリウム(Na)は電子を1個放出して、希ガス元素のネオン(Ne)と同じ数の電子を持とうとし、塩素(Cl)は電子1個を受け入れて希ガス元素のアルゴン(Ar)と同じ数の電子を持とうとする。その結果、ナトリウム(Na)は陽子の数より電子が一つ少ないため電気的に陽性のイオン(Na+)となり、塩素は(Cl)は電子が陽子の数より一つ多いため電気的に陰性のイオン(Cl-)となって相互に引き合って、電気的に中性な集団を形成し、安定な食塩という物質となっている。このように電子の授受によって原子と原子を結び付ける結合をイオン結合と呼ぶ。
金属結合と呼ばれる物質の安定化は、電子を放出して希ガス元素と同じ電子を持つと同時に電気的に陽性となった原子が格子状に並び、その間を放出された電子がどの原子に属するということなく自由に動き回ることによって原子どうしを結び付けるものである。金属としての鉄や銅が典型的な物質で、電気を伝える性質も、結合を形成している電子が自由に動くことに由来している。
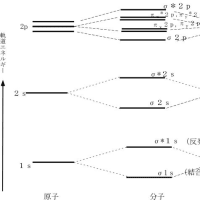
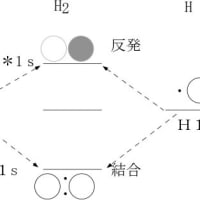
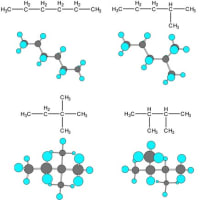
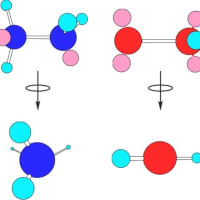
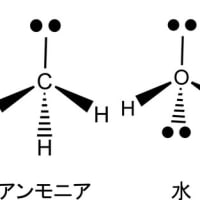
では、炭素はどのような結合によって物質として安定化しているのであろうか?炭素は、6個の陽子を持っていて、希ガス元素のヘリウム(He)と同じ電子数(2個)になろうとすると4個の電子を放出する必要があり、ネオン(Ne)と同じ電子数(10個)になろうとすると4個の電子を持ってくる必要がある。このような場合、完全に結合相手に電子を与えたり、結合相手から電子を奪ったりするよりは、相互に互角の立場で持ち合う方がエネルギー的にはるかに実現しやすい。この結合の仕方を、相手の原子と電子を共有して安定化するので、共有結合と言う。炭素の原子は、炭素原子どうしで容易に安定な共有結合を作ることができる。このことが、炭素が他の元素と際立った違いを見せる本質的な要因であり、生命現象をつかさどる有機化合物の形成も、炭素が持つこの性質があって、はじめて実現されるのである。
木炭を形作る炭(すみ)は、多くの炭素原子が共有結合によって結ばれた物質の集合体である。炭素原子どうしを結ぶ共有結合の様式には、σ(シグマ)結合と呼ばれる結合や、π(パイ)結合と呼ばれる結合など異なった種類のものがある。炭を構成している炭素の間には、異なった共有結合がランダムに混在している。炭素が実質的に特定の結合で秩序だって結ばれてできた物質の典型的なものに、ダイヤモンド(σ結合のみ)やグラファイト(σ結合とπ結合)が存在する。
















※コメント投稿者のブログIDはブログ作成者のみに通知されます