既述のページへのリンク: ①炭素という名称の起源 ②炭素の認識:木炭は何故炭素なのか ③元素としての炭素の性質 ④炭素の誕生 ⑤宇宙の炭素 ⑥原始太陽系の炭素 ⑦炭素と有機物 ⑧炭素原子とメタン分子 ⑨炭化水素分子内での炭素の結合 ➉分子内での炭素と酸素の共有結合 ⑪窒素の形成と水素と炭素と酸素 ⑫窒素を含んだ有機化合物と無機化合物 ⑬星(恒星)と炭素 ⑭炭化水素分子内での炭素―炭素結合と電子 ⑮複雑な構造の炭化水素、⑯複素環式化合物、⑰炭素化合物の多様性、⑱炭素原子と星間分子
------------------ーーーーーーーーーーー
窒素は宇宙の元素形成の早い段階で作られた安定元素の一つである。宇宙の元素合成の初期反応として水素(1H)からヘリウム4(4He)が合成される経路は、陽子‐陽子連鎖反応と呼ばれるものである。同様に水素(1H)からヘリウム4(4He)が合成される経路にCNOサイクルがある。出発物質の水素と生成物の中のヘリウムだけをみると陽子‐陽子連鎖反応と同じであるあるが、CNOサイクルの開始には炭素原子の存在が必須であることが陽子‐陽子連鎖反応との決定的な差である。CNOサイクルの反応経路には水素(1H)と炭素12(12C)からヘリウム4(4He)と炭素12(12C)が作られる経路(この場合には炭素は触媒の役目をしている)の他に、反応の途中から分岐してさらに2個の水素(1H)が加わって、ヘリウム4(4He)と窒素14(14N)が形成されるルートがある。この反応では炭素12(12C)が窒素14(14N)に変換されており、このルートが宇宙の窒素原子の供給源と考えられている。水素が豊富にある宇宙空間に炭素が放出され、再度集合して星を形成し、その星の内部で窒素原子が合成されるケースは、宇宙における元素合成の初期にも多くあったと考えられる。したって、有機分子の大半を形成する、水素、炭素、酸素、窒素の四つの元素は、宇宙における物質形成の早い時点から揃っていたことになる。
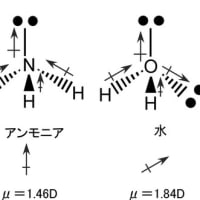
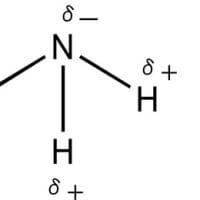
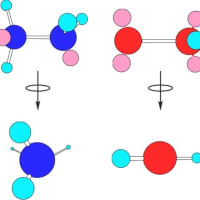
窒素14(14N)は原子核に陽子を7個、中性子を7個持っている。電子は、1s軌道に2個、2s軌道に2個、2p軌道に3個存在する。外殻電子は5個で、安定な8個にするには3個の電子を必要とする。従って共有結合では原子価は3となる。アンモニア分子を形成する場合には窒素原子はsp3混成軌道をを形成し、メタンと同様に正四面体の頂点に向かって電子が分布し、σ共有結合に関与する3個の電子の他に共有結合に関与しない2個の電子が1個の軌道に孤立電子対として存在する。窒素の原子価を全て水素との共有結合で満たすとアンモニア分子(NH3)が形成される。アンモニアの構造は以下のように表される。ただし、ピンクのボールは孤立電子対を表す。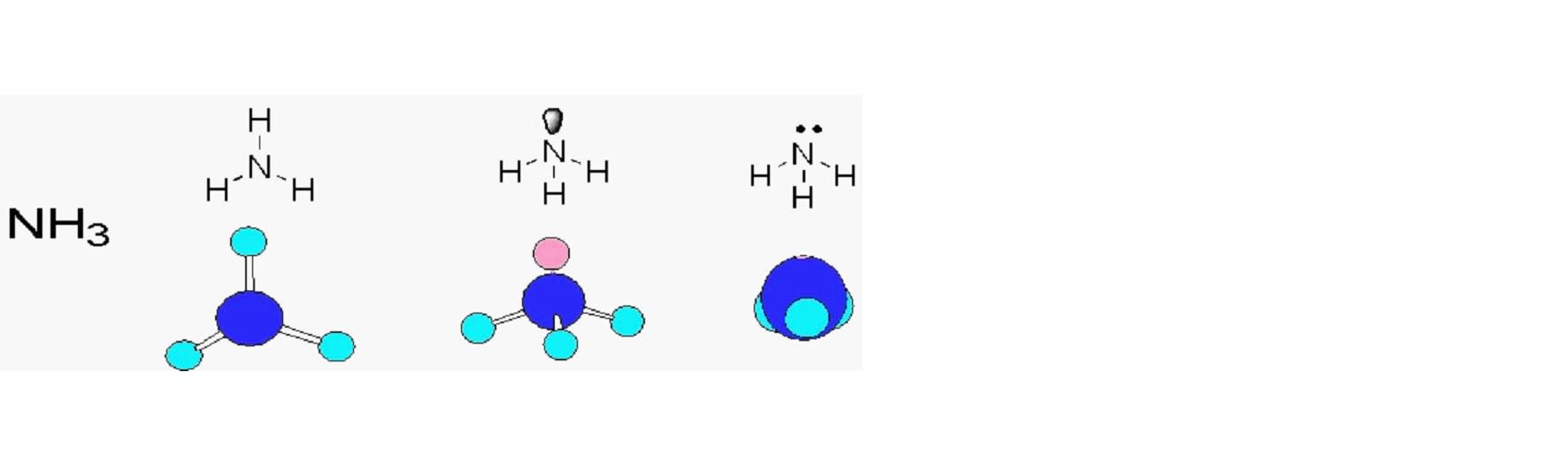
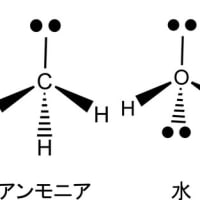
もし、水素が豊富に存在する適度に冷却された空間に窒素原子が放出されるとアンモニアが形成されることになる。宇宙における元素合成の過程で窒素よりも早い時点で形成蓄積される安定元素には、炭素と酸素があり、これらの元素も同様な条件でそれぞれメタン(CH4)と水(H2O)を形成する。このことは、宇宙における物質形成の早い時点から水(H2O)もメタン(CH4)もアンモニア(NH3)も存在し、それらの分子から様々な条件で誘導される多種多様な有機化合物が、宇宙のあちらこちらに存在する可能性がある。
窒素を含んだ有機化合物は、酸素を同時に含んだ化合物も含めると、一般的名称が与えられているものとして、アミン、イミン、ニトリル、イソシアン化物、ヒドラジン、アミド、ヒドラジド、シアン酸エステル、イソシアン酸エステル、イミド、アミジン、尿素、アミノ酸等がある。これらの化合物を命名する時の母体は窒素が結合している炭化水素でその炭化水素の水素が窒素の誘導体よって置換されたものと考える。アミノ酸は炭化水素の水素がカルボキシル基(COOH)に置換されてできるカルボン酸のアルキル鎖の水素がアミノ基(-NH2)で置換されたものの一般名称で、アミノ基の置換された位置を、カルボキシル基に近い方からα、β等のギリシャ文字で表す。それらの化学構造的な特徴を以下に示す。
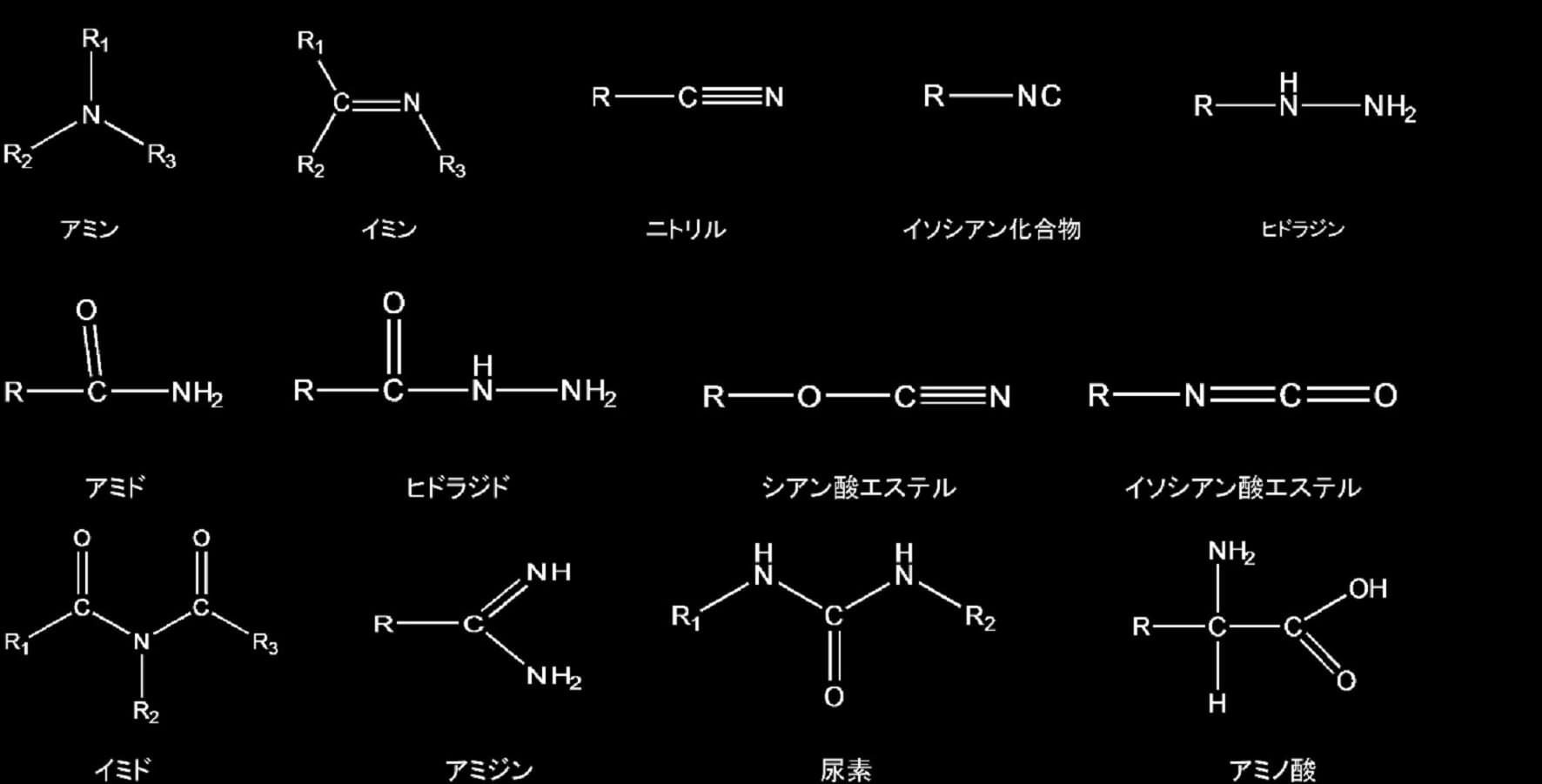
IUPACによる有機化合物命名法によると、窒素を含んだ特性基で接頭語としてのみ使われるものに、=N2(ジアゾ)、-N3(アジド)、-NC(イソシアノ)、―NCO(イソシアナト)、-NO(ニトロソ)、-NO2(ニトロ)がある。例えば、CH2N2(ジアゾメタン)、CH3NO2(ニトロメタン)等がある。―NH2(アミン)、=NH(イミン)、-NHNH2(ヒドラジン)の場合、それぞれが接頭語として使われる場合は、アミノ…、イミノ…、ヒドラジノ…と呼ばれ、接尾語として使われる場合は、…アミン、…イミン、…ヒドラジンと呼ばれる。アミドの場合には、酸素を特性基(-CONH2)に含めた場合、接頭語としてはカルバモイル…、接尾語としては…カルボキサミドという用語が用いられるが、アミドの炭素を母体化合物に含ませて(-(C)ONH2)命名する場合がある。この場合にはカルボン酸のカルボキシル基(-C(=O)OH)のOHがアミノ基(-NH2)に置換されたものみなし、酸の代わりにアミドという接尾語が使われる。例えばCH3(CH2)4CONH2の場合にはヘキサンアミドとなる。一つの分子にいろいろな特性基が存在する場合にどの特性基を接頭語とし、どの特性基を接尾辞とするかの規則も定められている。
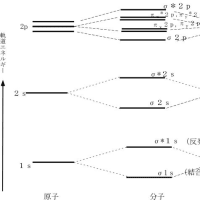
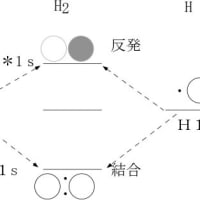
初期の宇宙で窒素原子ができた時には、安定元素として水素、ヘリウム、リチウム、炭素、窒素、酸素が作られている。これらの元素のうちヘリウム以外は地球上の通常の条件では、単独の原子として存在するよりは複数の原子で結合を作ることによってより安定化された分子として存在する。リチウムは金属的な性質が強く、LiHと表される化合物(水素化リチウム)もイオン結合(Li+H-)によるもので共有結合による分子とは異なる。ヘリウムは単独の原子で分子のように振る舞うので単原子分子と呼ばれる。前記の元素のうちリチウムとヘリウムを除いた元素(水素、炭素、窒素、酸素)は複数の原子が共有結合によって分子を形成した方が単独の原子の状態より安定になる。上記の元素のうち2個の同一種の元素で形成された分子は等核二原子分子と呼ばれ、地球でも水素分子(H2)、酸素分子(O2)、窒素分子(N2) は通常に存在する。2個の炭素でできた分子(C2)は二原子炭素と呼ばれるが、高温な状態などの特殊な条件下で存在する。地球で通常に存在する炭素を含んだ二原子分子としては一酸化炭素(CO)が存在する。このように異なった2個の元素で形成されている分子は異核二原子分子と呼ばれる。ここにあげた二原子分子は、全て無機化合物とされている。
炭素と窒素が結合してできる無機化合物にシアン化合物がある。有機化合物としてのニトリル( ![]() )が共有結合を介して分子を形成するのに対して、無機化合物のシアン化合物は、CN部分がシアン陰イオン(
)が共有結合を介して分子を形成するのに対して、無機化合物のシアン化合物は、CN部分がシアン陰イオン( ![]() )として存在し、陽イオンとイオン結合を介して化合物を形成する点が有機化合物のニトリルと異なっている。身近な例として有機化合物としてアセトニトリル(CH3―CN)、無機化物としてシアン化カリウム(青酸カリ:K+CN-)があげられる。
)として存在し、陽イオンとイオン結合を介して化合物を形成する点が有機化合物のニトリルと異なっている。身近な例として有機化合物としてアセトニトリル(CH3―CN)、無機化物としてシアン化カリウム(青酸カリ:K+CN-)があげられる。
炭素が水素と窒素と酸素とに結合して形成する無機化合物にシアン酸(HCON)、イソシアン酸(HCNO)、雷酸(HONC)があり、それらは以下の構造式で表される。

シアン酸とイソシアン酸は通常平衡状態にあり、液体状態やプロトン溶媒中のように水素結合が形成されやすい環境ではシアン酸が優位であるが、気体状態や非プロトン溶媒中ではイソシアン酸が優位となる。雷酸は上図のように共鳴構造で表される状態にある。
窒素と酸素で形成される無機化合物には、NO(一酸化窒素)、N2O(酸化二窒素)、NO2(二酸化窒素)、N2O3(三酸化二窒素)、N2O4(四酸化二窒素)、N2O5(五酸化二窒素)等のノックス(化学式のNOxに由来)と呼ばれる一群の化合物がある。五酸化二窒素は水に溶かすとHNO3(硝酸)を生ずる。硝酸は窒素のオキソ酸と一般名で呼ばれる化合物で、HNO2(亜硝酸)もこれに属する。
窒素原子を含んだ星間分子としては以下のものが報告されている。
CN、HN、N2、NO、NS、SiN、AlNC、HCN、HNC、NH2+、HNO、KCN、MgCN、MgNC、NH2、N2H+、N2O、NaCN、SiCN、SiNC、C3N、H2CN、HCCN、HCNH+、HNCO、HNCS、NH3、H2CCN、H2CNH、HC3N、HCC-NC、NH2CN、CH3CN、CH3NC、HCONH2、HC4N、CH2CNH、H3CNH2、CH2CHCN、HC4CN、H3CC2CN、CH2CCHCN、CH3CH2CN、CH3CONH2、HC6CN、HC7N、CH3C5N、HC8CN、HC10CN、DCN、DNC、N2D+、NH2D、NHD2、ND3、DCCCN、DC5N
















※コメント投稿者のブログIDはブログ作成者のみに通知されます