中学受験理科に「中和」があります。
アルカリ性と酸性を混ぜ合わせると中性になる、というアレですね。

こんなようなグラフを覚えなきゃ!と頑張っている人もいるみたいですが
こういったものをただ暗記して使っていてもやっぱりピンとこないままですので
今回は考え方の解説をしていきます。
問題でよく使うのは「塩酸」と「水酸化ナトリウム水溶液」です。
「塩酸」は「塩化水素」という酸性の気体が水に溶けた水溶液、
「水酸化ナトリウム水溶液」は「水酸化ナトリウム」というアルカリ性の固体が水に溶けた水溶液です。
イメージとしてはこう。

もちろん溶けている物質は目に見えませんが、こんな感じで水に入ってるんだな、と考えましょう。
この とか
とか の数で、濃さが変わると考えてください。
の数で、濃さが変わると考えてください。
では2つの水溶液を混ぜます。
どちらでもいいのですが、今回は塩酸の入っているビーカーに水酸化ナトリウム水溶液を入れてみます。

2つの水溶液が混ざると、溶けている とか
とか が、新たに現れた物質を見てあらやだあっちの方がいいわ!
が、新たに現れた物質を見てあらやだあっちの方がいいわ!

と反応します。
そしてどちらも相方を捨てて離れてしまい、

それぞれが相方を変えてくっつき合ってしまうのです。

混ぜ合わせた後のビーカーの中の液体には、もともと溶けていた塩化水素 と水酸化ナトリウム
と水酸化ナトリウム はなくなってしまって、代わりに
はなくなってしまって、代わりに と
と が溶けています。
が溶けています。
くっつき合って新しくできた は水、
は水、 は塩化ナトリウム(食塩)です。
は塩化ナトリウム(食塩)です。
水に食塩が溶けているので、これは食塩水ですね。
つまり、塩酸と水酸化ナトリウム水溶液をちょうどいい具合に混ぜ合わせると

↓
中性の食塩水ができあがるのです。
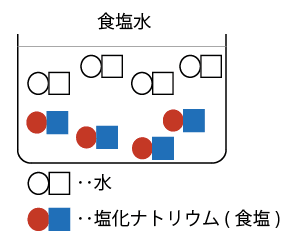
酸性の塩酸とアルカリ性の水酸化ナトリウム水溶液をちょうどいい具合に混ぜ合わせると
中性の食塩水ができることがわかりました。
ではちょうどいい具合に混ぜ合わせなかったら?という疑問がわきますが、それは次回に解説します!
→次回
※解説中の とか
とか とかの図は、中和の考え方をわかりやすくするための図です。
とかの図は、中和の考え方をわかりやすくするための図です。
実際の物質とは多少異なっています。
アルカリ性と酸性を混ぜ合わせると中性になる、というアレですね。

こんなようなグラフを覚えなきゃ!と頑張っている人もいるみたいですが
こういったものをただ暗記して使っていてもやっぱりピンとこないままですので
今回は考え方の解説をしていきます。
問題でよく使うのは「塩酸」と「水酸化ナトリウム水溶液」です。
「塩酸」は「塩化水素」という酸性の気体が水に溶けた水溶液、
「水酸化ナトリウム水溶液」は「水酸化ナトリウム」というアルカリ性の固体が水に溶けた水溶液です。
イメージとしてはこう。

もちろん溶けている物質は目に見えませんが、こんな感じで水に入ってるんだな、と考えましょう。
この
 とか
とか の数で、濃さが変わると考えてください。
の数で、濃さが変わると考えてください。では2つの水溶液を混ぜます。
どちらでもいいのですが、今回は塩酸の入っているビーカーに水酸化ナトリウム水溶液を入れてみます。

2つの水溶液が混ざると、溶けている
 とか
とか が、新たに現れた物質を見てあらやだあっちの方がいいわ!
が、新たに現れた物質を見てあらやだあっちの方がいいわ!
と反応します。
そしてどちらも相方を捨てて離れてしまい、

それぞれが相方を変えてくっつき合ってしまうのです。

混ぜ合わせた後のビーカーの中の液体には、もともと溶けていた塩化水素
 と水酸化ナトリウム
と水酸化ナトリウム はなくなってしまって、代わりに
はなくなってしまって、代わりに と
と が溶けています。
が溶けています。くっつき合って新しくできた
 は水、
は水、 は塩化ナトリウム(食塩)です。
は塩化ナトリウム(食塩)です。水に食塩が溶けているので、これは食塩水ですね。
つまり、塩酸と水酸化ナトリウム水溶液をちょうどいい具合に混ぜ合わせると

↓
中性の食塩水ができあがるのです。

酸性の塩酸とアルカリ性の水酸化ナトリウム水溶液をちょうどいい具合に混ぜ合わせると
中性の食塩水ができることがわかりました。
ではちょうどいい具合に混ぜ合わせなかったら?という疑問がわきますが、それは次回に解説します!
→次回
※解説中の
 とか
とか とかの図は、中和の考え方をわかりやすくするための図です。
とかの図は、中和の考え方をわかりやすくするための図です。実際の物質とは多少異なっています。










※コメント投稿者のブログIDはブログ作成者のみに通知されます