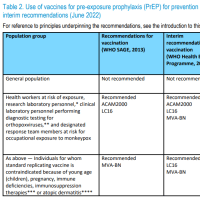
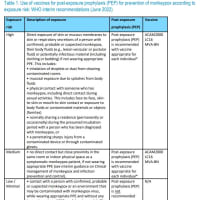
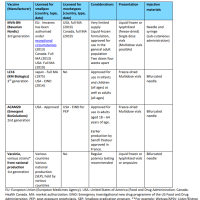
髄膜炎菌は、健常人の鼻腔や咽頭の粘膜に存在し、咳嗽等により人から人へ飛沫感染する。一部の感染者では、本来、無菌状態である血液や髄液に髄膜炎菌が侵襲することにより、敗血症や髄膜炎等の重篤な病態(侵襲性髄膜炎菌感染症)を引き起こすことが知られる。臨床経過としては、風邪と類似した症状で発症した後、急速に(通常24時間以内に)病態が進行増悪し、劇症型(Waterhouse-Friderichsen症候群)と呼ばれる痙攣,意識障害,汎発性血管内凝固症候群等を伴う病態へ移行することがあり、4-20%と致命率が高いことから、「危険な感染症」として広く認識されている。そのため、発生リスク等に応じて、欧米を中心に、定期予防接種等による髄膜炎菌感染症の予防方策がとられている。
髄膜炎菌は0.6~0.8μmのナイセリア属グラム陰性双球菌である。髄膜炎菌は人のみを宿主とし、人の鼻咽頭に定着する。近年では、性行為の多様化によって生殖器からの分離例や関節液や眼脂等、非典型的な患部からの分離例も認められる
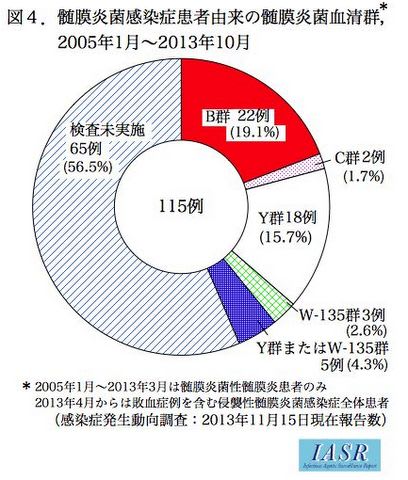
菌は莢膜多糖体の種類により13の血清型(A, B, C, D, X, Y, Z, E, W-135, H, I ,K, L)に分類される、人の感染で同定される血清型はA, B, C, (X), Y, W135の5(6)つが多い(A, B, Cでは流行を認め、人で同定される全体の90%を占める)。
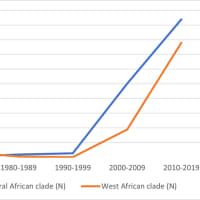
以前、アフリカで主流とされていたA群はアフリカに特化したA群の1価結合型髄膜炎菌ワクチンが2010年に導入されたことで減少し、2015年以降はほとんど見られなくなった。
2016年に髄膜炎ベルト地帯で最も多い髄膜炎菌の血清型はW、続いてCだった(WER Epidemic meningitis control in countries of the African meningitis belt, 2016)。
感染経路は人-人のみ
潜伏期は通常3-4日間(最大10日間)
エアロゾルで感染は拡大し、貧困、高人口密度、不衛生、低栄養でリスクが高い。
咽頭での保菌や喫煙との関連もあり。
米国では細菌性髄膜炎で最も多い原因菌(2500-3500/year)、致死率は13%(Durand ML, NEJM 1993)。
劇症型の場合には、突然発症し、短時間で致命率が高い病態(Waterhouse-Friderichsen 症候群)を取ることがある。
乾季(12-6月)にリスクが高く、髄膜炎ベルトはベナン湾からソマリアにかけて広がるが、アンゴラ、ルワンダ、タンザニア、コンゴでも近年流行が報告される。年間、約3万人の患者が報告される。
代表的な事例としては、サウジアラビアのハッジにおいて、1987年に1841例の大きな流行を認め、1988年には2価(A/C)の莢膜多糖体髄膜炎菌ワクチン接種が全て国からの巡礼者に対して必須となった。その後も100~300例程度の流行を散発的に認めたが、2002年までに4価の多糖体髄膜炎菌ワクチンが2年以上滞在する住民、メッカとメジナへの巡礼者に必須となり、大規模な流行を認めなくなった。
大巡礼はズルヒッジャ(イスラーム暦の12月)の8、9、10日の三日間にわたって行われる[Eurosurveillance, 2013]。
入国する際に接種から10日以上、3年未満の接種証明書の提示が求められる[CDC, Last-Minute Travelers]。
日本における疫学
髄膜炎菌に関連する届け出規定の変遷
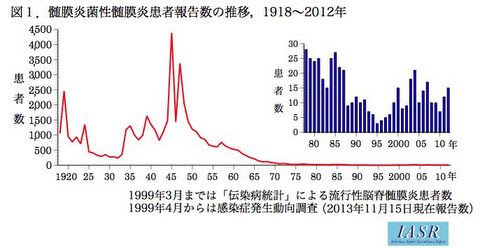
1918年に伝染病予防法により流行脳脊髄膜炎の届出開始開始(法定伝染病)
1999年4月に感染症法の施行により髄膜炎菌性髄膜炎が全数把握疾患(4類感染症)
2003年11月に5類感染症に変更
2013年4月に侵襲性髄膜炎菌感染症として定義が変更
2015年5月より診断後に直ちに(概ね24時間以内)届け出る体制に変更
2013年以降の報告数は、23例、37例、34例、43例、25例と増加した(IDWR年別報告数一覧)。

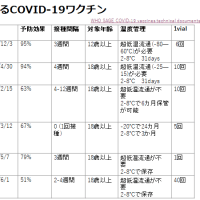
ワクチンは共益ワクチン(Conjugated Vaccine)、多糖類ワクチン(Polysaccharide Vaccine)、遺伝子組み換え蛋白ワクチン(protein-based vaccines)の3種類
ワクチンで発症は予防できるが保菌の予防はできないとされる
免疫原性の違い:
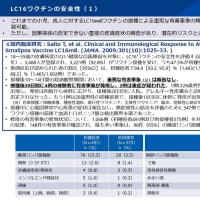
10代100人に接種して両者とも3年後の免疫状態を比較するとW135に関してはMCV4の方が高い(44% VS 21%), CとYでは特に差はなし。
1398人の健康な2歳から10歳までの子供に無作為二重盲検試験で両ワクチンを比較した米国の試験 [Pediatr Infect Dis J 2005 Jan;24(1)]では、両群とも大きな副反応はなかったが、4価の抗体価は全てにおいてMCV4の方が有意に高い(1700 VS 893 for A, 354 VS 231 for C, 637 VS 408 for Y, 750 VS 426 for W135)
MCV4は2~3歳に接種しても2年から3年後にも抗体価を維持できていた[Pediatr Infect Dis J. 2006 Nov;25(11)]
MCV4は乳児に接種してもその効果は弱い[Pediatr Infect Dis J. 2004 May;23(5)]
血清型B型の髄膜炎菌ワクチンについては、B群髄膜炎菌の莢膜多糖体はヒトの脳の糖鎖と構造が酷似しているため、開発が困難であり2013年までワクチンが存在しなかった。しかし、近年の全ゲノム塩基配列の解読および逆ワクチン学により,外膜小胞(outer membrane vesicle)に5種類の表層タンパクを挿入したB群ワクチンが開発されるに到った。
欧州で2013年1月14日にノバルティスの髄膜炎菌 serotype Bに対する不活化ワクチン、Bexsero®をEMAが承認。
米国では2014年10月29日にWyeth Pharmaceuticals, Inc.のTRUMENBAをFDAが承認
続いて、2015年1月23日にNovartis Vaccines and Diagnostics, Inc.のBEXSEROをFDAが承認
米国ACIPは2015年6月12日に10歳以上のハイリスク者に血清型Bの髄膜炎菌ワクチン接種を推奨
英国では2015年9月から1歳未満に定期接種化、JCVIは2016年7月定期接種の対象を拡大して推奨することについては費用対効果や安定供給の問題から否決
血清型B型のワクチンの予防効果は2015年から0-1歳に対して2+1のスケジュールで定期接種を導入した英国での報告では髄膜炎減らす効果があるものの、保菌は減らさず、大学生の流行中に免疫原性からみた効果は限定的との報告もある。
MCV4 (Menactra®, MCV-4 for serotype A, C, Y, W135):Meningococcal conjugate vaccine
ジフテリアトキソイドに結合した4価のMCV4が2005年から米国で接種可能となる。
用法と容量:0.5ml IM, single dose。GBS との関連性が指摘されている。
効果:11~18歳の接種群、19~55歳の接種群を比較すると、約4倍若い群の方が抗体獲得率は高い。成人群ではY型の抗体獲得率がやや低い(74-79%)[Arch Pediatr Adolesc Med 2005 Oct]
ワクチンの適応:
対象は生後9カ月以上から55歳まで(生後9~23カ月の接種が2011年4月にFDAによって認可された)。
2013年8月1日、生後2カ月以上からの接種がFDAに追加承認された(FDA 2013)。
米国での推奨は2-55歳にはMCV-4, 55歳以上にはMPSV-4。
接種方法:
生後9カ月から23カ月の乳幼児においては、0.5mlを3ヶ月間隔で2回、筋肉注射で接種する。2歳から55歳までの小児及び成人においては、0.5mlを1回、筋肉注射で接種する。
米国では11-12歳で1回、16歳で追加接種が実施されている(2014年8月に追加接種の適応が追加された<Vaccine 2016, PMID: 27642132>)。
5年後の追加接種する根拠として、経年的に予防接種後の発症予防効果が減弱することが挙げられる(Pediatrics 2017, PMID: 28100689)
ACIPによる追加接種間隔は7歳未満は3年、7歳以降は5年<MMWR 2013. Table 7>。


MPSV4(Mencevax®, Menomune® for serotype A, C, Y, W135):Meningococcal polysacccharide vaccine
10-55歳ではMCV-4同様に有効だが、2-10歳では免疫原性が弱い。
また接種後3-5年で予防効果が減弱するため追加接種が必要となる。
ただし、追加接種の効果は低いとする報告もある[R Peter, 2000. JID]
局所反応やGBSとの関連性はMCV-4より少ない。
用法と容量:0.5mlの皮下注射で7-10日後から有効。
2007年にACIPは全ての11-18歳(MCV4)、リスクの高い2-10歳にワクチンを推奨。成人に関しては流行地域への旅行者、兵役者、細菌学者等、リスクの高い成人にMCV4 (利用できなければMPSV-4)を推奨。
英国では1999年より全ての幼児にSerotype C のコンジュゲートワクチンを定期接種するようになり、症例数が減少した。
Limitation としてはSerotype B のポリサッカライドワクチンなし、2歳以下での反応が悪い
原因は不明であるが日本での発症は少ない
保菌率も欧米人(30%)と比較して0.4%と低い
日本での髄膜炎の原因菌はインフルエンザ桿菌bが55%、肺炎球菌が19.5%
症例の相談は国立感染症研究所 細菌第一部 高橋英之先生
2000年代初めに実施された、国内の大学生を中心とした健常者の保菌率の調査では、欧米を中心とした海外での保菌率(約5~20%)よりも10倍以上低い約0.4%程度であることが判明している。また、2014年に実施した大学生約800名を対象とした髄膜炎菌の保菌調査でも、それまでの報告と同様に保菌率は約0.8%と低値であることが示された。
学生寮での生活が保菌率上昇のリスクとなる
米国で学生寮での生活を開始後、1週間で保菌率が6.9%(57/825)から23.1%(82/268)に上昇したとの報告あり。
http://www.ncbi.nlm.nih.gov/pubmed?term=10731181
韓国では1カ月間で11.8%(16/136)から14.1%(18/128)に保菌率上昇の報告あり。
http://www.ncbi.nlm.nih.gov/pubmed/22665340
脾摘後のリスクについて
重症化する感染症の病原体として肺炎球菌が最多90% (他に髄膜炎菌、インフルエンザ桿菌)
脾摘患者では免疫グロブリンの産生低下(液性免疫低下)によりオプソニン化できない→マクロファージが貪食能低下→莢膜を持つ細菌に対して重症化(肺炎球菌、髄膜炎菌、インフルエンザ桿菌)
その他、液性免疫低下→Salmonellaや腸内細菌科、Bacteroides、イヌとの接触があればCapnocytophaga canimorsusというGNRのリスクが上昇。ウイルスではエンテロウイルス、原虫ではGiardiaの他、leishmania、trypanosomaの頻度も上昇する。
マラリア罹患との関連性ははっきりしない。
ovewhelming postsplenectomy sepsis (OPSS)は致死率50%以上で小児に多く、致死率も高い
脾摘後最初の1年にリスクが高い
脾症等の液性免疫低下者では免疫原性は、T細胞を介して免疫を誘導するコンジュゲートワクチン(プレベナー7 or 13)の方が高いとされる
http://www.ncbi.nlm.nih.gov/pubmed?term=15747240
曝露後予防
患者との濃厚接触(1m以内で8時間以上や発症から7日以内で抗菌薬開始から24時間未満の患者分泌物と直接接触等)があれば曝露後予防の適応(NEJM, 2006)
曝露後予防は24時間以内に開始することが望ましいが、14日以上経過して開始することは推奨されない(MMWR, 2013)
抗菌薬はリファンピン1200mg2x2day、シプロフロキサシン500mg single dose、セフトリアキソン250mg IM single dose、アジスロマイシン500mg single dose
ただし、曝露後予防が推奨されないような条件での発症事例もあり、高齢者においては紫斑性敗血症や髄膜炎よりも肺炎を生じやすい(Eurosurveillance, 2012)