いよいよシトクロムc(Cyt c)オキシダーゼの登場
 (クリックで拡大)
(クリックで拡大)
図1 Cyt c(Cytochrome c)はナノレベルの電子の運び屋である(PDBID:2B4Z, R=1.5A)。Journal: (2008) Proteins70: 83-92
Cyt c(Cytochrome c)は 図1に示すようにナノレベルの電子の運び屋である。中心にあるFe-ヘムを蛋白が囲み、電子を運ぶ他の多くの蛋白質と同様、つかまえにくい電子を扱うのに特別な補欠分子族(prosthetic group)を持っている。cyt cは、図中では鉄イオンを含むヘム基(heme group)を内側に強くつかんで持っている。この鉄イオンは簡単に電子の取り込みと解放を行う(Fe3+⇔Fe2+)。そして周りの蛋白質は、どれだけしっかり電子をつかんでいるかを調整し、電子にとって完全な環境を作り出す。また、cyt cが細胞の電子回路全体におけるどの位置に当てはまるかについても決めている。
cyt cは古代よりある蛋白質で、生命進化の早い段階に発達した。この必須蛋白質は、細胞の動力生産において重要な段階を担っており、ここ数百万年の間ほとんど変化してこなかった。従って、酵母、植物、そして我々の細胞どれを探しても非常に似た型のcyt cが見つかる。PDBを検索すると、他にも様々な電子運搬分子があることが分かる。cyt cには様々な変異があり、いずれも電子運搬にはヘムと鉄イオンを使うが、担当する仕事の違いに応じて電子を囲む蛋白質を変化させている。他の電子運搬体はまた別の補欠分子族を使って電子を運んでいる。そのような補欠分子族としては、フェレドキシン(ferredoxin)で使われている鉄硫黄クラスター(iron-sulfur cluster)や、アズリン(azurin)やプラストシアニン(plastocyanin)で使われる銅イオンのほか、より珍しい金属イオンを使ったものも存在する。cyt cのように、これらの蛋白質もそれぞれ単独で細胞電子回路に接続していて、ある地点から別の地点へ電子を運搬している。
図2a cyt c オキシダーゼ(1OCC)のサブユニットをchem3Dで拡大した図。ヘム骨格が2個垣間見える。
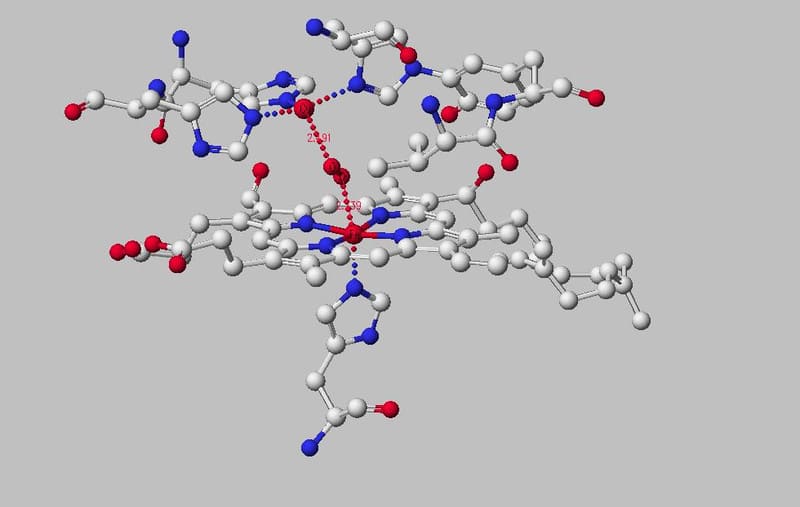
図2b cyt cオキシダーゼの活性中心における酸素分子の構造。PDBID:2Y69の酸素分子を中心にして、5A以内の隣接group を図示した(使用ソフトはCAChe)。
他方、Cyt c oxidaseは図2に示すようにいくつかの金属補欠分子族部位と13のタンパク質サブユニットから構成される巨大な内在性膜タンパク質である。10個のサブユニットは核由来で、残りの3個はミトコンドリアで合成される。cyt c oxidaseには2種のヘム(ヘムa 、ヘムa 3)、2種の銅中心(CuAとCuB)が含まれている。前者はサブユニットIに位置し、後者はサブユニットIIに配位している。サブユニットIのヘムa 3とCuBはそれぞれで二核中心を形成し、酸素の還元部位となっている。cyt c は、複合体IIIのシトクロムc 1によって還元された後、複合体IVのCuA二核中心と結合し、cyt c の鉄中心はFe2+からFe3+に酸化される。還元されたCuA二核中心はその電子をヘムa に送り、さらにそこからヘムa 3-CuB二核中心に送られる。この二核中心の2個の金属イオンは4.5 Å離れており、十分な酸化状態の水酸化物イオンに配位している。cyt c の結晶学的研究では、Tyr(244)のC6とHis(240)のε-Nが結合するという独特な翻訳後修飾が見られる。これにより、ヘムa 3-CuB二核中心が4電子を受け取って酸素分子を水に還元するという極めて重要な役割が可能になっている。
反応の概要をまとめると:
4 Fe2+-cyt c + 8 H+in + O2 → 4 Fe3+-cyt c + 2 H2O + 4 H+out
となる。まず、2個の電子がcyt cから、CuA二核中心とヘムa を通過して、ヘムa 3-CuB二核中心に至り、このFe3+はFe2+に、Cu2+はCu+に還元される。このときそれぞれの金属イオンに配位していたヒドロキシル配位子はプロトン化されて水として失われ、金属間に酸素分子が入る空間が作られる。酸素はFe2+-cyt c由来の2電子により迅速に還元され、フェリオキソ型(Fe+4=O)に変換される。CuB側の酸素原子はCu+からの1電子と、約4Å離れたTyr(244)の由来の1電子と1プロトンを受け取り、ヒドロキシ配位子に変換される。このときTyr(244)はチロシルラジカルとなる。別のcyt c から発生する3番目の電子は始めの2種の電子キャリアーからヘムa 3-CuBに至り、この電子と2プロトンによりチロシルラジカルがチロシンに戻り、そしてヒドロキシドはCuB2+に結合し後に水分子となる。同様に4番目の電子も始めの2種の電子キャリアーからヘムa 3-CuBに至ることによりFe+4=OがFe+3に還元され、同時に酸素原子がプロトンを受け取り、ヘムa 3-CuBがこのサイクルの始めの状態に戻る。まとめると、4分子の還元型cyt c と4個のプロトンが用いられ酸素分子を2分子の水に還元していることになる。
図3 図1の活性中心における酸素分子とチロシン(Y244:図の左上)の配置。
<問合せ先>: ◎ラジカルのことならキーコム。出張測定可!
キーコム(株)
〒170-0005 東京都豊島区南大塚3-40-2
KEYCOM Corp. 3-40-2 Minamiotsuka,Toshima-ku Tokyo 170-0005 Japan
TEL:+81-3-5950-3101, FAX:+81-3-5950-3380
Home Page: http//www.keycom.co.jp/
E-mail: ohya@keycom.co.jp