昨年11月のNew Eng J Med誌に,フランスにおける脂肪酸アミド加水分解酵素(FAAH)阻害剤の臨床試験(治験)の第一相試験において,重篤な神経障害が出現し,死亡者が出たという報告がなされた.画像所見に驚いたことに加え,私も脳卒中の治療薬の開発を目指し,第一相試験は徐々に視野に入りつつあるため,大きな関心を持って本論文と関連する文献を年末年始に読んでみた.考察を踏まえて紹介したい.
【第一相試験の基礎知識】
基礎研究で期待できる創薬シーズが見つかったあと,次に行なうのが非臨床試験である.これは薬理学的試験,薬物動態試験,毒性試験に大別される.経験的に,アカデミアで論文発表のために行われる実験よりはるかに精度の高い細かい実験データが求められる.この非臨床試験の結果,有効性が期待でき,安全性にも問題がないと考えられた場合,人で行なわれるのが臨床試験(治験)である.治験は3つのフェーズに大別され,第一相が臨床薬理試験,第二相が探索的試験,第三相が検証的試験である.第一相試験は,主に健康な成人ボランティアを対象として,治験薬の安全性・忍容性および薬物の体内動態について確認するためのものである.この段階で初めて人体に投与されるため,First-in-Human(FIH)試験と呼ばれる.FIH試験に進むためには,非臨床試験のうち,安全性薬理試験,薬物動態試験,反復投与毒性試験,遺伝毒性試験,がん原性試験,生殖発生毒性試験を行なう必要がある.第一相試験の試験デザインとしては,用量漸増試験が一般的に行われる.
臨床試験に関する詳細を学ぶために,以下の書籍は分かりやすく,お薦めしたい.
臨床試験ベーシックナビ―クリニカルクエスチョンにこたえる!
医師主導治験 STARTBOOK
またICH E8(臨床試験の一般指針)もぜひ確認していただきたい.
【第一相試験における過去の重大事故:TGN1412事件】
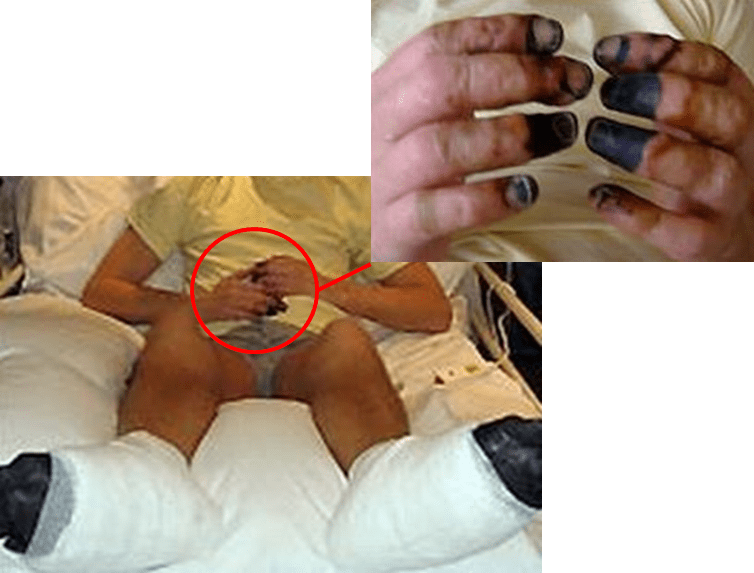
第一相試験で重大な有害事象が生じた事件として,英国で2006年に行われたTGN1412(T細胞表面のCD28に結合するスーパーアゴニスト抗体)の治験が有名である.健常ボランティア8例のうち実薬投与を受けた6人全員が,重篤なサイトカイン・ストームを引き起こし,多臓器不全に陥り,一時は全員が集中治療室に入った.幸い,全員退院したが,1人は壊死によって手指を切断されるに至った(図).英国医薬品庁(MHRA)は最終調査報告で,開発過程での過失は認められないと結論づけた.しかし,無過失と結論づけたため,再発予防はどうしたら良いのかという混乱が生じた.またなぜ6人同時にテストしたか,どうしてまずは1人から始めなかったのかという批判はあった.
原文(PDFフリーダウンロード)
【FAAH阻害薬とその神経合併症】
脂肪酸アミド加水分解酵素(fatty acid amide hydrolase:FAAH)はその活性が低下すると,内因性カンナビノイドの量が増加する.カンナビノイドは大麻(cannabis)が含む多数の生理活性物質の総称である.このFAAHを阻害する薬剤は,内因性カンナビノイドの作用により,動物モデルで鎮痛作用および抗炎症作用を示し,鎮痛剤や抗うつ剤としての臨床応用が期待されている.そしてFAAH阻害剤の一部は,すでに第一相試験,第二相試験が行われている.
今回の論文は,ポルトガルのBial社が開発した可逆的経口FAAH 阻害薬BIA 10-2474を,フランスのレンヌ大学において健常ボランティアに投与した結果を,治験担当医師が報告したものである.まずこの薬剤は,単回投与(0.25~100 mg)と反復投与(2.5~20 mg を 10 日間)が行われ,健常ボランティア計84例に投与された.この結果,重度の有害事象は報告されなかった(詳細は記載なし).このため,別のコホートを募り,プラセボ(2 例)と,BIA 10-2474投与群(6 例)に割り付け,50 mg/日の反復投与が行われた.後者の6 例のうち 4 例から,臨床・画像データを公表する同意が得られた.
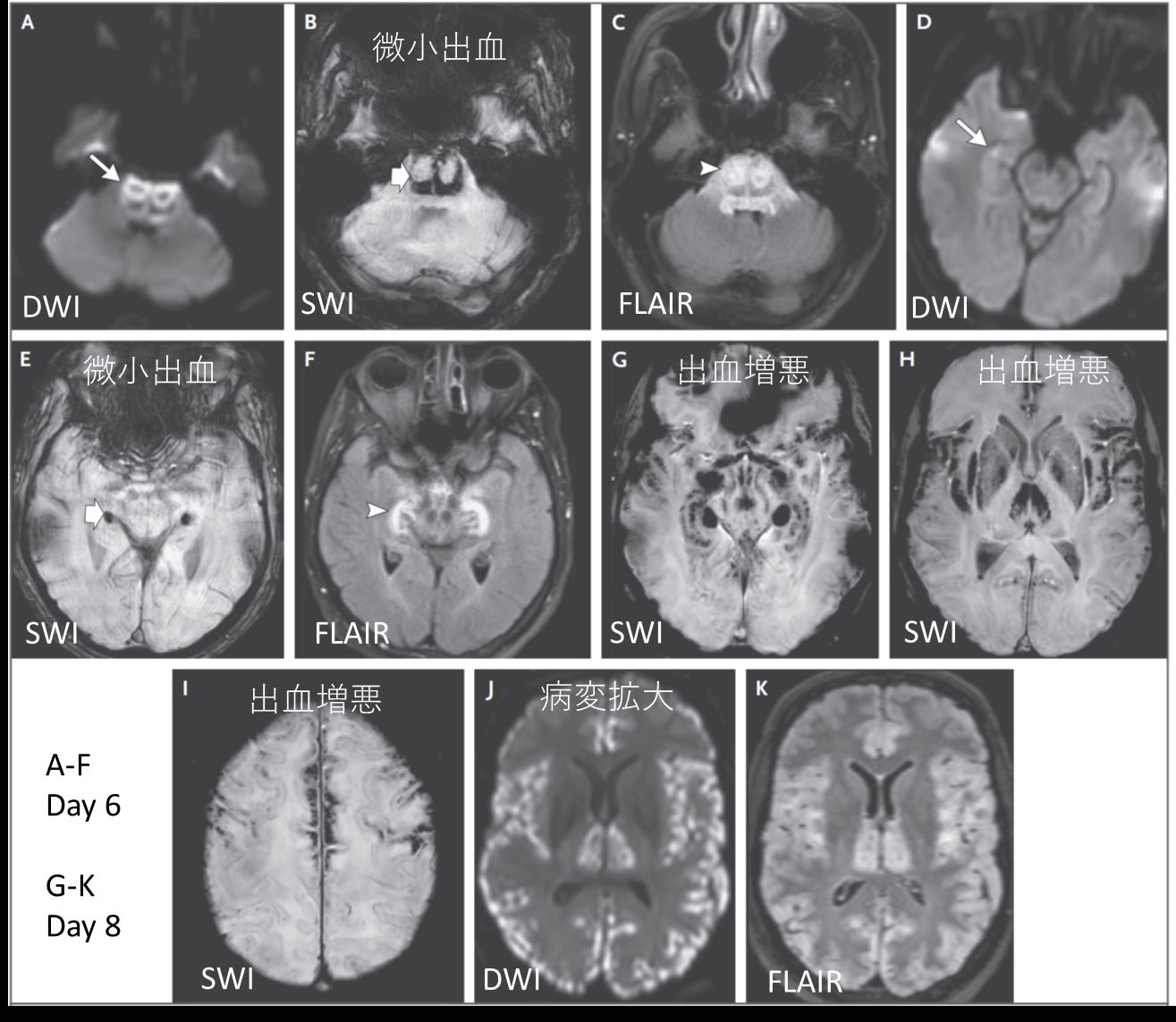
投与開始 5 日目より,4例中3 例に急速進行性の神経障害が出現した.具体的には,頭痛,小脳症候群,記憶障害,意識障害がみられた.図は症例1の投与6および8日目の頭部MRIであるが,橋や海馬を中心に,両側左右対称性に異常信号病変と微小出血が,急速に拡大する重篤な病変であることが分かる.ちなみにカンナビノイド受容体は海馬には存在するが,橋にはないため,これらの病変は内在性カンナビノイド系の分布とは一致しなかった.この症例1は脳死と判定され,その後,剖検がなされたが,著者らには結果が開示されず,論文に記載はない.残りの2例は症状は回復を認めたものの,1 例は記憶障害が残存,もう 1 例は小脳症候群が残存した.この中枢神経障害の発症機序は不明であると記載されている.
論評を読むと,結果的に6例中1例が死亡,4例に重篤な神経障害が見られたようだ.Bial社は,第一相試験に参加した複数のボランティアが深刻な副作用を被ったことに後悔の意を表明し,また同じFAAH阻害薬であるJNJ-42165279の第二相試験を行っていたジョンソン・エンド・ジョンソン社も試験を中断した.
【この悲劇的な出来事から何を学ぶべきか?】
本臨床試験の失敗は,非常に大きな衝撃を関係者に与え,同じ号のNew Eng J Med誌ではEuropean Medicines AgencyのSergio Boniniが論評を,また米国神経学会のNeurology Today紙にも特集記事が掲載された.論点をまとめると以下の3点になるだろう.
1.情報の開示の問題
まず十分な情報が開示されていないという問題がある.同意の得られなかった2例については臨床情報の記載がなく,また死亡例の剖検所見は治験担当医に開示されず,論文にも記載はなかった.さらに論文の前半部の健常ボランティア計84例に投与した臨床情報が「重篤な副作用はなかった」とあるだけで,重篤でない副作用を含め,ほとんど記載されていない.
情報が開示されなかった理由は2つあり,「薬剤開発における商業的利益の保持」と「個人情報開示の不同意」の問題である.しかし「公共の利益」に関わる重要な問題であることから,上記の2つの権利は制限され,遅滞することなく情報を開示すべきであるという考えもある.
2.治験をいつ中止するかという問題
この研究で一番の問題は,最初の症例に重篤な症状が出たあとすぐに,試験を中止しなかったことである.臨床試験に携わる医師は,試験を完遂することに努力するだけではなく,臨床的な常識を用いて,中止すべきときは中止をする必要があるということだ.しかしそのために,治験に関わる医師は治験薬の効果と安全性について十分理解する必要がある.しかし,第一相試験前の非臨床データが発表されることは稀で,共有されないことが多い.健常ボランティアや患者さんを守るためには,十分な情報の共有が必要である.また被害を最小限にするためには,すべての参加者に同時に治験薬を投与するのではなく,ずらして重ならないようにすることも大切である.
3.いかに治験参加者を守るかという問題
臨床試験ではまず安全性(リスク),つぎに効果(ベネフィット)の評価が行われ,その結果として,リスク・ベネフィット比を求め,治験薬の有用性を判断する.しかし,第一相試験は,健常ボランティアに行なうため,当然,何の効果も期待できず,ただ単にリスクのみ生じうるものだ.よって情報の開示とセーフガードがない限り,倫理的に認められない試験と言える.
ではどのように安全性を確保すべきか?非臨床面では,治験薬の薬理動態や毒性試験のデータより,最小推奨初回投与量をいかに決定するか,増量の方法や間隔はどのように決めるかの議論が必要である.一方,臨床面では,安全性に関連して,用量増量を許可するときのルールや,2で述べた研究中止のルールが重要である(本試験でも50mgという用量に進む前の試験で何が分かっていたのかは重要である).また投与方法や食事,健常ボランティアの年齢の影響も重要である.
基本的に,第一相試験のリスクは必ずしも高いものではなく,2005年以降EUで行われた3100の第一相試験で副作用が重篤と判定されたのは2試験(0.064%)とのことである.しかし,第一相試験での有害事象はあってはならないものであり,さらに減らすための戦略を検討する必要がある.その意味で基礎・臨床の研究者が今回の報告から学ぶべきことは多い.アカデミア基礎研究者の立場としては,単に治療効果を動物モデルで示すのみならず,その作用機序を徹底的に解明することは副作用の防止につながるだろう.また自身の経験を振り返ると,安全性より有効性の証明を優先しがちであることが問題と思われる(有効性のほうが論文に書きやすいため).一方,治験を行なう臨床医の立場としては,必ずしも治験薬の情報や作用機序を理解していないことや,いざという時にボランティアや患者さんの安全を守る行動を迅速に取れるかということが問題として考えられる.経験的に,有害事象の早期の段階で,治験を中断するのは勇気がいる.加えて,基礎と臨床の両者の連携,情報交換も重要と言えるだろう.
Kerbrat A et al. Acute Neurologic Disorder from an Inhibitor of Fatty Acid Amide Hydrolase. N Engl J Med. 2016 Nov 3;375(18):1717-1725.
【第一相試験の基礎知識】
基礎研究で期待できる創薬シーズが見つかったあと,次に行なうのが非臨床試験である.これは薬理学的試験,薬物動態試験,毒性試験に大別される.経験的に,アカデミアで論文発表のために行われる実験よりはるかに精度の高い細かい実験データが求められる.この非臨床試験の結果,有効性が期待でき,安全性にも問題がないと考えられた場合,人で行なわれるのが臨床試験(治験)である.治験は3つのフェーズに大別され,第一相が臨床薬理試験,第二相が探索的試験,第三相が検証的試験である.第一相試験は,主に健康な成人ボランティアを対象として,治験薬の安全性・忍容性および薬物の体内動態について確認するためのものである.この段階で初めて人体に投与されるため,First-in-Human(FIH)試験と呼ばれる.FIH試験に進むためには,非臨床試験のうち,安全性薬理試験,薬物動態試験,反復投与毒性試験,遺伝毒性試験,がん原性試験,生殖発生毒性試験を行なう必要がある.第一相試験の試験デザインとしては,用量漸増試験が一般的に行われる.
臨床試験に関する詳細を学ぶために,以下の書籍は分かりやすく,お薦めしたい.
臨床試験ベーシックナビ―クリニカルクエスチョンにこたえる!
医師主導治験 STARTBOOK
またICH E8(臨床試験の一般指針)もぜひ確認していただきたい.
【第一相試験における過去の重大事故:TGN1412事件】
第一相試験で重大な有害事象が生じた事件として,英国で2006年に行われたTGN1412(T細胞表面のCD28に結合するスーパーアゴニスト抗体)の治験が有名である.健常ボランティア8例のうち実薬投与を受けた6人全員が,重篤なサイトカイン・ストームを引き起こし,多臓器不全に陥り,一時は全員が集中治療室に入った.幸い,全員退院したが,1人は壊死によって手指を切断されるに至った(図).英国医薬品庁(MHRA)は最終調査報告で,開発過程での過失は認められないと結論づけた.しかし,無過失と結論づけたため,再発予防はどうしたら良いのかという混乱が生じた.またなぜ6人同時にテストしたか,どうしてまずは1人から始めなかったのかという批判はあった.
原文(PDFフリーダウンロード)

【FAAH阻害薬とその神経合併症】
脂肪酸アミド加水分解酵素(fatty acid amide hydrolase:FAAH)はその活性が低下すると,内因性カンナビノイドの量が増加する.カンナビノイドは大麻(cannabis)が含む多数の生理活性物質の総称である.このFAAHを阻害する薬剤は,内因性カンナビノイドの作用により,動物モデルで鎮痛作用および抗炎症作用を示し,鎮痛剤や抗うつ剤としての臨床応用が期待されている.そしてFAAH阻害剤の一部は,すでに第一相試験,第二相試験が行われている.
今回の論文は,ポルトガルのBial社が開発した可逆的経口FAAH 阻害薬BIA 10-2474を,フランスのレンヌ大学において健常ボランティアに投与した結果を,治験担当医師が報告したものである.まずこの薬剤は,単回投与(0.25~100 mg)と反復投与(2.5~20 mg を 10 日間)が行われ,健常ボランティア計84例に投与された.この結果,重度の有害事象は報告されなかった(詳細は記載なし).このため,別のコホートを募り,プラセボ(2 例)と,BIA 10-2474投与群(6 例)に割り付け,50 mg/日の反復投与が行われた.後者の6 例のうち 4 例から,臨床・画像データを公表する同意が得られた.
投与開始 5 日目より,4例中3 例に急速進行性の神経障害が出現した.具体的には,頭痛,小脳症候群,記憶障害,意識障害がみられた.図は症例1の投与6および8日目の頭部MRIであるが,橋や海馬を中心に,両側左右対称性に異常信号病変と微小出血が,急速に拡大する重篤な病変であることが分かる.ちなみにカンナビノイド受容体は海馬には存在するが,橋にはないため,これらの病変は内在性カンナビノイド系の分布とは一致しなかった.この症例1は脳死と判定され,その後,剖検がなされたが,著者らには結果が開示されず,論文に記載はない.残りの2例は症状は回復を認めたものの,1 例は記憶障害が残存,もう 1 例は小脳症候群が残存した.この中枢神経障害の発症機序は不明であると記載されている.
論評を読むと,結果的に6例中1例が死亡,4例に重篤な神経障害が見られたようだ.Bial社は,第一相試験に参加した複数のボランティアが深刻な副作用を被ったことに後悔の意を表明し,また同じFAAH阻害薬であるJNJ-42165279の第二相試験を行っていたジョンソン・エンド・ジョンソン社も試験を中断した.

【この悲劇的な出来事から何を学ぶべきか?】
本臨床試験の失敗は,非常に大きな衝撃を関係者に与え,同じ号のNew Eng J Med誌ではEuropean Medicines AgencyのSergio Boniniが論評を,また米国神経学会のNeurology Today紙にも特集記事が掲載された.論点をまとめると以下の3点になるだろう.
1.情報の開示の問題
まず十分な情報が開示されていないという問題がある.同意の得られなかった2例については臨床情報の記載がなく,また死亡例の剖検所見は治験担当医に開示されず,論文にも記載はなかった.さらに論文の前半部の健常ボランティア計84例に投与した臨床情報が「重篤な副作用はなかった」とあるだけで,重篤でない副作用を含め,ほとんど記載されていない.
情報が開示されなかった理由は2つあり,「薬剤開発における商業的利益の保持」と「個人情報開示の不同意」の問題である.しかし「公共の利益」に関わる重要な問題であることから,上記の2つの権利は制限され,遅滞することなく情報を開示すべきであるという考えもある.
2.治験をいつ中止するかという問題
この研究で一番の問題は,最初の症例に重篤な症状が出たあとすぐに,試験を中止しなかったことである.臨床試験に携わる医師は,試験を完遂することに努力するだけではなく,臨床的な常識を用いて,中止すべきときは中止をする必要があるということだ.しかしそのために,治験に関わる医師は治験薬の効果と安全性について十分理解する必要がある.しかし,第一相試験前の非臨床データが発表されることは稀で,共有されないことが多い.健常ボランティアや患者さんを守るためには,十分な情報の共有が必要である.また被害を最小限にするためには,すべての参加者に同時に治験薬を投与するのではなく,ずらして重ならないようにすることも大切である.
3.いかに治験参加者を守るかという問題
臨床試験ではまず安全性(リスク),つぎに効果(ベネフィット)の評価が行われ,その結果として,リスク・ベネフィット比を求め,治験薬の有用性を判断する.しかし,第一相試験は,健常ボランティアに行なうため,当然,何の効果も期待できず,ただ単にリスクのみ生じうるものだ.よって情報の開示とセーフガードがない限り,倫理的に認められない試験と言える.
ではどのように安全性を確保すべきか?非臨床面では,治験薬の薬理動態や毒性試験のデータより,最小推奨初回投与量をいかに決定するか,増量の方法や間隔はどのように決めるかの議論が必要である.一方,臨床面では,安全性に関連して,用量増量を許可するときのルールや,2で述べた研究中止のルールが重要である(本試験でも50mgという用量に進む前の試験で何が分かっていたのかは重要である).また投与方法や食事,健常ボランティアの年齢の影響も重要である.
基本的に,第一相試験のリスクは必ずしも高いものではなく,2005年以降EUで行われた3100の第一相試験で副作用が重篤と判定されたのは2試験(0.064%)とのことである.しかし,第一相試験での有害事象はあってはならないものであり,さらに減らすための戦略を検討する必要がある.その意味で基礎・臨床の研究者が今回の報告から学ぶべきことは多い.アカデミア基礎研究者の立場としては,単に治療効果を動物モデルで示すのみならず,その作用機序を徹底的に解明することは副作用の防止につながるだろう.また自身の経験を振り返ると,安全性より有効性の証明を優先しがちであることが問題と思われる(有効性のほうが論文に書きやすいため).一方,治験を行なう臨床医の立場としては,必ずしも治験薬の情報や作用機序を理解していないことや,いざという時にボランティアや患者さんの安全を守る行動を迅速に取れるかということが問題として考えられる.経験的に,有害事象の早期の段階で,治験を中断するのは勇気がいる.加えて,基礎と臨床の両者の連携,情報交換も重要と言えるだろう.
Kerbrat A et al. Acute Neurologic Disorder from an Inhibitor of Fatty Acid Amide Hydrolase. N Engl J Med. 2016 Nov 3;375(18):1717-1725.